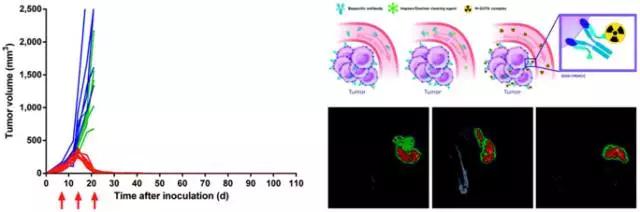
左:肿瘤生长呈现在每只小鼠的肿瘤体积随时间变化(绿色:无治疗;蓝色:仅177Lu-DOTA-Bn only治疗;红色:DOTA-PRIT治疗)。右上角:抗GPA33 DOTA-PRIT三步法的示意图。右下角:在第1周期注射24小时后从小鼠身上获得的代表性SPECT / CT图像。(S Cheal et al., Memorial Sloan Kettering Cancer Center, New York, NY)
纪念斯隆凯特灵癌症中心及麻省理工学院的研究人员新研发出一种三步系统,利用核药物来锁定和消除结直肠癌。研究人员在小鼠模型中得到100%的无进展生存率,且没有任何与治疗相关的毒性效应。这项研究报告发表在11月的《核医学杂志》上。
到目前为止,使用抗体靶向放射性核素治疗实体肿瘤的放射免疫治疗(靶向治疗)疗效有限。“这是项新颖的研究,其在治疗肿瘤剂量方面,是对人体正常组织的非毒性二次辐射。”Steven m . Larson及Sarah Cheal博士解释道,“小鼠肿瘤模型成功一方面源自团队开发试剂的独特质量,另一方面源自减少实践方法,包括一种可以很容易转移到病人身上的治疗诊断方法。”这种方法运用单一药物来诊断和治疗疾病。药物首先发现癌细胞,然后摧毁它们,使健康细胞不受伤害,通过这种方式减少副作用,改善病人的生活质量。
本研究中,糖蛋白A33(GPA33)用以识别A33肿瘤抗原。在小鼠模型上测试 DOTA-pretargeted放射免疫疗法(PRIT)。对随机选择的受试小鼠,用SPECT / CT成像来监测治疗反应,并计算肿瘤的辐射吸收剂量。受试小鼠反应良好,被评估的小鼠在显微镜下均未发现癌症迹象,包括骨髓和肾脏在内的关键器官未见明显的辐射损伤。
小鼠模型中100%的无进展生存率是一个可喜的发现,表明抗GPA33-DOTA-PRIT 将成为GPA33阳性结肠直肠癌的一种有效的放射免疫治疗方案。
根据疾控中心的数据,结直肠癌是影响男性和女性的第三种最常见癌症。在美国,每年大约有140000例新发病例,并造成5万人死亡。
推荐阅读:结直肠癌基因检测







































 首页
首页 咨询
咨询 方舟新药
方舟新药 营养商城
营养商城