17年8月30日,杨森公司宣布 CFDA 批准依鲁替尼胶囊,用于单药治疗既往至少接受过一种治疗的慢性淋巴细胞白血病(CLL)/ 小淋巴细胞淋巴瘤(SLL)、套细胞淋巴瘤患者。
依鲁替尼是全球第一个上市的 BTK 抑制剂,由强生和 Pharmacyclics 合作开发,最早是于 2013/11/13 获得 FDA 批准上市,上市之后销售额突飞猛进,由此也引起了 AbbVie 的巨大兴趣。AbbVie 于 2015 年 3 月斥资 210 亿美元重金收购了 Pharmacyclics,获得了依鲁替尼的美国市场商业权利。强生则拥有依鲁替尼在全球其他国家的商业权利。2016 年强生和 AbbVie 合计销售收入 30.83 亿元,2017 上半年,强生和 AbbVie 合计销售收入 20.36 亿美元。
强生最早于 2013/9/6(CDE 承办时间)在中国提交了依鲁替尼的注册申请,2016/11/ 7 提交了生产申请,2016/12/ 2 获得以“与现有治疗手段相比具有明显治疗优势”的理由被 CDE 纳入优先审评,2017/8/28 获得 CFDA 颁发的生产批件。依鲁替尼在中国上市申请的整个审评周期大约 10 个月,最终上市时间比美国晚了大约 4 年。
ASH2016 大会上曾公布过依鲁替尼的两项 5 年随访研究结果,均显示 CLL/SLL 患者越早使用依鲁替尼,生存获益越大(见:依鲁替尼 5 年随访数据公布:越早使用,生存获益越大),依鲁替尼在中国获批上市是中国患者的福音。
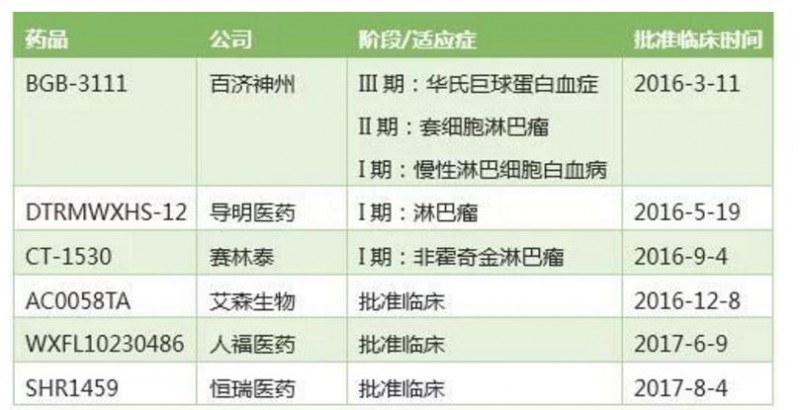
强生之外,国内目前共有其他 6 家公司的 BTK 产品向 CDE 注册申报,且均已获批临床。特别是百济神州的 BGB-3111,已经推进到了 III 期阶段。国内外在研的 BTK 抑制剂信息如下:
国内申报注册的 BTK 抑制剂







































 首页
首页 咨询
咨询 方舟新药
方舟新药 营养商城
营养商城