根据俄亥俄州立大学综合癌症中心最近开展的一项研究,发现150年前首次发现并用作平滑肌松弛剂的药物可能会使肿瘤对放射治疗更加敏感。
这种名为罂粟碱的药物可以抑制线粒体的呼吸,消耗氧气和产生能量,可以使模型肿瘤对放疗敏感,且该药物不会影响正常组织对放疗的敏感性。
此外,研究人员表明,修饰罂粟碱分子可能会提高分子的安全性,可能成为一类新的放射增敏药物,且副作用较少。细胞缺氧限制了放射治疗的有效性,这是一个严重的临床问题,超过一半的癌症患者需要接受放疗。研究发现在放射治疗前服用一剂罂粟碱可以减少线粒体呼吸,减轻缺氧,并大大增强模型肿瘤对放疗的反应。
放疗以两种方式杀死癌细胞:一直接破坏DNA,二间接地通过产生被称为氧自由基的反应性损伤分子。细胞缺氧减少了放疗诱导的DNA损伤和有效毒性。
“如果肿瘤缺氧区域的恶性细胞能够在放射治疗中存活,它们就会成为肿瘤复发的根源,”Denko说。 “我们必须找到克服这种治疗形式的方法,这一点至关重要。”
Denko说,克服辐射抗性的策略通常侧重于为肿瘤提供更多的氧气。 “但这些尝试几乎没有取得临床成功,因为肿瘤的血管系统形成不良,”他补充道。 “我们采取了相反的方法。我们不是试图增加氧气供应,而是减少氧气需求,这些研究结果表明罂粟碱或衍生物是一种很有前途的代谢放射增敏剂。”
2、一滴血就知道O药(nivolumab)治疗肺癌有没有效
日本Tasuku Honjo博士因发现免疫T细胞蛋白PD-1而获得2018年诺贝尔生理学或医学奖。这一发现导致了一系列称为检查点抑制剂的抗癌药物,其中第一种是nivolumab(纳武单抗,Opdivo)。
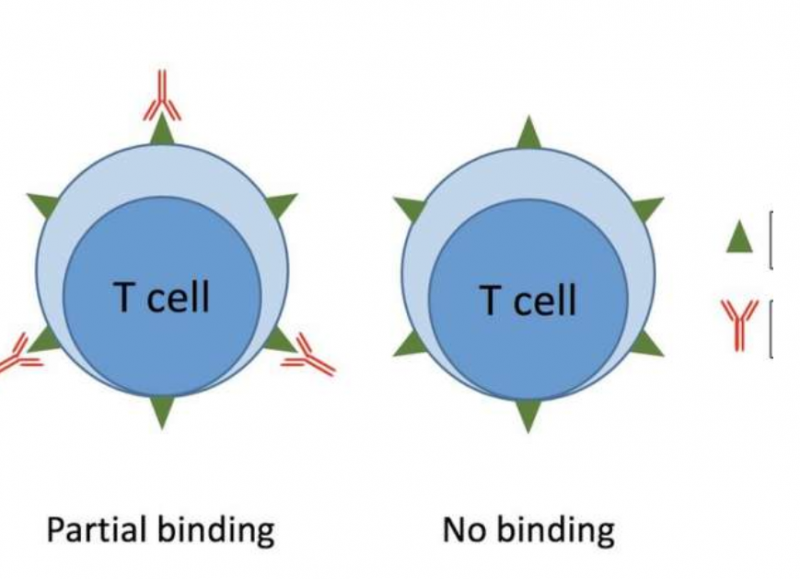
Nivolumab帮助T细胞对抗肿瘤,然而,不同的患者应答结果不同。现在看来,用简单和新颖的方法监测nivolumab对关键免疫细胞的影响可能有助于指导优化治疗的决策。
Shohei Koyama博士和大阪大学的一组研究人员设计了一种简单的方法来测试nivolumab在体内的影响。该方法测量nivolumab在治疗后数周内如何与T细胞上的PD-1结合,并且可以提供更有效地监测治疗所需的信息。《JCI Insight》上发表。
研究人员分析了肺癌患者血液和肺液的微小样本,测量了与T细胞结合的nivolumab的量,分离了与nivolumab结合的那些T细胞以全面分析细胞活化。
研究人员发现,nivolumab对T细胞的作用通常在给药后相当长的时间内持续存在于患者体内。
“我们的简化方法在现实世界的患者中是可行的,并且证明即使在患者停止治疗后,nivolumab也能够将T细胞结合20周以上,”该研究的共同作者Atsushi Kumanogoh说。 “此外,nivolumab停止结合T细胞的血浆浓度和结合T细胞的百分比因患者而异。”
他们的发现也证实了T细胞结合水平并不表明该药物的功能效果,需要进一步测量T细胞增殖情况。我们需要测量与T细胞结合的nivolumab的量和T细胞增殖的程度以做出治疗决定,只需一滴血即可实现。”
两位研究参与者的结果说明了测量增殖和T细胞结合的重要性。当增殖低时,第一位患者没有反应。相反,当增殖较高时,第二名患者未显示肿瘤生长。
“我们的监测nivolumab结合和T细胞增殖状态的组合策略,是一种更好的方法来确定这种药物的效果,而不是单独监测nivolumab的血液水平,”共同作者Takeshi Uenami说。
总体而言,了解患者nivolumab随时间持续存在的效果可能有助于预防治疗相关的副作用并指导其他疗法的选择。
3、见光死?乳腺癌新疗法——光介导精准靶向肿瘤
转移性乳腺癌预后令人沮丧。辛辛那提癌症中心Nalinikanth Kotagiri医学博士希望研究紫外线通过激活光敏药物的方法来治疗这个问题。Kotagiri已被授予国防部乳腺癌突破奖,三年超过600,000美元。他的项目将重点放在光介导疗法上,这种疗法可以激活光敏药物,且仅靶向癌细胞。
通过用放射性核素作为'内部'光源的光替换外部光源-如激光和灯,我们已经能够更好地控制体内治疗。这可能意味着更有效的治疗方法,对重要器官和组织的毒性最小。由于放射性核素可用于成像和定位肿瘤,我们现在可以使用相同的放射性核素同时成像和治疗乳腺癌转移。
这有可能成为一种常见的影像引导治疗策略,用于治疗疾病早期和晚期的患者,安全性高,它可以与其他治疗方法一起有效地使用,如化疗和免疫疗法,没有额外副作用的风险。这可以极大地使患者受益,因为除了开创其他FDA批准的光敏药物作为放射性核素激活疗法的先例之外,它还可以改善治疗效果,扩大这些药物目前治疗的疾病的范围,更重要的是癌症患者又多了一项治疗选择。

4、睡美人技术识别肝癌的治病基因
日本大阪的研究人员发现,在人类基因组中约有二万个蛋白质编码基因,精确定位一种疾病的特定基因就像在干草堆中寻找针头一样难,对于肝细胞癌(HCC)来说更是如此。本研究确定了HCC患者癌症基因组中超过一万个突变,开发靶向治疗也显得异常困难。
HCC属于世界上第二大致命的癌症类型,每年诊断出患有HCC的患者人群正在增多。这类肝癌的一个主要新兴风险因素,特别是在西方国家,是非酒精性脂肪肝病(NAFLD),其特征是肝脏中脂肪储存过多。与高脂肪饮食和2型糖尿病相关,NAFLD对肝脏造成的损害程度不次于严重酗酒。
大阪大学的研究小组着手确定推动NAFLD-HCC发展的基因。利用一项新技术,通过大规模筛查导致与脂肪肝相关的肝癌发展的基因和信号转导途径,全面检索个体动物中的致癌基因。这项新技术涉及小的,可移动的DNA序列,迷人地命名为睡美人转座子。在两个独立的NAFLD小鼠模型中随机整合到基因组中。转座子插入破坏通常参与肿瘤抑制或激活附近癌基因,使研究人员能够通过受影响小鼠中加速或过度的肝肿瘤发展来鉴定潜在的HCC致病基因。
主要作者Takahiro Kodama说,“在数百个候选基因中,我们发现Sav1是Hippo通路的一个组成部分,Sav1和Hippo途径参与调节器官的大小。如果该途径被破坏,则肝细胞不受控制地复制,导致肿瘤的形成。在缺失Sav1基因的NAFLD小鼠中,肝脏受到严重损伤,Sav1的缺失导致肝脏肿大和肝脏肿瘤的发展,但这些新发现提供了Hippo途径失调与NAFLD中HCC发展之间的关键联系,对开发针对Hippo途径的新型肝癌治疗方案有积极意义。
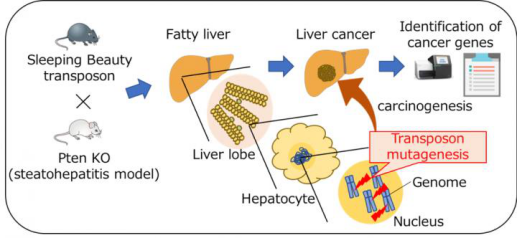
图片来源:大阪大学
5、基因组测序可指导肿瘤患儿的治疗
美国人类遗传学会(ASHG)2018年年会在加利福尼亚州圣地亚哥举行,会上公布了研究结果,对儿科癌症患者的肿瘤和非癌组织进行全面的基因检测是一种可行且对临床有益的方法,可以指导患者的治疗护理。
一个跨学科团队研究了253名儿科肿瘤患者。在79%的病例中,发现可以通过这个方法提供诊断依据,揭示患者特定风险或确定药物目标来帮助指导治疗。研究人员对患者的肿瘤以及同一患者的非癌组织进行全基因组测序(WGS),全外显子组测序(WES)和RNA测序。WGS涉及对患者完整基因组的测序,而WES涉及对转录成mRNA的部分进行测序,涵盖大部分编码的蛋白质。这项工作是儿童基因组研究(G4K)的一部分,这项研究旨在了解如何最好地利用基因数据进行儿科癌症的诊断和治疗。与其他研究不同,该研究除需要足够的肿瘤组织用于检测之外没有任何先决条件。
这是第一项为具有足够样本的新患者提供前瞻性综合测序的研究,所测试的癌症的多样性有助于验证基因变异与疾病之间的关系。研究人员开发了软件渠道和分析方法,他们发现了染色体内或染色体之间DNA的结构重排,因此使用全面的检测方法检测更具有挑战性。而且这种全面的测试不会使增加分析过程的负担,并且在大约40天内提供信息,具有临床价值。研究人员希望他们的研究结果能够为所有儿科癌症患者采用WGS。随着临床相关时间范围内的结果,以及定价与放射学和病理学测试的可比性越来越高,WGS对儿科肿瘤患者越来越容易被接受!现在G4K的信息汇编成可公开访问的在线数据库,研究人员鼓励全球协作并进一步分析其数据。他们继续对现有患者进行测序,且自最初的研究结束以来,已经成功地将这种方法用于大约300名患者。该团队计划继续研究测序方法,希望以更及时的方式生成临床适用的数据。
6、专家精确分析早期胰腺癌的新辅助疗法
根据医学博士Afsaneh Barzi的说法,胰腺癌最令人期待的一些数据来自佐剂吉西他滨和nab-紫杉醇(Abraxane)的联合研究。一项随机的III期APACT试验正在探讨切除胰腺癌患者使用nab-紫杉醇联合吉西他滨与单用吉西他滨的辅助治疗(NCT01964430)的相关问题。LAPACT试验研究了吉西他滨和nab-紫杉醇的治疗组合。据LAPACT试验所示,36%的患者对治疗有反应,其中约15%的患者实际接受手术治疗。其在诱导期间分别显示78%和33%的疾病控制率和客观反应率。治疗失败的中位时间为8.8个月,中位无进展生存期为10.8个月。
此外,Barzi认为,对胰腺癌患者及其家属进行基因检测极其重要,这可能是预防疾病的第一步。一些较小的FOLFIRINOX研究进行了荟萃分析显示,这些研究在当地晚期人群中进行。大约28%的患者能够进行手术。关键性试验ESPAC-4建立了吉西他滨和卡培他滨的组合,优于单独的吉西他滨。该研究共有730名患者,并且该组合的总生存期(OS)显示出18%的改善。这项研究有一些注意事项。它具有非常高的R1切除百分比 - 约60%的研究人群具有R1切除,其高于已发表的任何其他佐剂研究。他们研究了R1人群,当你单独观察吉西他滨与吉西他滨加卡培他滨时,生存率完全没有差异。这是我们应该记住的重要事项。
FOLFIRINOX与吉西他滨是另一项[新辅助]研究,科研人员在辅助治疗中对吉西他滨和FOLFIRINOX,与ESPAC-4相比,在无病生存率和OS方面表现出了更大的改善。因此,FOLFIRINOX是更好的选择。但大家都认为FOLFIRINOX毒性很大,有33%的患者因毒性而停止治疗,但通过充分的支持性护理来控制毒性对于维持患者的治疗是至关重要的。欧洲正在进行另一项正在进行的辅助研究,该研究正在研究吉西他滨和顺铂的组合。这些结果应该很快就会出来。对于患有转移性胰腺癌的人群,有时在他们的组织中检测分子标记物如BRCA1 / 2,我们将这些患者转诊进行基因检测,以确定该突变是基因组还是体细胞。
https://medicalxpress.com/news/2018-10-year-old-drug-therapy-cancer.html
https://medicalxpress.com/news/2018-10-method-blood-lung-cancer-treatment.html
https://medicalxpress.com/news/2018-10-breast-cancer-therapy.html
https://www.eurekalert.org/pub_releases/2018-10/ou-sbh101718.php
https://www.sciencedaily.com/releases/2018/10/181017211700.htm
https://www.onclive.com/conference-coverage/soss-gi-usc-2018/expert-discusses-emerging-treatments-in-early-pancreatic-cancer?p=2







































 首页
首页 咨询
咨询 方舟新药
方舟新药 营养商城
营养商城