10月19日,2018 ESMO(欧洲肿瘤内科学会年会)在德国慕尼黑隆重召开!肺癌,是发病率和死亡率极高的一种癌症,也是目前国际上研究以及进展较多的一种癌症。在今年ESMO大会上,肺癌的新研究有哪些?小编带您去看看!
1、厄洛替尼可改善早期突变非小细胞肺癌的无进展生存期
慕尼黑 ESMO 2018年大会上公布对于表皮生长因子受体(EGFR)突变且完全切除IIIA-N2期非小细胞肺癌(NSCLC),比较厄洛替尼与吉西他滨联合顺铂作为新辅助治疗的研究数据。
“CTONG 1103研究表明,在IIIA-N2期非小细胞肺癌中使用生物标志物指导的新辅助EGFR-酪氨酸激酶抑制剂(TKI)治疗策略是有希望的,这是第一项在IIIA-N2 EGFR突变NSCLC的新辅助治疗研究,证明厄洛替尼优于吉西他滨加顺铂化疗的无进展生存(PFS)优势。”中国广东省肺癌研究所终身教授吴一龙博士说。
研究共筛选出来自中国17个中心的386名患者,其中72名患者以1:1的比例随机分配至治疗组,并纳入意向治疗人群。新辅助治疗厄洛替尼与吉西他滨联合顺铂化疗的客观缓解率(ORR)为54.1% vs 34.3%。新辅助治疗后,厄洛替尼组83.8%的患者和吉西他滨联合顺铂组68.6%的患者接受了手术治疗。
厄洛替尼中位无进展生存期(PFS)显着延长,与吉西他滨加顺铂化疗相比,21.5个月vs 11.9个月,总体生存率还不成熟,吴博士说。目前可切除IIIA-N2 EGFR突变的NSCLC治疗策略是有争议的,但EGFR-TKIs已被证明可以改善晚期EGFR突变NSCLC患者的预后。
吴博士解释说,以顺铂为基础的双联化疗作为IIIA-N2 NSCLC的新辅助治疗,五年总生存率仅5%,该患者人群的医疗需求未得到满足。“最近,CTONG 1104试验(2)首次表明,与N1N2切除的NSCLC辅助化疗EGFR-TKI吉非替尼可以使无病生存期(DFS)提高10个月(28.7个月vs 18.0个月)。这提高了EGFR-TKI可能在该亚组的新辅助治疗中发挥有益作用的可能性。总的来说,这项重要的研究为我们提供了考虑新辅助EGFR TKI的基本原理。
2、肺癌一线化疗效果优于TKI——因罕见EGFR突变
靶向表皮生长因子受体(EGFR)的酪氨酸激酶抑制剂(TKI)是肺腺癌患者的标准治疗方法。然而,对大型EGFR测序结果数据库和相应临床试验分析显示,一线TKI治疗后对比化疗后出现的罕见EGFR突变与生存获益相关。该发现的第一作者法国病理科Aurelien Brindel在ESMO 2018次大会上报告了研究结果。
2009年至2017年,Brindel教授及其同事使用Sanger测序和二代测序等技术进行了7539次分子分析,涵盖了EGFR的外显子18、19、20、21。该分析包括EGFR突变体肿瘤,不包括L858R,外显子19缺失,T790M和外显子20插入。两位病理学家对所有突变进行了评估,并从患者的相应医疗记录中收集临床数据。
测序产生了857个EGFR体细胞突变,其中95个(11%)被认为是罕见的EGFR突变。47个(50%)罕见突变是外显子18突变,包括15%E709X和35%G719X改变。发现26(27%)个外显子20突变,包括9%的S768I和18%的A767_V769dup突变。此外,22(23%)个外显子21突变中的L861Q。更令人感兴趣的是27个(28%)产生其他突变,其中9个含有L858R突变。
相应的患者数据显示,接受一线化疗后出现罕见突变患者的中位总生存期(OS)长于接受一线TKI治疗出现相同突变的患者,中位数OS为27.7 vs 16.9个月(包括所有突变)。研究者进一步将OS与突变类型相关联,发现外显子18和外显子20与更好的预后相关,而L861Q与更差的预后相关。
3、肺癌EGFR突变新三代靶向药一线治疗初显成效
nazartinib纳扎替尼(EGF816)是第三代表皮生长因子受体(EGFR)酪氨酸激酶抑制剂(TKI),对未接受过治疗的EGFR突变的非小细胞肺癌(NSCLC)患者持续应答。 来自单药纳沙替尼的II期试验的主要疗效和安全性数据在德国慕尼黑的ESMO 2018大会上公布。
Nazartinib选择性靶向L858R和ex19del激活突变,以及T790M抗性突变体,同时保留野生型EGFR,新加坡国立癌症中心医学肿瘤学Daniel Lang Tan解释说。
纳扎替尼I / II期多中心研究(NCT02108964,EUDRACT编号2013-004482-14)在具有活化EGFR L858R和/或ex19del突变的晚期EGFR突变NSCLC的初治患者中进行。 所有45名患者连续接受推荐的II期口服剂量150 mg,每日一次。
中位年龄为64岁,试验中60%的患者为女性,62%为亚洲人。58%患者的ECOG表现状态为1,18名患者(45%)在基线时有脑转移。EGFR突变在56%的患者中有效,L858R在40%,4%的患者有其他EGFR突变。
29(29/45)例对纳扎替尼应答,ORR为64%,一名患者获得了完全反应。
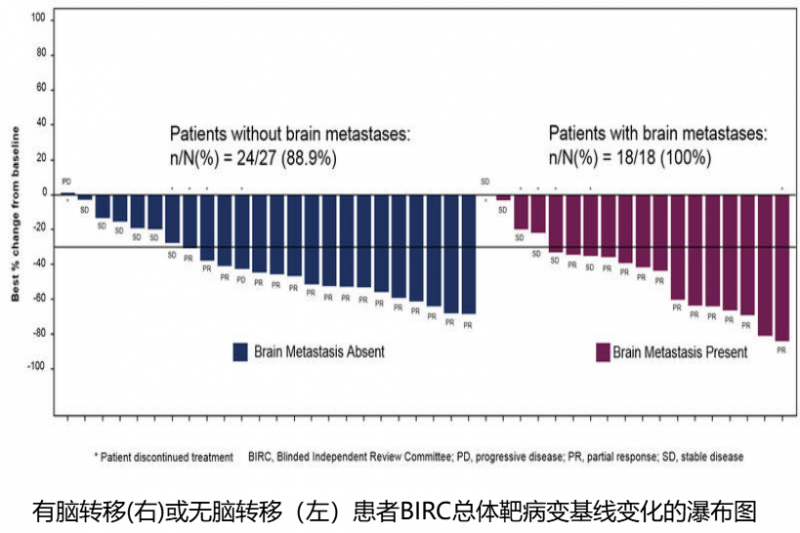
截至2018年3月22日的数据截止,29名中有27名继续应答,6个月的反应率(DoR)为91%,中位数DoR不可估计(NE),疾病控制率为93%。 纳扎替尼的6个月无进展生存率为83%,6个月总生存率为95%。 评估17例非靶病变基线脑转移患者,其中9例(53%)患者有脑转移消退。无基线脑转移的27名患者中,仅1名在研究中发生了新的脑转移。 45名患者对纳扎替尼中位持续时间为43.3周。
常见不良反应(AE)是包括腹泻(38%),斑丘疹(31%),口腔炎(24%),咳嗽(22%),食欲下降(22%),瘙痒(20%)和发热(20%)。 最常发生的3至4级AE(≥5%)是斑丘疹,9%的患者报告了这种情况。 由于病情进展,9名患者停药,1名患者因斑丘疹而停药,1名因患者选择而停药,1名患者因死亡而停药。
第三代EGFR-TKI具有良好的脑渗透性,PFS,DoR和OS尚未成熟,≥3级皮疹的发生率高于osimertinib。纳扎替尼初步研究显示出有希望的疗效,并为晚期EGFR突变NSCLC治疗初治患者提供了持久的反应,包括有基线脑转移的患者,但是仍需要大量数据证实是否优于osimertinib。
4、亚洲数据:艾乐替尼一线治疗ALK+肺癌完胜克唑替尼
脑渗透性强的ALK抑制剂-alectinib(艾乐替尼)一线治疗ALK+非小细胞肺癌(NSCLC)比克里唑替尼更有效,根据德国慕尼黑举行的ESMO 2018年大会上III ALESIA试验的结果。
中国上海市肺科医院肿瘤内科周彩存教授团队在亚洲患者中进行了alectinib 对比crizotinib的III期开放标签ALESIA(NCT02838420)试验。入组ALK阳性IIIB / IV期NSCLC患者,以2:1的比例随机分配,每日600 mg(n = 125)alectinib或每日250 mg(n = 62)克唑替尼,定期进行肿瘤和CNS成像观察。
根据RECIST v1.1,研究者的主要终点是无进展生存期(PFS),次要终点包括独立审查委员会(IRC)的PFS,CNS进展时间,客观缓解率(ORR),反应持续时间( DoR),总生存(OS),CNS ORR,生活质量(QoL)和安全性。
主要目的是证明亚洲患者的PFS与全球ALEX试验中报告的一致,ALEX研究数据:alectinib的中位PFS为34.8个月,而使用critzotinib为10.9个月,Alectinib对比克唑替尼显着降低病情进展风险。
本研究达到次要终点
crizotinib中位数PFS(IRC)为10.7个月,Alectinib未达到。在相应的治疗组中,评估ORR为91.2% vs 77.4%,中位DoR为未达到vs 9.3个月。虽然OS数据不成熟,但现有数据有利于alectinib。使用alectinib的不良事件为6.4%,而使用crizotinib则为21.0%。中位OS均为达到。
本研究证实Alectinib有CNS活性
对有脑转移的患者,使用alectinib的CNS ORR(IRC)为72.7%,而使用crizotinib为21.7%。在相应组中,完全应答率50.0% vs 13.0%。根据IRC审查,CNS进展的患者使用alectinib效果更佳。
尽管患者服用alectinib的时间较长,但3-5级不良事件(AEs)较少。使用alectinib和crizotinib治疗持续时间分别为14.7和12.6个月,3-5级AE发生率分别为29%和48%,严重AE发生率分别为15%和26%,7%的alectinib与10%的crizotinib患者因AE终止治疗。
研究人员得出结论,ALESIA研究的结果与全球ALEX研究一致。该研究证实了alectinib在亚洲晚期ALK阳性NSCLC患者一线治疗中的临床益处。
5、TMB在预测PD-1阿特朱单抗治疗的临床效用
大约30%的非小细胞肺癌(NSCLC)患者在进行基因检测时肿瘤组织不足,研究人员正在探索基于血液的肿瘤突变负荷(TMB)是否能成为一种生物标志物,评估其对患者使用检查点抑制剂治疗的预测价值。
在ESMO 2018年大会上,美国Kim教授介绍了前瞻性II期B-F1RST( NCT02848651)试验,评估了新型血液TMB检测作为atezolizumab(阿特朱单抗)的预测生物标志物的效用,该药物作为一线治疗PD-L1未选择的局部晚期或转移性NSCLC患者。
在B-F1RST中,152名意向治疗(ITT)人群,每3周接受1,200mg静脉注射阿特朱单抗,直至疾病进展或丧失临床益处。在该组中,119名患者被纳入生物标志物可评估人群(BEP)。根据预设的血液TMB临界值≥16(高TMB)或(低TMB)<16,评估Atezolizumab临床疗效。共同主要终点是客观反应率(ORR)和无进展生存期(PFS)。在ITT人群中,119名患者具有足够的循环肿瘤(ct)DNA,29名患者的ctDNA肿瘤脱落到血液中的比例不足。
至少6个月的随访时间,整体ITT人群的ORR为14.5%,BEP的ORR为10.1%。在具有良好预后特征的非BEP中,ORR为34.5%。高(≥16)与低(<16)血液TMB患者的atezolizumab反应的评估显示ORR为28.6% vs 4.4%。TMB低患者的中位PFS为3.7个月,而高血TMB患者为4.6个月。血液TMB高患者的中位总生存期(OS)无法估计(NE),而血液TMB低患者为13.1个月。
B-F1RST有重大发现,液体活检的作用可能是关键。但血液TMB可能无法捕获更敏感的肿瘤。
B-F1RST初步分析展示了第一个前瞻性数据集,该数据集评估了血液TMB作为晚期肺癌患者一线atezolizumab单药治疗的预测生物标志物的临床效用。作者得出结论,在预先指定的血液TMB≥16临界值时,患者显示出PFS,ORR和OS的数值益处,研究随访将持续到最终分析,根据协议,随访将持续≥18个月。
https://www.esmo.org/Press-Office/Press-Releases/CTONG1103-Lung-cancer-NSCLC-Zhong
https://www.esmo.org/Oncology-News/Uncommon-EGFR-mutations-lung-adenocarcinomas-Brindel
https://www.esmo.org/Oncology-News/Nazartinib-EGF816-treatment-naive-EGFR-mutant-NSCLC-Tan
https://www.esmo.org/Oncology-News/B-F1RST-blood-based-tumour-mutational-burden-atezolizumab-first-line-NSCLC-Kim







































 首页
首页 咨询
咨询 方舟新药
方舟新药 营养商城
营养商城