10月19日,2018 ESMO(欧洲肿瘤内科学会年会)在德国慕尼黑隆重召开!乳腺癌,是全球女性癌症第一杀手,也是目前国际上研究以及进展较多的一种癌症。在今年ESMO大会上,乳腺癌的进展有哪些?小编带您去看看!
1、每个人都能做到的抗癌策略——千万不要懒
运动或锻炼作为癌症护理的一部分可以显着改善症状管理,生活质量和治疗期间和之后的健康状况,法国研究人员在慕尼黑 ESMO 2018年大会上汇报了两个相关报告。即使在生活质量较差、风险最高的患者中,运动也会产生影响。
法国法兰西医学肿瘤学家Thierry Bouillet博士解释说,每年有超过3,500名癌症患者参加了法国80多个癌症中心的锻炼计划,费用约为每位患者400欧元,并且这一数字还在继续增加。如果患者在化疗或放疗六个月内每周至少运动一到三次,然后再进行六个月,那么锻炼会成为他们生活的一部分。
第一项报告:114名接受癌症治疗的患者接受每周两次,60分钟的力量训练和有氧运动课程,结果显著减少了3个月和6个月时的疼痛和疲劳评分,83%乳腺癌,21%转移癌。3个月时,疲劳评分由3.3降到2.8,疼痛评分从2.8降到2.3。6个月时, 71名患者中,疲劳评分由3.1降到2.1,疼痛评分从3降到1.9。此外,身体脂肪也显着减少,而体重保持稳定,就四头肌耐力,双臂强度和非显性腿部平衡而言总体适应性有显着改善。
第二项报告:在2525例接受辅助化疗的I-III期乳腺癌患者的研究中,每周进行75分钟剧烈运动或150分钟中度运动的患者在治疗后6个月和12个月的总体生活质量明显优于那些不运动患者(见下表)。
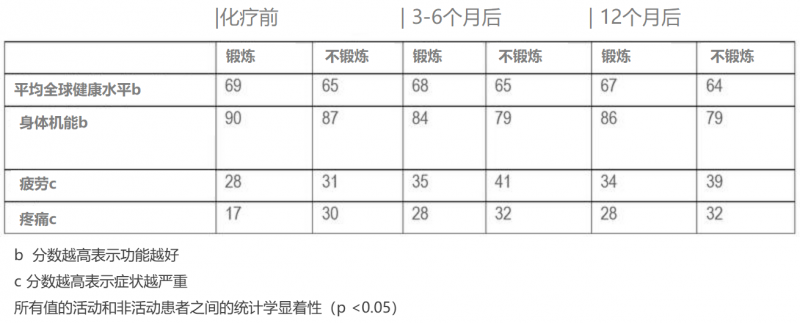
获益的患者身体状况更好:疲劳减少,疼痛减少和呼吸困难减少。剧烈运动包括有氧舞蹈、重型园艺或快速游泳等活动,而适度运动包括快走、水中有氧运动或排球。他们还有明显更好的身体健康,减少疲劳,疼痛和呼吸困难。剧烈运动包括有氧舞蹈,重型园艺或快速游泳等活动,而适度运动包括快走,水中有氧运动或排球。吸烟或收入低的乳腺癌患者在运动后,也能获益。身体活动计划可以改善对化疗和放疗的依从性,从而改善治疗结果,因此要鼓励癌症患者运动。
2、绝经前HR+早期乳腺癌激素+唑来膦酸联合DFS延长 但副作用严重增加
根据2018 ESMO的一项报告,HR+绝经前早期乳腺癌妇女,使用来曲唑加唑来膦酸加对比他莫昔芬的辅助疗法无病生存期(DFS)显著提高。这是第一项评估绝经前乳腺癌特异性组合的研究,并增加了先前对接受卵巢抑制的绝经前妇女中唑来膦酸加阿那曲唑的观察。
研究显示,绝经后妇女使用唑来膦酸加激素治疗HR +乳腺癌可降低复发率和乳腺癌死亡率,但绝经前妇女的益处以前不太清楚。唑来膦酸是一种双膦酸盐,可降低骨转换率,批准治疗骨质疏松症并减少癌症中骨转移损伤。与阻断雌二醇与雌激素受体结合的他莫昔芬不同,来曲唑是一种芳香酶抑制剂,能够极大地抑制雌二醇水平,但之前未在绝经前乳腺癌中进行过评估。
III期HOBOE-2试验包括1065名ER/PR阳性的早期乳腺癌患者,曾接受过曲普瑞林(每4周3.75mg)治疗5年,直至55岁,以抑制卵巢功能,近三分之二(63%)在随机分组前接受化疗。
患者随机接受他莫昔芬(20mg /天)或来曲唑(2.5mg /天)的激素治疗,或唑来膦酸(每6个月4mg静脉注射)联合来曲唑(2.5mg /天)(ZL)联合治疗五年。中位随访65个月后,该研究于2018年5月初停止。
在ESMO 2018报告的结果显示,接受ZL治疗的患者中有32例乳腺癌复发或二次乳腺癌或二次其他癌或死亡,使5年无病生存率(DFS)为93%。接受他莫昔芬治疗的患者有58例事件,来曲唑组有44例事件,5年DFS分别为0.85%和0.93%。
与他莫昔芬治疗相比,随机接受ZL治疗5年无病生存率显着提高,5年DFS的绝对优势为8%。接受ZL治疗的患者乳腺癌复发或非癌症死亡的风险几乎减半(风险比[HR] 0.52,95%置信区间0.34-0.80,p = 0.003)。比较来曲唑与他莫昔芬或将ZL与单独的来曲唑进行比较,DFS均没有统计学差异。
正如预期的那样,ZL治疗患者的副作用更多,9%的患者经历3-4级毒性,而接受他莫昔芬治疗的患者为4%,接受来曲唑治疗的患者为7%,与研究药物相关的最令人担忧的副作用中有4例ZL臂下颌骨坏死。
但是,专家指出两种治疗方法都会增加除他莫昔芬之外的毒性,所以最好只限于中高风险妇女,其风险收益可能是是可以接受的吗,对于早期乳腺癌还无法保证其获益。
3、帕博西林III期临床试验结果出炉:总生存期延长近7个月
根据ESMO 2018报道的PALOMA-3研究的总生存结果:HR+/HER2-晚期乳腺癌患者的细胞周期蛋白依赖性激酶(CDK)4/6抑制剂palbociclib(帕博西林)治疗实现临床意义上的总体生存率改善6.9个月,这些患者激素治疗耐药或者复发或进展。
III期PALOMA-3试验显示,521例HR+/HER2-晚期乳腺癌患者随机分配到palbociclib(口服125mg /天)加氟维司群(每次500mg)或安慰剂加氟维司群,中位随访44.8个月后,当521名患者中约60%(n≈310)死亡时,研究人员进行了OS分析。
结果显示, palbociclib加氟维司群组中位总生存期改善6.9个月(34.9个月vs 28.0个月)。对先前内分泌治疗敏感的患者的获益更大,中位OS的绝对改善为10.0个月。在没有内脏疾病的患者中,中位OS显着改善了11.5个月。随访时间越长,未发现新的安全问题。
“这对患者来说非常重要,因为它表明先前研究中观察到的PFS改善可能对总生存率产生积极影响,OS改善是治疗的最终目标,因此即使患有晚期疾病也能提高长期生命的机会,“Cristofanilli说。他补充说:“这项研究对OS积极影响的证明也为临床医生和患者提供了额外的信心,即这种组合可以作为晚期乳腺癌适当有效的治疗方法。”
评论ESMO的研究结果,意大利米兰欧洲肿瘤研究所的Carmen Criscitiello博士说:“这些数据非常值得期待,因为用CDK 4/6抑制剂获得的临床益处无可争辩,但是有一个热门的问题是PFS的好处转化为OS的好处。这项随机III期试验首次显示,在ER+/HER2-乳腺癌的转移性环境中使用CDK4 / 6抑制剂改善了OS。“
比利时布鲁塞尔Jules Bordet研究所的ESMO研究员Matteo Lambertini博士同意:“通过调查内分泌治疗和CDK 4/6抑制剂联合治疗的随机试验进行更长时间的随访,收集成熟的OS数据,现在得到了PALOMA-3更新结果的支持,这有力地表明这种治疗方法应该广泛用于患有晚期HR+/HER2-乳腺癌的女性。“他说:”进一步的研究需要更好地了解如何在这种情况下优化可用治疗方案的排序,以及识别可能仅受益于内分泌治疗的患者。“目前,关于早期乳腺癌两项研究-PENELOPE-B和PALLAS的palbociclib随机辅助试验正在进行中。

4、研究证实乳腺癌化疗后不易怀孕的假设不成立
众所周知,化疗对年轻乳腺癌患者的生殖功能有负面影响。然而,对女性治疗后生育能力的影响仍然知之甚少。ESMO 2018年大会上报道的一项研究证实,化疗后可能会发生自然妊娠,但幸存者在治疗后生育的愿望会大大减少,因此需要系统地采用生育保护措施。
生育保护措施一般基于体外受精和冷冻卵或胚胎,通常提供给40岁以下的乳腺癌患者。全球范围内,这一年龄组乳腺癌比例不到7%,但与一般人群相比,这些幸存者的怀孕几率低70%。据来自法国的研究者JérômeMartin-Babau博士说,“法国患者获得生育保护措施的主要障碍是它需要实验室设施和只有大医院才有的专业知识,患者不易获得。“
在研究过程中,确定了96名年龄在18-40岁之间化疗过的非转移乳腺癌的合格患者,其中60人同意参与调查。调查问卷基于文献中的现有工具,并添加了月经周期变化的问答。结果显示,83%的患者在化疗期间经历了闭经,86%的患者月经一年内恢复正常,这表明治疗没有完全损伤他们的卵巢。还评估了患者在疾病过程中生育孩子的愿望的演变:超过1/3的女性在开始治疗前曾计划怀孕。只有1/10的人化疗结束后仍然有这个愿望。仍然想要生孩子的6名患者中,4名女性实际上已经怀孕了,尽管其中有2名最终流产。因此,乳腺癌之后难以自然怀孕的假设不成立。
在评论ESMO的研究时,比利时布鲁塞尔Jules Bordet研究所的ESMO研究员Matteo Lambertini博士说:以前的数据已经表明,在乳腺癌诊断时,只有一小部分女性实际上选择接受生育保护措施。目前的研究结果虽然基于一个小的患者队列,但告诉我们,乳腺癌幸存者生育孩子的愿望在他们完成治疗时减少,同时确认化疗后仍然可以进行自然妊娠。然而,这并不意味着肿瘤学家不应该与患者讨论生育保护措施。作为医生,我们必须继续与我们的每一位乳腺癌患者讨论卵巢功能和生育能力的损失,就像我们对治疗的任何其他副作用一样:尽可能早地和广泛地进行,了解每位患者的具体情况非常重要。虽然这项研究提醒我们,不应过高估计对生育保存措施的需求,但我们也应该注意不要在向妇女提供这些选择时夸大这种程序的风险。“

5、研究表明HER2 +早期乳腺癌可选择短期曲妥珠单抗治疗
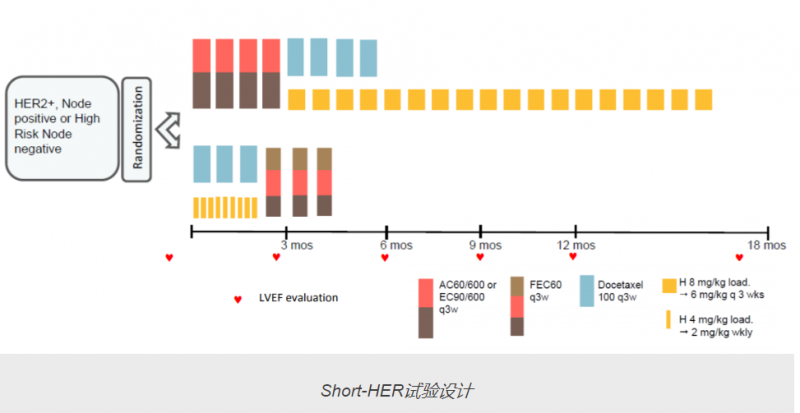
在2018 ESMO 2018年大会上报告的Short-HER试验一项亚组分析,患有HER2阳性早期肿瘤负荷小乳腺癌的女性曲妥珠单抗辅助治疗9个周对比一年治疗,有相似的无症状生存期和较低的心脏毒性风险。
目前的指南推荐一年的抗HER2抗体治疗作为HER2阳性早期乳腺癌患者的标准辅助治疗的一部分,人们感兴趣的是,较短疗程的曲妥珠单抗是否可能达到类似疗效,同时降低副作用和成本风险。
Short-HER试验将1254例HER2阳性早期乳腺癌患者随机分为9周或1年的曲妥珠单抗治疗组,两组均接受化疗。中位随访6年后,短期疗程非劣效性研究结果未达到,但严重重心脏毒性发生率降低。为了分析较短疗程的曲妥珠单抗治疗可能不逊于较长疗程的患者亚组,确定了三个预后组:
风险低(病理肿瘤大小[pT] <2cm和N0),占患者的37.5%;
中度风险(pT <2cm和任何N类),占51.9%;
高风险(pT> 2cm和N4 +),占患者人群的10.5%。
结果显示,低风险和中等风险患者的五年DFS相似:曲妥珠单抗疗程为9周(88%)对比一年(89%),但9周治疗组心脏事件的风险几乎降低了近三倍(4.5% vs 12.8%)。尽管得到如此数据,一年内曲妥珠单抗仍然是HER2阳性早期乳腺癌女性的标准治疗方法”。 研究者建议考虑使用较短时间的曲妥珠单抗也可以帮助那些无法负担更长疗程费用的患者。肿瘤负荷高的患者肯定会从较长时间的曲妥珠单抗中获益。肿瘤负荷低的患者也可以放心,他们没有失去疗效。
6、为期6个月的曲妥珠单抗治疗相比12个月可为每位患者节省近10,000英镑
2018 ESMO一项研究结果显示,与12个月相比,6个月的曲妥珠单抗辅助治疗具有成本效益,平均每位患者可节省近10,000英镑(89,448 RMB)。
研究人员分析了参加PERSEPHONE试验的HER2+早期乳腺癌患者标准12个月疗程与6个月辅助曲妥珠单抗的成本效益。这是最大的3期随机试验,并证明了降低曲妥珠单抗持续治疗时间的非劣效性。
这项新研究分析了4009名6个月无病患者的生活质量和健康服务活动和成本; 由于缺乏数据,250人被排除在外。结果显示,接受曲妥珠单抗治疗6个月的患者的平均费用为2,538.64英镑(22,700RMB),而治疗12个月患者每名患者的平均费用为12,333.83英镑(110,290RMB)。
治疗6个月可使每位患者平均节省9,793.25英镑(87,572RMB)。曲妥珠单抗的治疗和预后管理占这种成本节约的绝大部分,其余部分来自心脏评估和治疗费用以及住院天数。
6个月组和12个月组的个体平均质量调整生命年(QALYs)分别为1.146和1.128。平均QALY差异为0.018。因此,6个月的治疗组占主导地位,成本效益概率为100%。Harbeck评论说:“显示用6个月的曲妥珠单抗治疗比12个月治疗更经济,这是全球治疗的重要贡献。”但她补充说:“PERSEPHONE的亚组分析不能排除一年曲妥珠单抗的益处,因此一年仍然是标准持续时间。“
https://www.esmo.org/Press-Office/Press-Releases/HOBOE-breast-cancer-Triptorelin-Perrone
https://www.esmo.org/Press-Office/Press-Releases/trastuzumab-deescalation-breast-cancer-Shorther-persephone-Conte-Hulme







































 首页
首页 咨询
咨询 方舟新药
方舟新药 营养商城
营养商城