血癌、血液肿瘤、淋巴瘤、白血病CAR-T治疗,各种新型实体瘤CAR-T细胞免疫疗法全面升级
在人类与癌症抗争的历史长河中,嵌合抗原受体T细胞(CAR-T)细胞疗法绝对称得上是突破性疗法,占据了肿瘤免疫治疗的半壁江山,尤其是在血液肿瘤方面,FDA在2017年先后批准了全球仅有的两个CAR-T细胞疗法商业产品:诺华的Kymriah(淋巴瘤)与吉利德的Yescarta(白血病),可谓是彻底地改变了癌症治疗的格局。
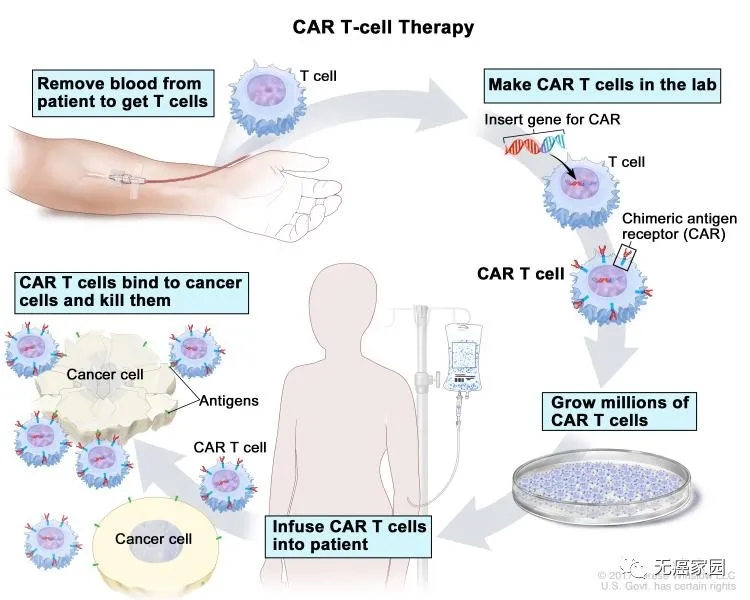
就在刚刚落幕的2020年美国癌症研究协会(AACR)会议上,CAR-T疗法风头正盛,在治疗血液肿瘤领域取得了突破性成果,那么接下来就让小编给大家介绍下会议上公布的研究成果。
缓解率近100%!通用型CAR-T疗法治疗T-ALL数据惊艳!
近日,中国亘喜生物科技集团在2020年AACR会议上公布了其通用型TruUCAR GC027治疗复发性或难治性(R/R)急性T淋巴细胞白血病(T-ALL)的一项I期临床试验的结果。
该临床试验是由研究者发起的首次人体试验,旨在评估通用型TruUCAR GC027治疗R/R T-ALL患者的安全性和有效性。截止到今年2月,该试验共入组5名R/R T-ALL受试者,受试者曾接受的既往治疗中位数为5次(范围为1~9 次)。
所有患者均接受了单次TruUCAR GC027的输注,输注计量为高中低三组计量组中的一种:0.6*10^7 细胞/公斤、1.0*10^7 细胞/公斤,或1.5*10^7 细胞/公斤。值得注意的是,5名受试者均未进行人类白细胞组织相容性抗原(HLA)配型,输注后均未接受造血干细胞移植(HSCT)。
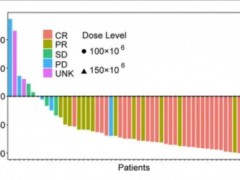
通过28天随访,5名受试者的评估结果:
(1)5名(100%)受试者获得完全缓解,其中包括血细胞数量完全或未完全恢复(CR/CRi);
(2)4名(80%)受试者获得最小残留疾病阴性的完全缓解(MRD-CR)。
(3)所有5名受试者均能够耐受TruUCAR GC027单次输注,试验中未观察到神经毒性事件或急性移植物抗宿主病(aGvHD)发生,同时观察到所有5名受试者均出现不同程度的细胞因子释放综合征(CRS),均在可控范围内。
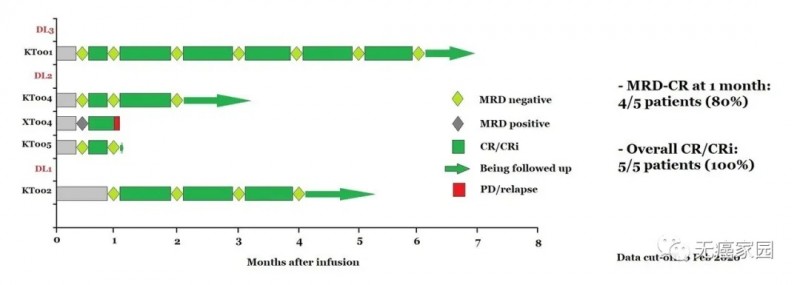
5名受试者随访后的临床疗效
全球肿瘤医生网王立宏博士说道,T-ALL是一种急性淋巴细胞白血病(ALL),在儿童ALL中的比例占到12%~15%,而在成人ALL中的占比高达20%~25%,属于难治性疾病,治疗手段极为有限,而且大多数T-ALL患者在多种药物联合化疗后的2年内容易复发。
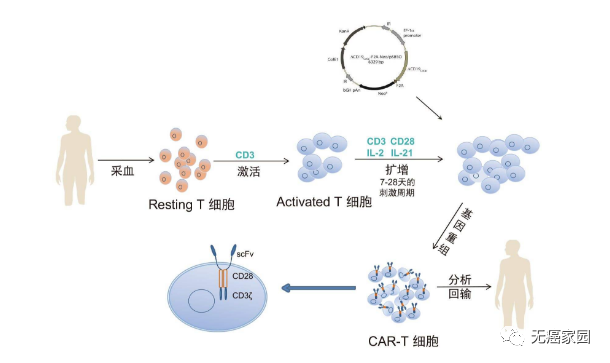
GC027使用了亘喜独有的TruUCAR专利技术,利用无需进行HLA匹配的健康供者T细胞,是一种在研的即用型CAR-T细胞疗法,能够靶向CD7抗原表达的肿瘤细胞,用于治疗T细胞恶性肿瘤。
此外,TruUCAR技术使得同种异体CAR-T细胞可在HLA不匹配的患者(受者)体内增殖并持续存在,同时控制移植物抗宿主病(GvHD)的风险。更重要的是,TruUCAR属于即用型,患者不仅能够及时得到救治,而且其低廉的制造成本使重复给药成为可能!
抗癌无进展生存率达72%,新型CAR-T技术打破实体瘤壁垒
除了上述的血液肿瘤外,医学研究者们在实体瘤方面也可谓是鞠躬尽瘁。在2019年的美国癌症研究学会(AACR)年会上,一款靶向间皮素的新型CAR-T细胞技术,吸引了众人的目光,其疗效数据可谓是让人眼前一亮。这项名为LcasM28z的CAR-T细胞疗法倾注了纪念斯隆凯特琳癌症中心胸外科副主任Prasad Adusumilli研究团队的心血。
【研究背景】
这项临床试验共纳入21例既往经其他治疗均失败的复发难治的间皮素表达阳性的晚期实体瘤患者,其中包括晚期恶性间皮瘤19例,晚期肺癌1例,晚期乳腺癌1例。所有患者均接受LcasM28z联合PD-1抗体治疗。LcasM28z是由Adusumilli及其团队利用第二代激活CD28全人类间皮素CAR T细胞加以Icaspase-9安全基因所研制而来。而且绝大多数患者在CAR-T治疗前接受过大剂量化疗清髓预处理。需要注意的是,此操作必须在非常有经验的大医院进行,需要高度预防感染。
【研究成果】
接受治疗38周后,21例患者中有13例的外周血中依然可以检测到持续存在的CAR-T细胞。有11例患者顺利完成CAR-T注射及至少3个疗程的PD-1治疗。经过至少3个月的随访,11例患者中,有8例患者肿瘤明显缩小,甚至包括2例患者PET-CT提示肿瘤完全消失,总体缓解率高达72%。
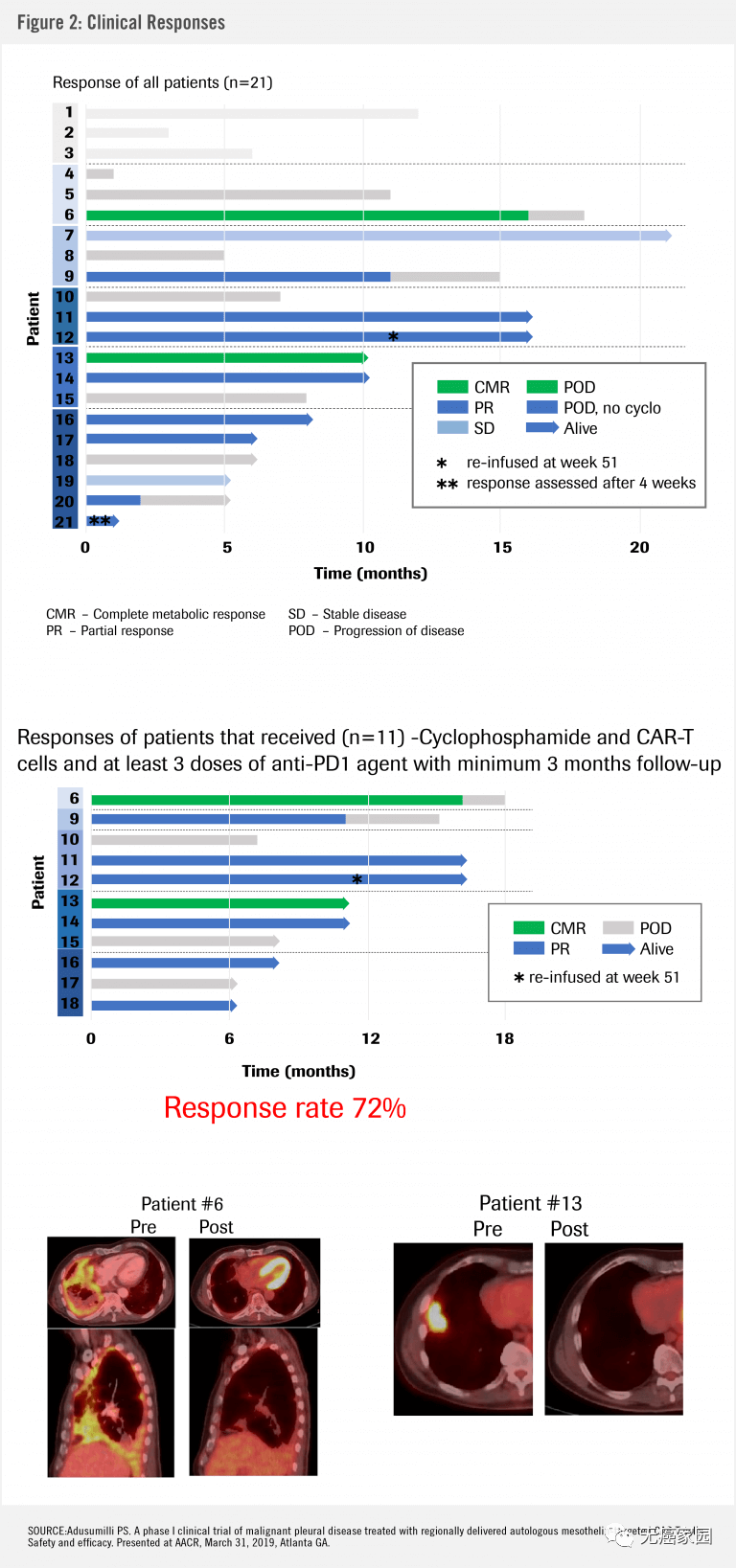
【安全性】
此项技术的副作用轻微,仅有1例患者在预处理阶段发生了严重的中性粒细胞减少,经过对症治疗后好转。在CAR-T联合PD-1抗体治疗阶段,无一例严重的神经毒性、细胞因子释放综合征及其他重要器官的损伤等发生。
晚期肉瘤不用怕!靶向HER2的CAR T疗法初试锋芒!
2019年AACR会上报道了另一靶向HER2的CAR-T疗法。美国贝勒医学院Hegde报告的一项小型I期研究显示,在罹患晚期HER2阳性肉瘤的儿童和成人患者中,靶向HER2的CAR T细胞治疗联合淋巴细胞耗竭性化疗安全且有临床活性。
软组织和内脏肉瘤是一组罕见的间充质肿瘤,有70多种亚型;这些不同肿瘤的治疗极具挑战性,且晚期患者的预后通常较差。
该研究入组10例难治性或转移性HER2阳性肉瘤患者,其中5例骨肉瘤,3例横纹肌肉瘤,1例尤文肉瘤,1例滑膜肉瘤。既往治疗方案多达5线。经氟达拉滨单药或联合环磷酰胺清除淋巴细胞后,最多输注3次靶向HER2的CAR T细胞。初始应答者另接受5次CAR T细胞治疗。
结果显示,除2例患者外,CAR T细胞在其余患者中均扩增,第7天达到中位峰值,输注6周后所有患者中均可检出CAR T细胞。
1例骨髓转移的横纹肌肉瘤患儿获得12个月的完全缓解,复发后再次接受CAR T细胞治疗,获得了持续17个月的完全患者。1例肺转移的骨肉瘤患儿获得了持续32个月的完全缓解。3例疾病稳定,5例疾病进展。
总体而言,治疗相关毒性有限。输注CAR T细胞后24小时内,8例发生了1~2级的细胞因子释放综合征,并于支持治疗5天内完全恢复。未见心功能降低或肺毒性事件。
此实验表明,以HER2为靶点的CAR T细胞疗法与淋巴结清扫疗法相结合是安全的,尽管是早期试验,但它显示出对晚期HER2阳性肉瘤患者具有良好的抗肿瘤活性。
小编有话说
近年来,医学研究者们已经做出了相当大的努力开发新的攻克实体瘤的新技术,竭尽全力地采取优化策略针对不同特定适应症的CAR-T疗法。小编相信在不久的将来,越来越多的临床前/临床试验数据能够不断涌现,充分展示CAR-T细胞疗法治疗实体瘤的真正实力。
参考文献
1.https://www.aacr.org/professionals/blog/aacr-annual-meeting-2019-promising-data-from-car-t-cell-clinical-trials-for-advanced-solid-tumors/
2.https://www.fiercebiotech.com/biotech/aacr-after-blood-cancer-successes-car-t-treatments-see-inroads-for-solid-cancers
3.https://www.evaluate.com/vantage/articles/events/conferences/aacr-2020-gracell-validates-novel-car-t-target
4.https://www.onclive.com/conference-coverage/aacr-2020/universal-allogeneic-car-tcell-product-demonstrates-efficacy-in-a-cohort-of-adult-tall
5.https://www.cancertherapyadvisor.com/home/cancer-topics/hematologic-cancers/acute-lymphoblastic-leukemia-first-human-universal-cart-therapy-active/