非小细胞肺癌靶向药新药,非小细胞肺癌EGFR外显子20插入突变基因突变靶向药新药及临床试验汇总
提到肺癌靶向药,很多人首先想到的一定是EGFR-TKI药物。众所周知,在肺癌靶向药中EGFR-TKI药物的研究最广泛,EGFR-TKI药物中治疗肺癌的适应症也最充足。但在EGFR突变中有一种亚型,被称为EGFR外显子20插入突变(EGFR ex20in),对于各类EGFR-TKI药物均不敏感,治疗难度很大,靶向药物的使用仍然存在不小的尴尬。
目前,国外针对EGFR ex20in突变型有部分在研药物或正在进行的试验,但尚无获批药物及治疗方案。对于国内患者来说,已有药物疗效欠佳、外国在研药物又难以获得,生存质量并不理想。
但幸运的是,我国药厂自主研发的新药JMT-101靶向EGFR ex20in突变型,临床试验已经如火如荼地展开。在目前国际上EGFR ex20in治疗领域获批药物仍处空白的情况下,国研药物JMT-101的登场可谓是一个重磅消息,为这部分患者带来了福音。
热门突变中的稀有类型——了解EGFR ex20in
名称:EGFR ex20in
全称:EGFR 20号外显子插入突变
位置:7号染色体短臂
突变类型:插入突变
特点:
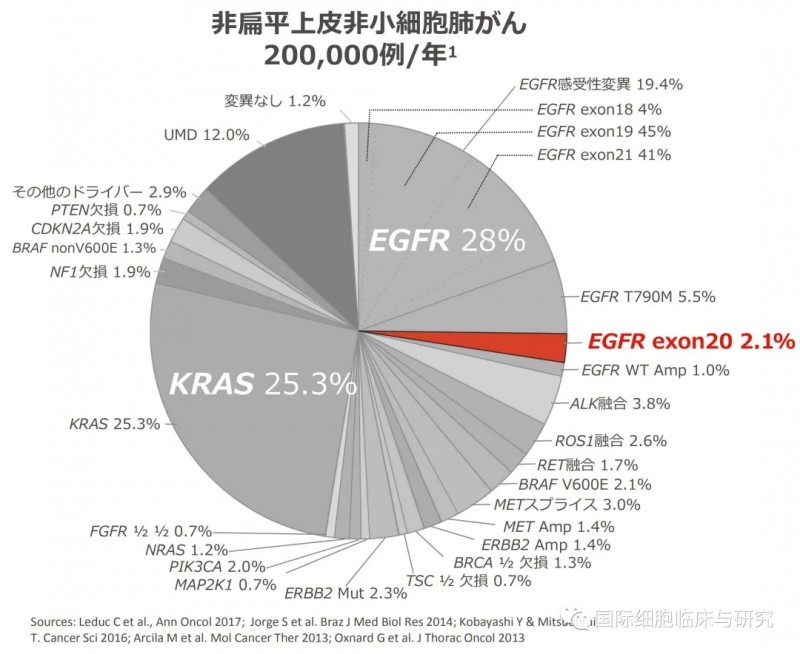
1、属于EGFR罕见突变中最常见的类型,占罕见突变的30%,占所有突变的4.8%~12%;整体来说,EGFR ex20in占非小细胞肺癌的2%~3%;
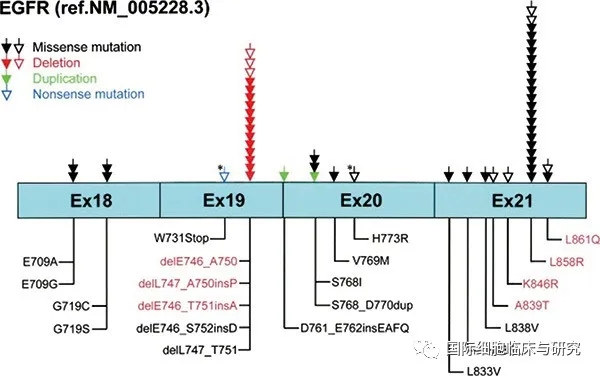
2、EGFR ex20in包括多种类型,发生率有一定差异;

3、一、二代EGFR-TKI药物治疗EGFR ex20in疗效并不理想,总无进展生存率仅0~11%;三代EGFR-TKI药物治疗中位无进展生存期约6.2个月。
EGFR ex20in突变型非小细胞肺癌治疗方案研究进展
与常见的EGFR突变型不同,EGFR-TKI药物治疗EGFR ex20in患者效果并不理想,已有多项国内外研究数据证实。但临床上已有多款新药正在研发或进行试验,疗效值得期待。
国内治疗现状:疗效欠佳,仍需突破性新药
一项国内研究分析了EGFR 20号外显子插入突变型非小细胞肺癌患者的治疗模式和结局,结果显示,2018年3月17日至2018年12月20日,中国26个不同地区99家医院治疗的165例携带EGFR ex20in的晚期非小细胞肺癌患者数据接受了分析。共鉴定出39种不同的EGFR ex20in分子变异类型,其中V769_D770insASV最常见,约占23.0%。
在基线诊断时,脑转移发生率为23.0%。一线含铂化疗患者的中位PFS为6.4个月,显著长于各代EGFR-TKI的2.9个月,其中包括第一代EGFR-TKI的2.0个月。
二线化疗者的中位PFS为4.0个月,明显长于二线EGFR-TKI治疗者的2.0个月。一线化疗后,脑转移患者的中位PFS为3.6个月,明显短于无脑转移的患者的6.5个月,及一线EGFR-TKI治疗患者的2.0个月。
整体来说,国内EGFR ex20in突变型非小细胞肺癌患者的治疗情况并不理想。
一、二代EGFR-TKI:疗效显著低于典型EGFR突变型
采用一、二代EGFR-TKI药物治疗,EGFR ex20in突变型患者的疗效明显低于其他EGFR突变型患者。
根据日本机构统计的结果,采用现有的EGFR-TKI药物进行治疗,典型EGFR突变型患者的中位无进展生存期可以达到12.0个月时,EGFR ex20in突变型患者的中位无进展生存期仅2.0个月。
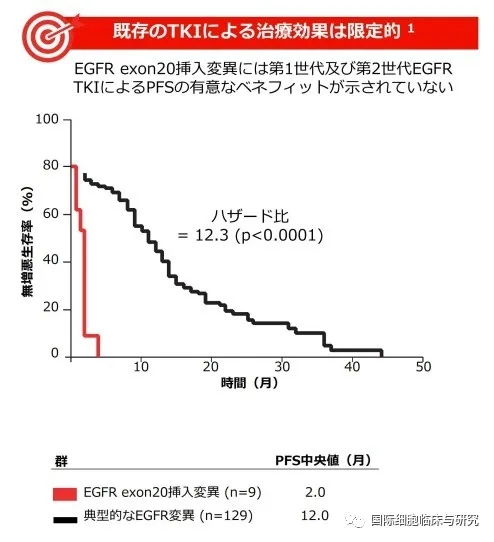
第三代EGFR-TKI奥希替尼:无进展生存期6.2个月,具备治疗潜力
在一项纳入6例患者的小型研究中,接受奥希替尼治疗的EGFR ex20in患者中位无进展生存期为6.2个月,最长者无进展生存期14.6个月;最常见的不良事件为腹泻、瘙痒、口腔炎和恶心,未发生3级或以上不良事件。
这一结果说明,采用奥希替尼治疗部分EGFR ex20in患者存在一定的可能性,但患者数量较少,仍需更多研究数据支持。
第二代EGFR-TKI阿法替尼:联合西妥昔单抗治疗具有一定的临床潜力
在小鼠研究中的结果显示,采用阿法替尼联合西妥昔单抗,对于小鼠模型的疗效比单独应用阿法替尼或西妥昔单抗的效果更好。
这一结果提示,当单一用药疗效不佳时,可能考虑联合用药方案进行治疗,但仍需更多临床研究来支持这一结果。
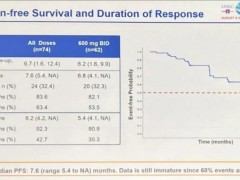
新药TAK-788:客观缓解率43%,无进展生存期7.3个月
Mobocertinib(TAK-788,曾用代号AP32788)由日本武田制药研发,目前已获得FDA的突破性疗法指定。
Mobocertinib基于奥希替尼的骨架核心改进,提高了对EGFR ex20in的治疗活性,28例可供评估的EGFR ex20in非小细胞肺癌患者,客观缓解率(ORR)为43%,中位无进展生存期为7.3个月。
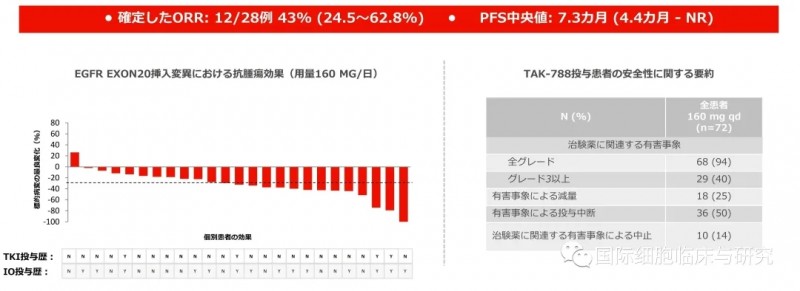
在不良反应方面,常见不良反应包括腹泻、恶心、皮疹、呕吐、食欲下降等,多为1~2级;3级以上不良反应发生率19%,多为腹泻。
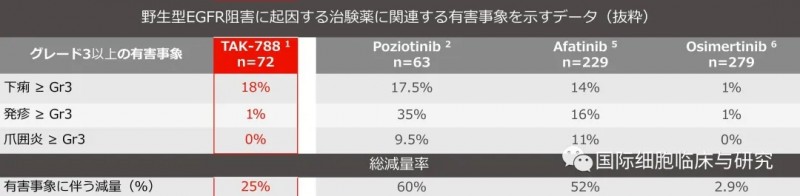
目前,针对这一药物的临床试验正在多个国家开展,查阅clinicaltrials网站可以得知,其中日本地区的试验项目正在招收患者。

新药JNJ-6372:缓解率28%,突破奥希替尼耐药瓶颈
JNJ-6372是一种具有免疫细胞定向活性的EGFR-MET双特异性抗体,靶向活化和耐药的EGFR和MET突变和扩增。目前,JNJ-6372已经于2020年3月10日获得了FDA的突破性疗法指定。
在该指定依据的Ⅰ期试验中,JNJ-6372治疗复发性EGFR突变和EGFR ex20in的患者,部分缓解率达到28%;在三代EGFR-TKI耐药的患者中,仍然获得了21%的缓解率。针对EGFR ex20in患者,缓解率达到30%。
尽管国际研究快速进展,但对于国内患者来说,这些药物及临床试验还是显得“触手难及”。再兼如今国际局势所致,出国就医困难重重,患者亟待国内研究者推出有效方案,改善治疗效果。
开云见霁,我国创新药物JMT-101投入试验
2019年年底,我国自主研发的、专门治疗EGFR ex20in突变型患者的人源化EGFR单克隆抗体创新药物JMT-101获得批准投入临床试验。从大肠癌开始,以包括非小细胞肺癌在内的多种实体瘤为目标,向癌症发起挑战。
与TAK-788和JNJ-6372相比,JMT-101为我国自主研发药物,是我国靶向药物研发实力的体现,同时更易于国内患者获取、价格更便宜。目前,JMT-101治疗非小细胞肺癌的Ⅰ期临床试验已经在招募患者,非小细胞肺癌患者可以免费接受新药治疗了!
免费用药机会来了!JMT-101治疗非小细胞肺癌临床招募进行中
近期,JMT-101治疗多种实体瘤的Ⅰ期临床试验已经陆续开始。其中,治疗非小细胞肺癌的Ⅰb期试验正在招募患者。
试验名称:评价JMT101联合阿法替尼或奥希替尼治疗EGFR 20号外显子插入突变的ⅢB 或Ⅳ期非小细胞肺癌患者的安全性和有效性的Ⅰb期临床研究
试验分期:Ⅰb期
主要纳入标准:
1、年龄18~75(含)周岁,性别不限;
2、ⅢB或Ⅳ期非小细胞肺癌,不适合进行根治性手术或放疗,且证实具有EGFR 20号外显子插入突变(包括重复突变),初治或一线治疗失败后的患者;
3、基线至少存在一个符合RECIST 1.1标准定义的可测量的病灶;
4、ECOG体能状态评分:0或1分;
5、预计生存时间≥3个月等。
主要排除标准:
1、既往接受过EGFR单克隆抗体靶向治疗;
2、具有临床症状的中枢神经系统转移或脑膜转移;
3、在首次使用研究药物前4周内接受过其他治疗方案等。
申请流程:
1、按要求将病历资料提交至全球肿瘤医生网医学部;
2、医学部初步评估后匹配合适的临床试验;
3、向相应的试验中心提交病历资料;
4、评估通过后协助患者参加临床试验。
↓扫描二维码申请入组↓
![]()
写给患者的话
的确,长期以来,EGFR 20号外显子插入突变型患者的治疗效果并不理想,与其他EGFR突变型患者相比存在不小的差距。但各位病友并不应该为此而感到绝望、更不能提早放弃。我们可以看到,随着医疗水平的发展,研究者已经将目光放到了这些“罕见突变”上,新药涌现,光明的前景正在徐徐展开。
如今,我国医疗水平逐渐跟上了世界的脚步,自主研发的新药频频问世,国内患者获得先进药物治疗的希望终于不再遥不可及。我们衷心地希望,JMT-101能够帮助更多国内患者战胜肿瘤、收获幸福生活。
参考文献
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC6754574/#b42
https://meetinglibrary.asco.org/record/188532/abstract