乳腺癌新疗法,盘点2020年展望2021年,乳腺癌有哪些不容错过的重磅新药
2020年是不平凡的一年,而癌症领域同样取得了不平凡的突破。在乳腺癌领域,同样有多款新药与新疗法上市,为患者的生存“续航”。
值此2020与2021相接之际,全球肿瘤医生网-基因药物汇为大家盘点了过去一年中获批上市的乳腺癌新药物与新疗法,以及2021年可能获批的重磅新药预告,让病友们带着更多的希望与期待跨入新的一年。
乳腺癌新药新疗法
乳腺癌是一种与性别有较大关联的癌种,约99%的乳腺癌患者是女性,男性仅占1%。仅以患者数量而言,乳腺癌不亚于肺癌。由于HER2靶向药物曲妥珠单抗的问世,与肺癌相比,乳腺癌的5年生存率整体较高,许多早期患者的病情可以通过手术得到有效的控制。但三阴性乳腺癌患者、尤其是晚期患者的生存情况仍然不理想,5年生存率亟待提升。
乳腺癌同样是一类比较容易发生转移的癌种。许多患者病情进展到晚期,或发生转移,5年生存率急剧下降,仍然需要更多有效的药物来改善生存情况。
01、生存期再次延长!来那替尼联合用药方案带来全新突破
HER2阳性乳腺癌在所有乳腺癌中约占15%~20%,自以曲妥珠单抗为代表的各类HER2抑制剂问世以来,HER2阳性乳腺癌患者的生存期得到了跨越式的延长。但曲妥珠单抗及其它HER2抑制剂耐药后的治疗方案仍是一个临床难题。
2020年2月27日,FDA批准了来那替尼(Neratinib)+卡培他滨(Capecitabine)联合用药方案,用于治疗已接受2线或以上抗HER2疗法治疗的晚期或转移性HER2阳性乳腺癌成年患者。
该批准主要基于Ⅲ期NALA试验的结果,该结果表明,来那替尼+卡培他滨联合用药组的中位总生存期为21个月,1年无病生存率为29%,2年无病生存率为12%;而常规拉帕替尼(Lapatinib)+卡培他滨联合用药组的中位总生存期为18.7个月,1年无病生存率为15%,2年无病生存率仅为3%。
02、图卡替尼提前四个月获批,晚期乳腺癌患者迎来重磅新药
同样用于治疗晚期HER2阳性乳腺癌,包含图卡替尼(Tucatinib)的联合用药方案在预计批准期前4个月提前获批。
2020年4月18日,FDA批准图卡替尼+曲妥珠单抗+卡培他滨联合用药方案,曾接受过≥1次抗HER2治疗方案的不可切除的局部晚期或转移性HER2阳性乳腺癌患者,包括脑转移患者。
该批准基于Ⅱ期HER2CLIMB试验的数据,结果显示,三联治疗组患者中位总生存期为21.9个月,1年生存率76%,2年生存率62%;曲妥珠单抗+卡培他滨治疗组患者中位总生存期为17.4个月,1年生存率45%,2年生存率27%。在发生了脑转移的患者中,三联疗法也使患者的死亡风险降低了52%。
三阴性乳腺癌新药新疗法
三阴性乳腺癌指雌激素受体(ESr或Er)、孕酮受体(Pr)及HER2表达均为阴性的乳腺癌类型,在全部乳腺癌中占比约15%左右。部分研究认为,三阴性乳腺癌的发生与BRCA1突变相关。
由于无法接受内分泌治疗及HER2靶向药治疗,三阴性乳腺癌患者的治疗难度普遍高于其它类型的乳腺癌患者。
01、三阴性乳腺癌也有靶向药了!首款靶向TROP-2的ADC药物来袭
2020年4月23日,FDA批准Sacituzumab Govitecan-hziy用于治疗转移性三阴性乳腺癌的成年患者,患者既往应接受过≥2种方案治疗。
该批准基于TNBC的sacituzumab govitecan Ⅰ/Ⅱ期研究的结果,中位随访9.7个月时,患者客观缓解率为33.3%,中位缓解持续时间为7.7个月,临床获益率(客观缓解+疾病稳定率)为45.4%;通过独立审查委员会评估,客观缓解率为34.3%,中位缓解持续时间为9.1个月。
02、免疫疗法也有新进展,派姆单抗获批三阴性乳腺癌适应症
由于靶向治疗难度较大,免疫治疗成为了晚期及转移性三阴性乳腺癌治疗的一个重要方向。2020年11月14日,FDA批准派姆单抗用于治疗局部复发、不可切除或转移性的三阴性乳腺癌患者,患者PD-L1表达阳性(CSP≥10)。
该批准基于KEYNOTE-355试验(NCT02819518)。接受派姆单抗+化疗治疗的患者,中位无进展生存期9.7个月;而接受安慰剂+化疗治疗的患者,中位无进展生存期5.6个月。
根据2020年ASCO大会上公开的结果,在CSP≥10的患者中,接受派姆单抗+化疗治疗的患者,1年无进展生存率为39.1%;接受安慰剂+化疗治疗的患者,1年无进展生存率为23.0%。
2021展望:化疗也有新进展,口服紫杉醇有望替代静脉输注紫杉醇
目前为止,化疗药物紫杉醇的用药方式均为静脉输注给药。但一项针对口服紫杉醇的研究获得成功,使口服紫杉醇治疗成为了一种潜在的选择。
共402例转移性乳腺癌患者参加了试验,其中,接受口服紫杉醇+Encequidar(一种P-gp抑制剂)治疗的患者,整体缓解率为36%,静脉输注紫杉醇治疗的患者整体缓解率为24%。同时,接受口服组合药物治疗的患者,缓解持续超过150天的比例是静脉输注治疗的患者的2.5倍。
口服的用药方案可以有效降低患者接受治疗的难度,使一些难以频繁前往医院的患者同样能够得到规律的治疗。同时,口服用药的联合方案也展现出了更好的疗效。
2020年9月1日,FDA已经为口服紫杉醇+Encequidar方案授予优先审查资格,预计将于2021年2月28日前公布审核结果。
方舟计划,2021再启航
靶向和免疫治疗已经显着改善了非小细胞肺癌患者预后,尤其在EGFR和ALK两类突变型患者的治疗中成果显著。除此以外,在肺癌新药的研发过程中,更多的黄金靶点及众多值得期待的重磅新药涌现,比如针对EGFR 20ins突变型的JMT-101,针对ROS-1突变型的TQ-B3101等,为患者抗癌增添了有益的助力。
“方舟援助计划”由全球肿瘤医生网联合无癌家园、权威基因检测机构、国际药厂、知名肿瘤中心发起的针对癌症基因突变肿瘤患者的活动。本计划旨在降低肿瘤患者基因检测费用,为患者提供上市新药和未上市新药免费治疗的机会。
“方舟援助计划”将为所有参与的癌症患者持续提供抗癌药物,带来新的生存希望!
申请方式
将基因检测报告、诊断报告的电子版或清晰照片发送至邮箱doctorjona0404@gmail.com,邮件中留下联系方式;或者联系全球肿瘤医生网医学部(400-666-7998)进行详细咨询。
"方舟计划一"-基因检测支持
全基因检测的市场价格普遍在15000~20000元之间,属自费项目,对于很多家庭来说仍是一笔不小的费用。方舟援助计划将为符合条件的患者提供经济援助,帮助病友减轻经济负担。
方案一:经过指定基因检测机构付费检测,发现指定基因突变的患者,并成功入组相关新药临床研究的患者,可获得5000元基因检测经济援助。
方案二:经过指定基因检测机构付费检测,未发现指定突变的患者,可获得1000元基因检测经济援助。
方舟援助计划覆盖的基因突变
实体肿瘤存在以下基因突变:EGFR、KRAS、ERBB2、BRAF、PIK3CA、AKT1的驱动突变以及ALK、ROS1、RET、NRG1、NTRK1/2/3、FGFR1/2/3/4、MET、EGFR、BRAF、ETV6基因的融合与跳切等。
*随新药研制进度,基因突变种类和范围会不断扩大,并不限于上述突变其他靶点可联系医学部进行解读及有无援助政策。
参加方舟援助计划流程
1、按要求提交病理组织切片或者基因检测报告;
2、全球肿瘤医生网医学部分析基因检测报告,或送基因检测机构进行检测;
3、如有符合新药适应症的基因突变,全球肿瘤医生网医学部协助患者对接国际药厂和医院研究中心专家;
4、患者成功加入新药治疗研究后,给予相应基因检测经济援助;
5、未发现突变靶点或发现靶点但未能入组相关临床试验,给予相应基因检测经济援助。
"方舟计划二"-抗癌新药免费
通过“方舟援助计划”检测出有意义基因突变或基因检测报告显示相关突变,将优先为患者参加国内及国际抗癌新药临床试验项目筛选。这些新药临床项目均在国内北上广等权威三甲医院开展,患者可以与国内知名专家对接,接受与国际同步开展的国际多中心新药临床研究。
"方舟计划三"-3D类器官筛选
通过“方舟援助计划”检测出有意义基因突变或基因检测报告显示相关突变,将优先为患者参加国内及国际抗癌新药临床试验项目筛选。这些新药临床项目均在国内北上广等权威三甲医院开展,患者可以与国内知名专家对接,接受与国际同步开展的国际多中心新药临床研究。
所有的抗癌药物都会出现耐药问题,这也是很多患者最担心的问题。“方舟计划”专门针对患者参加临床试验后耐药问题,推出类器官培养和筛选援助,对入组临床试验出现耐药的患者免费进行类器官培养,寻找下一步用药方案。
"什么是类器官培养"
类器官是近年国际上突破发展的一种体外3D组织培养技术,可以在体外高成功率、快速的培养人的组织细胞,形成保留原器官组织结构和生物信息的“微组织”,在个性化治疗和再生医学领域有广泛的应用前景。肿瘤类器官培养技术,通过在体外建立类似体内的微环境,把患者组织分离的肿瘤细胞在体外实现3D培养,形成微型肿瘤模型。利用该模型帮助肿瘤患者个性化的测试多种药物的敏感性,实现个性化的精准医疗。
"哪些患者可申请类器官培养"
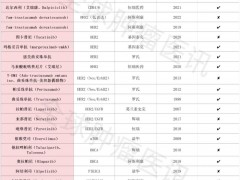
成功入组以下表格中的临床试验,耐药后出组的患者可免费接受类器官培养,帮助患者寻找下一步用药方案。

注:肿瘤类器官培养需要获得患者活体肿瘤细胞培养,需要通过穿刺或者手术获取肿瘤细胞。不是所有的患者都能取得活体肿瘤细胞!
肿瘤类器官培养由科途生物公司为符合条件的患者提供,本计划不保证所有患者都能获得免费类器官培养,并不能保证所有患者培养成功。