新码生物重组人源化抗HER2单抗-AS269偶联物(ARX788)HER2阳性乳腺癌临床试验II/III期招募整在进行中
根据国家药监局最新公示,浙江医药旗下子公司新码生物研发的注射用重组人源化抗HER2单抗-AS269偶联物(ARX788)已于5月25日结束公示,正式纳入突破性治疗品种目录,拟定适应症为HER2阳性晚期乳腺癌二线治疗。
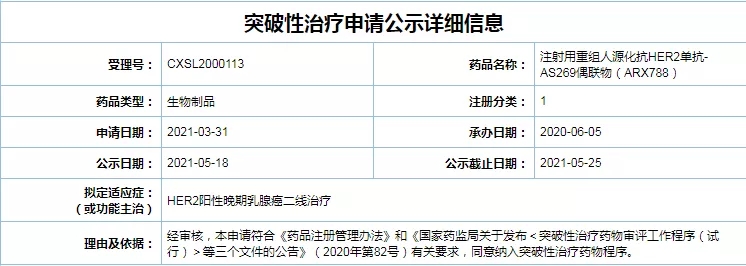
国家药监局官网
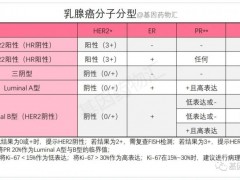
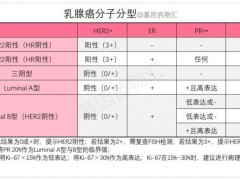
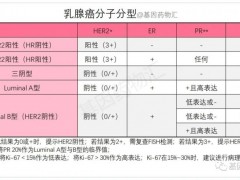
当前乳腺癌已成为全球发病率最高的癌症,其中HER2阳性约占全部乳腺癌的20%~25%,这类患者往往具有预后差、疾病易复发、生存期短的特点。目前,我国尚无抗HER2-ADC类药物在HER2阳性晚期乳腺癌二线治疗获批上市,巨大的临床需求有待填补。
ARX788是新码生物与Ambrx共同开发的一款靶向HER2阳性肿瘤抗体药物偶联物(ADC)。该产品由2个细胞毒素分子AS269与曲妥珠单抗借助非天然氨基酸专利定点偶联技术制成,能够实现毒素在单抗分子上的精确偶联,从而实现更高的安全性及稳定性。
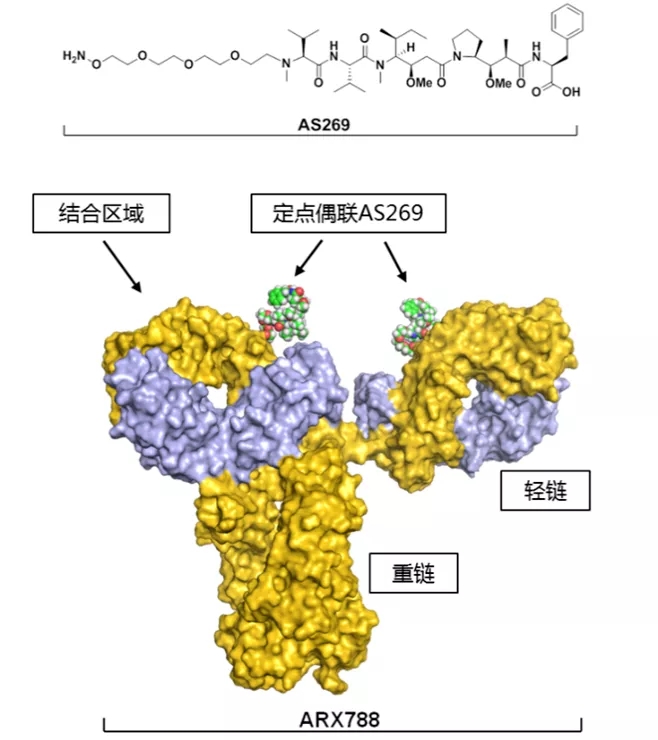
图片源自新码生物
目前,ARX788治疗HER2阳性晚期乳腺癌的Ⅰ期临床研究正在进行。根据新码生物公布的数据,截止2021年1月21日,69名患者中有33人达到客观缓解,总客观缓解率(ORR)为47.8%,其中1.5 mg/kg Q3W(II期推荐剂量)剂量组ORR为65.5%,并且患者接受治疗后的不良反应以轻中度为主,显示该产品具有良好的安全性。
据悉,ARX788针对乳腺癌和胃癌的II/III期临床研究已经相继启动,国内开发进度快于欧美。在美国,ARX788已获得FDA授予快速通道资格,用于治疗已接受过一种或多种抗HER2治疗的晚期或转移性HER2阳性乳腺癌,以及FDA授予孤儿药资格,治疗HER2阳性胃癌和胃食道结合部癌。
推荐阅读:
浙江医药ARX788临床试验,评价重组人源化抗HER2单抗-AS269抗体偶联药物(ARX788)治疗HER2阳性的晚期乳腺癌临床试验
内容太专业看不懂?没关系,点击在线咨询,在线客服会详细为您讲解招募相关情况,欢迎咨询!
参考资料:
[1]新码生物官网
[2]国家药监局官网
[3]http://www.myzaker.com/article/6024c9088e9f094e861decaf
[4]https://mp.weixin.qq.com/s/utnfO13QMye6ld5-fdRhuw
内容来源:林山月 生物探索