2022年7月29日罗氏不限癌种的广谱抗癌药恩曲替尼(Entrectinib)胶囊在中国获批上市
2022年7月29日,中国国家药监局(NMPA)官网公示显示,罗氏(Roche)公司申报的恩曲替尼(entrectinib)胶囊已在中国获批。公开资料显示,恩曲替尼是一款针对NTRK和ROS1基因融合而设计的特异性酪氨酸激酶抑制剂,本次申请用于治疗NTRK融合阳性局部晚期或转移性实体瘤。

截图来源:NMPA官网
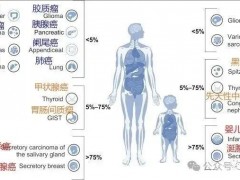
NTRK融合阳性肿瘤产生的原因是NTRK1/2/3基因与其它基因融合,导致编码的TRK蛋白(TRK A/B/C)出现异常,激活与特定癌症增殖相关的信号通路。NTRK基因融合可能出现在起源于身体不同位置的肿瘤中,包括乳腺癌、胆管癌、结直肠癌、神经内分泌癌、非小细胞肺癌、胰腺癌等等。
恩曲替尼是罗氏开发的一款针对NTRK和ROS1基因融合而设计的特异性酪氨酸激酶抑制剂,它能够抑制TRK A/B/C和ROS1激酶活性。2019年6月,恩曲替尼获得日本厚生劳动省批准,治疗携带NTRK基因融合的晚期复发实体瘤患者。随后该药又获得美国FDA加速批准,用于治疗携带NTRK基因融合的成年和青少年癌症患者,以及携带ROS1基因突变的非小细胞肺癌患者,成为了FDA批准的第三款“不限癌种”的抗癌疗法。
2021年10月,中国国家药品监督管理局药品审评中心(CDE)受理了恩曲替尼胶囊的上市申请,并将其纳入优先审评。根据优先审评公示信息,该药本次申请拟用于治疗NTRK融合阳性局部晚期或转移性实体瘤。

截图来源:CDE官网
恩曲替尼治疗NTRK融合阳性局部晚期或转移性实体瘤的效果已在多项临床试验中得到验证,其中包括名为STARTRK-2的关键性2期临床试验,以及名为STARTRK-1和ALKA-372-001的1期临床试验。对这些试验数据的汇总分析表明:
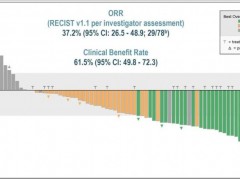
在NTRK融合阳性实体瘤患者中,接受恩曲替尼治疗的患者客观缓解率(ORR)为57.4%,中位缓解持续时间(DOR)为10.4个月;
多达10种不同类型的实体瘤患者对这一疗法产生响应;
对于肿瘤转移到大脑的实体瘤患者,恩曲替尼也能达到54.5%的颅内客观缓解率,获得缓解的患者中四分之一达到完全缓解。
希望罗氏的恩曲替尼早日来到患者身边,让他们拥有新的治疗选择。
参考资料:
[1]2022年07月29日药品批准证明文件待领取信息发布 . Retrieved July 29, 2022. From https://www.nmpa.gov.cn/zwfw/sdxx/sdxxyp/yppjfb/20220729132536104.html
[2] Japan becomes the first country to approve Roche’s personalised medicine Rozlytrek. Retrieved June 18, 2019, from https://www.roche.com/media/releases/med-cor-2019-06-18.htm
[3] FDA approves third oncology drug that targets a key genetic driver of cancer, rather than a specific type of tumor. Retrieved August 15, 2019, from https://www.prnewswire.com/news-releases/fda-approves-third-oncology-drug-that-targets-a-key-genetic-driver-of-cancer-rather-than-a-specific-type-of-tumor-300902681.html
内容来源:医药观澜