肿瘤治疗新进展,2022年度美国癌症研究协会癌症治疗5大突破性进展报告出炉
全球的癌症组织及研究者前仆后继,不断研发出全新的抗癌药物和技术纷纷亮相,向癌症宣战!
2022年9月21日,美国癌症研究协会在华盛顿特区发布了2022年度最新的癌症进展报告,报告中全面总结了从 2021年 8 月 1 日到 2022 年 7 月 31 日,刚刚过去的这一年里,癌症治疗最值得关注的新进展,全球肿瘤医生网医学部为大家整理了其中的精华部分,快来看下这份权威的报告给我们带来了哪些全新的抗癌希望。

注:AACR(美国研究协会)成立于1907年,是世界上成立最早,规模最大的致力于全面、创新和高水准癌症研究的科学组织。每年AACR都会公布年度最新的癌症治疗最新进展,包括目前癌症仍然存在的巨大挑战有哪些,以及癌症治疗取得了哪些重大突破,是全球最权威的进展盘点之一,对于医生和患者们意义重大!
美国癌症研究协会:癌症治疗五大支柱的突破性进展
美国癌症研究协会关于整个癌症治疗领域的进展统计显示,在过去一年中,横跨癌症治疗的五大支柱--手术、放疗、化疗、分子靶向治疗和免疫治疗都取得了重大进展,正在挽救更多的癌症患者并改善治疗效果。
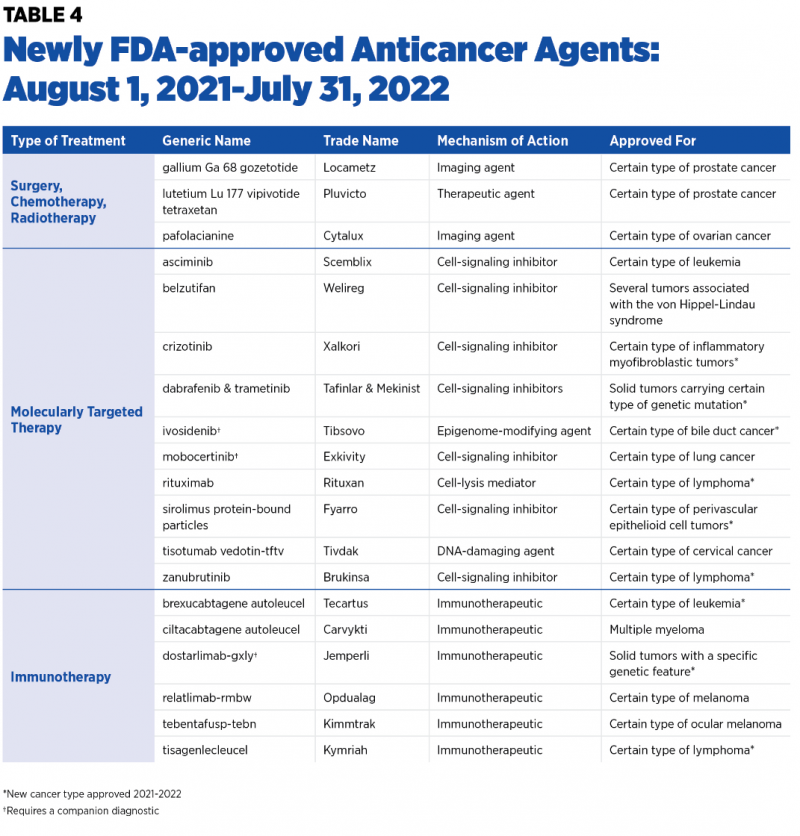
从 2021 年 8 月 1 日到 2022 年 7 月 31 日,FDA 已批准了 8 种新的抗癌疗法,同时FDA还扩大了10 种先前批准的抗癌疗法的使用范围,以治疗其他癌症类型,为更多患者带来新的治疗选择和希望。
(注:全球肿瘤医生网医学部为大家重点整理了新增药物的表单和药物详情,如果想申请其中新药的治疗,可以联系医学部评估是否符合免费用药条件。)
FDA新批准的抗癌疗法:2021年8月1日-2022年7月31日
手术
19世纪末以前,手术是治疗癌症患者的唯一方法,直至今日,手术仍是癌症治疗的第一大支柱。最近的一项研究表明,到 2040 年,全球对癌症手术治疗的需求将增加 52 % ( 413 ). 研究人员不断创新新的和改进的策略,以最大限度地提高癌症患者手术的益处并最大限度地减少伤害。
放疗
放射疗法在1896年成为癌症治疗的第二大支柱,临床中大约50%的患者需要接受放射治疗来缩小或消除肿瘤或防止局部复发。目前,立体定向消融放射治疗,调强放疗和质子质子是最先进的放疗技术,可以更精确地将放射线靶向肿瘤,避免肿瘤周围的健康组织受到放射线造成的损害,从而可以减少放射疗法的长期副作用。
化疗
细胞毒性化学疗法是第三种成为癌症治疗支柱的治疗方法)。如今,越来越多新型化疗药物能够提高患者生存率和生活质量。
靶向治疗
在 2021 年 8 月 1 日至 2022 年 7 月 31 日期间,FDA 批准了 8 种新的靶向疗法。其中最大的突破是全球首款且目前唯一一个用于BRAF V600E突变成人及儿童泛瘤种治疗药物组合获批。此外,FDA 还扩大了10种先前批准的分子靶向疗法的使用,以治疗新型癌症。越来越多的难治性靶点打破了治疗僵局,迎来了首款靶向药物,又有很多幸运的病友们等来了新的希望和治疗选择。
非小细胞肺癌
1、2021年9月15日,TAK788获批治疗EGFR20ins非小细胞肺癌
2021年9月15日,FDA 加速批准mobocertinib (Exkivity,莫博替尼,代号为TAK-788)用于EGFR外显子20插入突变的非小细胞肺癌成年患者。这是EGFR外显子20插入突变肺癌患者的第二款靶向疗法,是医学届对于这部分患者的一项重大进步,具有重大的意义!
乳腺癌
2、奥拉帕尼获批早期高危乳腺癌的辅助治疗
2022年3月11日,美国FDA批准奥拉帕尼(Lynparza)用于已经完成化疗和局部治疗的早期HER2阴性、BRCA突变的高危早期乳腺癌。
3、DS8201获批乳腺癌二线治疗适应症
2022 年 5 月 4 日,美国FDA批准 fam-trastuzumab deruxtecan-nxki (Enhertu, DS8201) 用于不可切除或转移性HER2阳性成年乳腺癌,既往全身治疗中曾接受抗HER2治疗,或于新辅助治疗或辅助治疗中接受抗HER2治疗并在治疗期间或治疗完成后6个月内发生疾病复发的患者。这是暨乳腺癌三线治疗及胃癌二线治疗后,DS8201获批的第三个适应症。
4、2021年10月12日,FDA批准Verzenio用于早期乳腺癌
2021 年 10 月 12 日,FDA批准 abemaciclib(Verzenio,礼来公司)与内分泌疗法(他莫昔芬或芳香酶抑制剂)联合用于激素受体(HR)阳性、人表皮生长因子成人患者的辅助治疗受体 2 (HER2) 阴性、淋巴结阳性、复发风险高且 Ki-67 评分≥20% 的早期乳腺癌。这是第一个被批准用于乳腺癌辅助治疗的 CDK 4/6 抑制剂。
甲状腺癌
5、2021年9月17日,FDA批准卡博替尼用于甲状腺癌
2021 年 9 月 17 日,FDA批准卡博替尼(Cabometyx,Exelixis,Inc.)用于 12 岁及以上患有局部晚期或转移性分化型甲状腺癌 (DTC) 的成人和儿童患者,这些患者接受过 VEGFR-靶向治疗或不适合或难以接受放射性碘的人。
胆管癌
6、2021年8月25日,FDA批准Tibsovo用于晚期胆管癌
2021 年 8 月 25 日,FDA批准 ivosidenib(Tibsovo,Servier Pharmaceuticals LLC)用于IDH1突变的既往治疗过的局部晚期或转移性胆管癌成年患者。
肾癌
7、FDA批准乐伐替尼联合派姆单抗一线治疗晚期肾癌
2021年8月10日,FDA批准乐伐替尼(Lenvima,卫材)联合派姆单抗(Keytruda,默克)用于成年晚期肾细胞癌(RCC)患者的一线治疗。
白血病
8、首个白血病IDH1抑制剂获批
2022 年 5 月 25 日,美国FDA批准 ivosidenib(Tibsovo)与阿扎胞苷联合用于新诊断的具有易感 IDH1 突变的75岁以上急性髓性白血病(AML)患者。Ivosidenib是IDH1酶的一种口服靶向抑制剂,是FDA批准的治疗R/R AML和IDH1突变患者的第一个也是目前唯一的治疗方法。
宫颈癌
9、2021年9月20日,FDA批准Tivdak用于晚期宫颈癌
2021 年 9 月 20 日,FDA加速批准了 tisotumab vedotin-tftv(Tivdak,Seagen Inc.),这是一种组织因子导向抗体和微管抑制剂偶联物,用于化疗后疾病进展的复发性或转移性宫颈癌成人患者。
前列腺癌
10、PSMA阳性前列腺癌首款靶向放射配体疗法获批
2022年3月23日,FDA批准靶向放射性配体疗法Pluvicto(Lutetium Lu 177 vipivotide tetraxetan)上市,用于治疗前列腺特异性膜抗原(PSMA)阳性、转移性去势抵抗性前列腺癌(mCRPC)患者。Pluvicto是首款被FDA批准的用于治疗这类mCRPC患者的靶向放射配体疗法。
实体瘤
11、全球首款BRAF V600E泛癌种疗法获批
2022年6月22日,FDA 已加速批准 dabrafenib 联合曲美替尼用于治疗 6 岁及以上患有不可切除或转移性实体瘤、携带 BRAF V600E 突变且在先前治疗后进展且没有令人满意的替代治疗选择的成人和儿童患者。值得一提的是,这是全球首款且目前唯一一个获批用于BRAF V600E突变成人及儿童泛瘤种治疗药物组合,同时,这也是BRAF/MEK抑制剂首次获批用于儿童患者的治疗,具有里程碑式的意义!
免疫治疗
癌症免疫治疗通过释放患者免疫系统的能力来对抗癌症,肿瘤的免疫治疗虽发展晚,却以前所未有的速度进入临床,近年来,它已成为癌症治疗的第五大支柱,并有望最终成为治愈肿瘤的重要武器。
我们一起看下过去一年有哪些新批准的免疫疗法给病友们带来生存奇迹。
免疫检查点抑制剂(PD-1/L1)
2021 年 8 月 1 日至 2022 年 7 月 31 日期间,多种免疫检查点抑制剂已被批准用于治疗 各类实体瘤。最重要进展之一是 FDA 批准了一种新的检查点抑制剂 relatlimab,用于治疗转移性黑色素瘤。此外,FDA 还扩大了四种先前批准的检查点抑制剂的使用——cemiplimab-rwlc (Libtayo)、nivolumab (Opdivo)、pembrolizumab (Keytruda) 和 ipilimumab (Yervoy)。
1、首个非小细胞肺癌新辅助治疗-OPDIVO+化疗方案获批
2022年3月4日,美国FDA批准Opdivo(nivolumab,O药)联合化疗,作为新辅助疗法,治疗可切除(肿瘤≥4cm或淋巴结阳性)非小细胞肺癌患者,不论患者PD-L1表达情况。这是首个也是目前唯一一个获批的NSCLC术前新辅助治疗方案。
2、2021年10月15日,阿特珠单抗获批非小细胞肺癌辅助治疗
2021 年 10 月 15 日,FDA批准批准Tecentriq(T药)用于 II 至 IIIA 期转移性非小细胞肺癌 (NSCLC) 患者手术及铂类化疗后的辅助治疗,PD-L1 ≥ 1% 。这是第一个、也是目前唯一一个可以用于非小细胞肺癌辅助治疗的癌症免疫疗法。这一方案开启了一个全新的时代,让早期肺癌患者也有接受免疫治疗的机会,并增加临床治愈的比例。
3、2021年10月13日,派姆单抗获批宫颈癌一线治疗
2021 年 10 月 13 日,FDA批准派姆单抗(Keytruda,默克)联合化疗,联合或不联合贝伐单抗,用于PD-L1(CPS ≥1)的持续性、复发性或转移性宫颈癌患者。
4、2021年8月19日,FDA批准纳武单抗用于尿路上皮癌
2021年8月19日,FDA批准nivolumab(Opdivo,Bristol-Myers Squibb Co.)用于接受根治性切除术后复发风险高的尿路上皮癌(UC)患者的辅助治疗。
5、2021年12月3日,FDA批准派姆单抗用于成人及儿童黑色素瘤的辅助治疗
2021 年 12 月 3 日,FDA批准派姆单抗(Keytruda,默克)用于IIB 或 IIC 期成人和儿童(≥12 岁)完全切除后的黑色素瘤患者的辅助治疗。
6、2021年8月17日,FDA批准Jemperli用于晚期实体瘤
2021 年 8 月 17 日,FDA加速批准 dostarlimab-gxly (Jemperli, GlaxoSmithKline LLC) 用于治疗错配修复缺陷 (dMMR) 复发性或晚期实体瘤成年患者,这些患者既往接受过治疗后进展或临床上没有治疗选择。
7、全球首款LAG-3免疫疗法获批上市!"史上最强"双免疫疗法诞生
2022年3月18日,FDA 批准 relatlimab (瑞拉利单抗)联合nivolumab 的固定剂量组合用于治疗 12 岁或以上且患有不可切除或转移性黑色素瘤的成人和儿童患者,这一“黄金搭档”也有了专属的名字--Opdualag。这是全球首款LAG-3抑制剂,也是继PD-1和CTLA-4之后第三个应用于临床的免疫检查点,具有里程碑式的意义!这款疗效更好的新型的免疫疗法将给癌症患者带来全新的“治愈”希望!
8、免疫联合疗法获批食管癌一线治疗
2022年5月27日,美国FDA批准了免疫疗法纳武利尤单抗(Opdivo,即O药)两种联合治疗方案(O药与含氟嘧啶和含铂化疗联用;O药与伊匹木单抗(Y药)联用)作为一线疗法,治疗晚期不可切除或转移性食管鳞状细胞癌(ESCC),无论患者PD-L1状态如何。这两种基于纳武利尤单抗的联合疗法都显示出巨大的生存获益,为食管癌患者提供了更好的治疗选择。9子宫内膜癌迎来第三款免疫疗法
2022年3月22日,FDA批准了派姆单抗(Pembrolizumab,Keytruda)的新适应症,用于经过前线全身治疗后疾病进展的微卫星不稳定性高(MSI-H)或错配修复缺陷(dMMR)的晚期子宫内膜癌患者,这些患者必须不适合接受治愈性手术或放射治疗。好消息是,除了派姆单抗,众多子宫内膜癌的新药目前正在临床招募中,想参加的患者可以通过方舟新药计划申请。
过继性细胞免疫疗法(CAR-T、TILs、TCR-T)
另一种在某些类型的癌症上表现出非凡成功的免疫疗法称为过继细胞疗法或细胞免疫疗法,这种方法可以显着增加杀死癌症的 T 细胞的数量,从而增强患者的免疫系统以寻找和摧毁癌细胞。
1、全球首款实体瘤TCR-T细胞免疫疗法获批
2022年1月25日,FDA批准tebentafusp-tebn(Kimmtrak,Immunocore Limited),一种双特异性 gp100 肽-HLA 导向的 CD3 T 细胞接合剂,用于 HLA-A*02:01 阳性的无法切除或转移性葡萄膜黑色素瘤。值得一提的是,这是2022年FDA批准的全球首款抗癌疗法,同时也是全球首款获批的实体瘤TCR-T疗法,这意味着T细胞疗法向实体瘤正式发起挑战,具有里程碑式的意义!
2、首款国产CAR-T疗法获批骨髓瘤
2022年2月28日,FDA批准传奇生物的靶向BCMA CAR-T疗法--Carvykti 上市,用于治疗复发或难治性多发性骨髓瘤(R/R MM)患者,这些患者既往接受过四种或四种以上的治疗,包括蛋白酶体抑制剂、免疫调节剂和抗CD38单克隆抗体,给晚期走投无路的患者带来了新的选择,同时它也有了自己的大名--西达基奥仑赛。值得一提的是,这是首款国产的CAR-T免疫疗法获得FDA批准上市,意味着中国的CAR-T疗法正式登上世界舞台!这是中国抗癌史上又一值得镌刻的里程碑!
3、大B细胞淋巴瘤全球首款二线CAR-T疗法
2022年4月1日,FDA批准CAR-T细胞治疗药品Yescarta用于一线化疗免疫疗法难治或一线化疗免疫疗法后12个月内复发的大B细胞淋巴瘤(LBCL)成年患者。这也是全球首款获得FDA批准作为LBCL二线疗法的CAR-T药物。
4、首款CAR-T疗法获批滤泡淋巴瘤
2022 年 5 月 27 日,美国 FDA加速批准 tisagenlecleucel(Kymriah)用于治疗两线或多线全身治疗后的复发或难治性滤泡性淋巴瘤(FL)成年患者。这是FDA 批准的Kymriah 的第三项适应证,也是在成人/儿童适用疗法中唯一获批的 CAR-T 细胞疗法。好消息是,众多CAR-T疗法目前正在临床招募中,想参加的患者可以通过方舟新药计划申请。
5、大B细胞淋巴瘤第二款二线CAR-T疗法获批
2022年6月25日,FDA批准了Breyanzi(lisocabtagene maraleucel,liso-cel),用于成人大 B 细胞淋巴瘤患者的二线治疗(包括弥漫性大 B 细胞淋巴瘤、高级别 B 细胞淋巴瘤、原发性纵隔大 B 细胞淋巴瘤和滤泡性淋巴瘤淋巴瘤 3B 级)。
未来,癌症治愈终将成为现实
癌症研究处在一个令人兴奋时代。近年来在癌症基因组学和免疫学研究的发现成功建立起了癌症治疗的两大支柱——靶向疗法和免疫疗法。它们为更多不同类型的癌症患者造福。随着这些新型抗癌药物、疫苗和不断开发中的单克隆抗体研究,将被称为“绝症”的晚期癌症变为一种慢性疾病,从根本上改变对癌症治疗的观念。我们期待,从现在起20年后,人类能够接种疫苗来预防癌症,战胜癌症,相信这一天离我们不远了!
参考资料:
https://www.aacr.org/