中国获批上市的CAR-T细胞疗法有哪些
我国已获批的五款CAR-T疗法,在血液肿瘤治疗领域"大展拳脚"
随着印度NexCAR19的研发成功,CAR-T未来的发展与竞争势必会更加激烈!印度具有独特的仿制药及专利保护政策,与中国已有五款CAR-T产品获批上市不同,印度的CAR-T研发领域一直处于空缺状态,故而可牺牲一定的产品疗效,来兑换性价比和可及性,从目前局势来看,印度的CAR-T之路难以被中国复制。不过值得欣慰的是,在各方的努力下,我国CAR-T疗法的降价空间也已打开,而且疗效取得了更为亮眼的成绩!
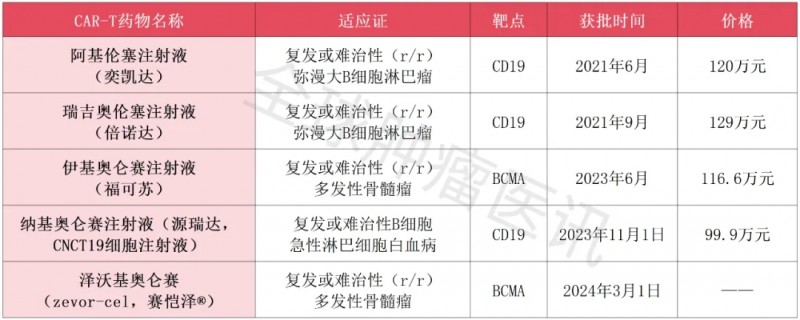
▲我国已获批的CAR-T产品
01、阿基仑赛:剑指大B细胞淋巴瘤,总生存率达84.3%
阿基仑赛注射液(奕凯达®,FKC876)是由复星凯特生物公司研发的一款靶向CD19的CAR-T细胞产品,2021年6月22日,获中国国家药监局(NMPA)批准上市适用于成人复发或难治性(R/R)大B细胞淋巴瘤。该药是中国首款获批上市的CAR-T疗法,同时也是全球第6款获批上市的CAR-T产品!
研究显示,阿基仑赛治疗复发难治性非霍奇金淋巴瘤,12个月总生存率高达84.3%,最佳完全缓解率(CRR)为58.4%,最佳总缓解率达83.2%。
02、瑞基奥仑赛:重击大B细胞淋巴瘤,中位总生存率高达90.8%
瑞基奥仑赛注射液(倍诺达®,relma-cel)是由药明巨诺研发的一种靶向CD19的CAR-T细胞产品,中国国家药监局(NMPA)于中国国家药监局(NMPA)批准其上市,用于成人复发或难治性大B细胞淋巴瘤(r/r LBCL)(二线或以上系统治疗失败)。它是中国获批的第二款CAR-T产品!
瑞基奥仑赛在2020年美国血液学会(ASH)年会上,公布了其惊艳的数据,在58例可评估疗效的r/r LBCL患者中,结果显示:
1)3个月的完全缓解率(CR)达51.7%,客观缓解率(ORR)达58.6%。
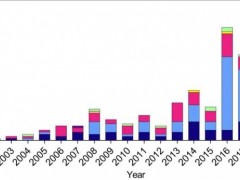
2)6个月的中位总生存(OS)率为90.8%,无进展生存(PFS)率为54.2%,缓解持续时间(DOR)为60%(详见下图)。
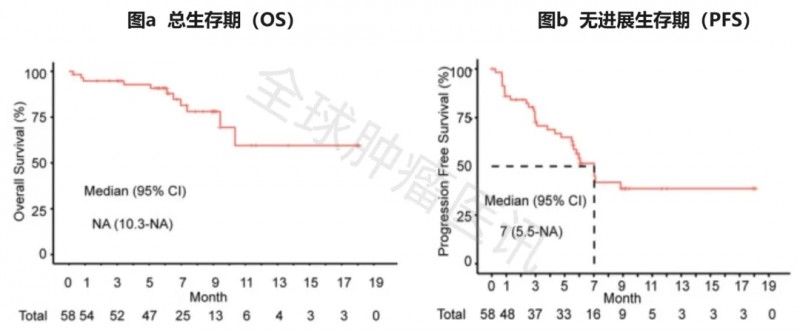
▲图源“Cancer Med”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
03、伊基奥仑赛:多发性骨髓瘤克星,总缓解率高达96.0%
伊基奥仑赛注射液(福可苏®)是由信达生物及驯鹿生物合作研发的一款BCMA CAR-T细胞疗法,国家药品监督管理局(NMPA)于2023年6月30日批准其上市,治疗复发/难治性多发性骨髓瘤(R/R MM)。它是全球首款全人源靶向BCMA CAR-T疗法!同时也是中国首款获批的BCMA CAR-T产品!
1/2期临床研究(FUMANBA-1),共纳入103例既往接受过≥3线治疗的R/R MM患者,入组接受伊基奥仑赛治疗后,经过13.8个月的中位随访,结果显示如下:
在101例可评估疗效的患者中,总体缓解率(ORR)高达96.0%(97/101),12个月中位无进展生存期(PFS)率达78.8%(95% CI: 68.6–85.97),严格意义的完全缓解/完全缓解率(sCR/CR)为74.3%(75/101)。
04、纳基奥仑赛:重锤B细胞急性淋巴细胞白血病,ORR可达82.1%
纳基奥仑赛注射液(CNCT19细胞注射液,源瑞达®)是由合源生物研发的一款CAR-T细胞产品,2023年11月8日,国家药监局(NMPA)批准上市,用于治疗复发或难治性B细胞急性淋巴细胞白血病(r/r B-ALL)的成人患者,国内定价为99.9万元/支。
在第64届美国血液学年会(ASH)上,公布了该药的一项关键性临床研究结果(NCT04684147),共纳入39例成人r/r B-ALL患者,结果显示:
1、总体缓解率(ORR):治疗3个月内的ORR高达82.1%,治疗3个月时的ORR达64.1%。
2、完全缓解(CR)率:治疗3个月内获ORR的患者(32例),其CR率达66.7%;治疗3个月时获ORR的患者(25例),其CR率达51.3%。
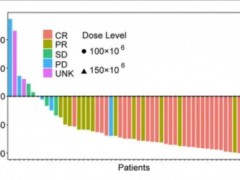
2、微小残留病灶(MRD)阴性率:在治疗≤3个月时,达CR患者其MRD阴性率为92.0%;达CR/CRi(完全缓解但计数不完全恢复)的患者,其MRD阴性率竟然达到100%(详见下图)!
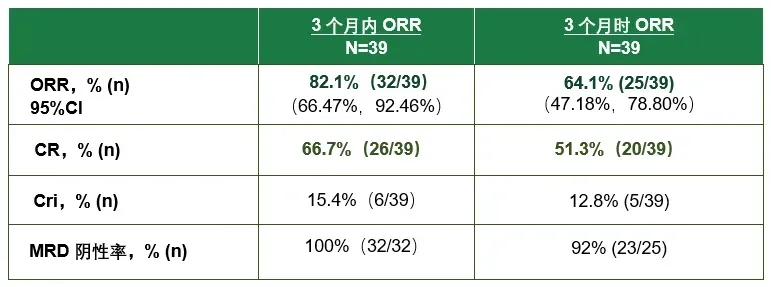
▲纳基奥仑赛有效性数据总结
05、泽沃基奥仑赛:78.6%获完全缓解
泽沃基奥仑赛(zevor-cel,赛恺泽®)是由科济药业研发的一款自体BCMA靶向的CAR-T细胞产品,国家药品监督管理局于2024年3月1日,批准其新药上市申请,用于复发或难治性多发性骨髓瘤(R/R MM)的治疗。它是第二款BCMA靶向的CAR-T产品,同时也是我国上市的第五款CAR-T细胞产品!
本次获批主要基于“泽沃基奥仑赛的Ⅰ/Ⅱ期临床试验(LUMMICAR STUDY 1,NCT03975907)”结果。本次研究共入组14例R/R MM患者,中位年龄为54岁,既往接受过至少3种治疗方案。患者入组后现接受淋巴细胞清除治疗,之后单次输注泽沃基奥仑赛注射液,经过37.7个月的中位随访,结果显示:
1)总缓解率(ORR):ORR达到了惊人的100%(14/14)!其中78.6%获得完全缓解(CR)或严格完全缓解(sCR);21.4%获得部分缓解(PR)。
2)中位缓解持续时间(DOR):全部患者的中位DOR达24.1个月,sCR/CR患者的中位DOR达26.0个月。
3)无进展生存期(PFS):全部患者的中位PFS达25.0个月,sCR/CR患者的中位PFS达26.9个月(详见下图)。
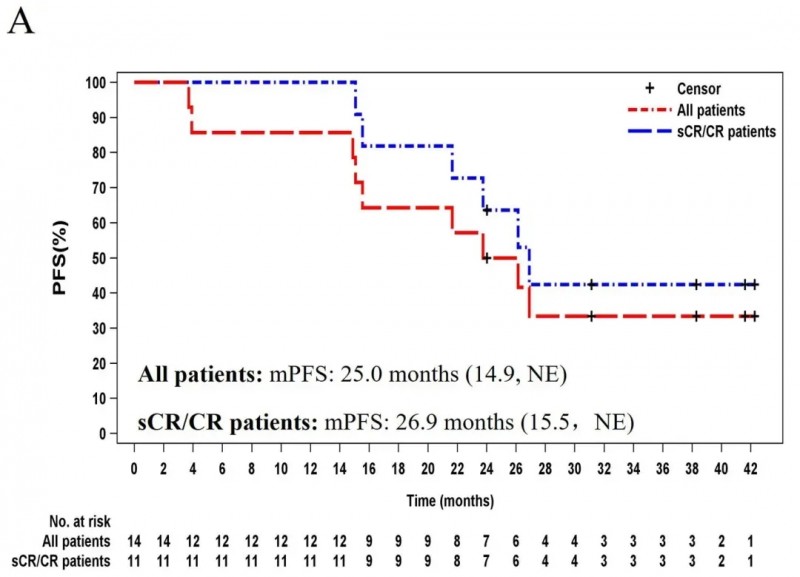
▲图源“ScienceDirect”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
综上,经过3年的随访,泽沃基奥仑赛治疗R/R MM,保持了深度和持久的反应,且安全性良好!
小编寄语
我国CAR-T的研发一直紧随美国,处于世界领先位置。而且近年来,我国也在尝试攻坚病毒载体,探索通用型细胞治疗产品(包括异体CAR-T、CAR-NK等),以期望降低成本,让CAR-T这一新兴的抗癌“明星产品”能惠及更多的患者!
目前我国多款CAR-T细胞疗法正在招募患者,感兴趣的病友可将近期病理结果、出院小结、治疗经历等资料,提交至医学部,进行初步评估。