TIL疗法治疗实体瘤肿瘤大幅缩小或完全消失,缓解超76个月
当亲身经历医生使用TIL疗法帮助我的免疫系统培育出一支T细胞大军来对抗黑色素瘤后,我是惊讶又欣慰的,从来没想到能够用自身免疫细胞来杀灭癌细胞!
——罗伯托·罗梅罗 (Roberto Romero)
标准疗法用尽!打入肿瘤内部的"特种兵"TILs疗法让患者绝处逢生
自从2015年患上黑色素瘤开始直到2022年的夏天,Roberto Romero已经接受了几次手术和多轮药物治疗,几乎用尽了所有标准治疗手段。但癌症(最初只是脚趾甲下的一个黑点)仍在继续生长,并且已经侵入了他的器官。
临近2022年的圣诞节,Roberto机缘巧合下开启了TILs疗法的治疗之旅。外科医生在手术后从他的腹部靠近结肠内壁切除了肿瘤。在康复后,他接受了高剂量化疗,让身体为TILs治疗做好准备,细胞被送至实验室进行培养。10天后,培育的细胞通过他胸部的一个端口注入,在整个系统中循环并狙击更多的癌细胞。随后,他又服用名为白细胞介素-2的免疫刺激药物,以进一步增强他的免疫系统。
最初的几周对于Roberto相当煎熬,他经常发高烧,庆幸在坚持治疗下情况好转。让他感到惊讶和欣慰的是,CT扫描显示他的肿瘤正在缩小,这实在是太神奇的治疗经历!
这位癌症患者的肿瘤病灶逐渐缩小得益于一种新型的细胞免疫疗法——肿瘤浸润淋巴细胞(TIL)疗法,也是今天无癌家园小编要给各位癌友们详细介绍的主角。
让你认识下"古老"的TIL细胞疗法
TILs疗法可以说是一种“古老”的细胞疗法,拥有30多年的历史,早在1988年,美国癌症研究员的Steven Rosenberg主任,就通过对TIL细胞的研究和改进,发明了此种癌症治疗方法。
TILs是一种对实体肿瘤有着天然归巢优势的细胞免疫疗法,即从患者的肿瘤中分离出淋巴细胞,将分离的细胞在体外激活扩增或加以改造,然后再回输到患者体内。通俗点讲,这款疗法相当于直接从战场上拉回有战斗经验的老兵,经过一轮“政治审查”和业务能力“大比拼”,把内奸、叛徒尽量剔除出去,留下战斗力最强的,提供补给,再重新送回战场继续战斗。
与其他免疫疗法(例如,CAR-T、PD-1/PD-L1抗体)相比,TIL具有多靶点、肿瘤趋向和浸润能力强、副作用小等优势;是实体瘤治疗的理想选择,前景广阔。最早用于恶性黑色素瘤,近年来在宫颈癌、肺癌等多种实体瘤中都体现出了不俗的数据。
2024年2月16日,Iovance Biotherapeutics公司宣布Lifileucel(LN-144)获得美国食品和药物管理局(FDA) 批准上市,用于治疗PD-1抗体治疗后进展的晚期黑色素瘤,商品名为AMTAGVI™。这是全球首款获批上市的TIL疗法,也是全球首款获批的用于治疗实体瘤的T细胞疗法,具有里程碑的意义!

▲ 图片来源:FDA官网
目前无癌家园有TILs免疫细胞临床试验正在招募中,主要治疗黑色素瘤、肺癌、头颈部鳞癌、食管鳞癌、宫颈癌、子宫内膜癌;乳腺癌,卵巢癌,输卵管癌,肾癌,尿路上皮癌等实体瘤。
有意向的患者若想参加可整理出完整的病理报告、治疗经历、出院小结等再致电医学部,详细评估病情。
肿瘤部分缓解持续76个月,TIL疗法联合PD-1挑战转移性黑色素瘤
近期备受瞩目的2024年第115届美国癌症研究协会(AACR)年会刚落幕不久。作为全球历史悠久的肿瘤研究学术会议之一,AACR年会一直引领着肿瘤研究的前沿。其中就不伐抗癌领域的焦点——细胞治疗,大会上也更新了大家备受关注的TIL疗法。
一项针对帕博利珠单抗联合淋巴细胞清除、使用肿瘤浸润淋巴细胞(TIL)的过继细胞移植(ACT)和高/低剂量IL-2治疗转移性黑色素瘤患者的II期临床研究中,共纳入14例患有皮肤、葡萄膜、黏膜或未知的原发性黑色素瘤的患者分别为8例、2例、2例、2例。所有患者既往接受过至少3种疗法,其中包括抗PD-1治疗(n=13)。

在肿瘤标本采集盒TIL扩增后,用环磷酰胺和氟达拉滨对患者进行淋巴清除,然后输注离体扩增的 TIL 联合 IL-2(第1组:720,000 IU/kg IV,每8小时至15剂;第2组:200万IU SC,持续14天)。在TIL输注后21天开始,给予患者静脉注射200mg 帕博利珠单抗,随后每3周给药一次,持续2年,观察其临床疗效。
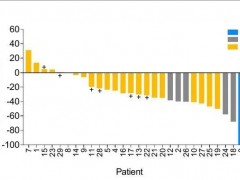
结果显示,在第1组中,1例患者在10个月内部分缓解(PR),2名患者病情稳定(SD),3名患者病情进展(PD),1名患者无法评估(NE)。在第2组中,1名患者PR持续超过76个月,1名患者SD,5名患者PD。由于每组的ORR<40%,治疗14名患者后停止入组。两组患者的无进展生存期和总生存期无显著差异。
综上所述,该治疗策略在低剂量和高剂量IL-2之间无显著差异,提示低剂量IL-2作为替代方案的潜力。
完全缓解率33%,客观响应率50%!新型TIL疗法OBX-115小试牛刀!
在2024年AACR大会上,来自美国安德森癌症治疗中心的研究人员公布了新型TIL疗法——OBX-115的1期临床试验结果。截止到报告时间,共纳入6例晚期转移性黑色素瘤患者,将其分为两组,一组接受30亿细胞回输配合125mg乙酰唑胺,另一组接受100亿细胞回输配合125mg乙酰唑胺。所有患者均采用过多线治疗且出现免疫耐受,平均治疗线数2.5,经过11-51周(中位数20周)的治疗后随访,2名患者完全缓解(CR),1名患者部分缓解(PR),2名患者情况稳定(SD)。所有患者均仍在世,6个月无进展生存期达到了67%!
值得一提的是,OBX-115是首款无需配合白介素2使用的TIL疗法,因而也避免了使用白介素2所产生的毒性。
专家提醒:手术后将TILs细胞储存起来
几乎所有患者的肿瘤组织在手术后仅取一小部分做成病理蜡块,其余部分就直接作为医疗垃圾处理掉,浪费了我们自身宝贵的抗癌资源!
建议大家在手术前争得主治医生的同意,将新鲜手术组织保存,交由专业机构将TIL细胞提取,可以在术后回输预防复发,或者是先冻存起来,以备未来不时之需。因为手术后未经其他治疗时新鲜组织中的TIL细胞对肿瘤的杀伤能力才是最强的,一旦接受化疗和放疗,免疫细胞的杀伤能力会被削弱。具体的方法和冻存流程大家可以致电医学部进行详情咨询。
国内研发产品层出不穷,横扫多种实体瘤
Lovance的全球首款获批上市的肿瘤浸润淋巴细胞(TIL)疗法Amtagvi定价为51.5万美元(约合人民币370万)。这在所有上市的免疫疗法中是最昂贵的,如此昂贵的天价让众多病友望而却步。
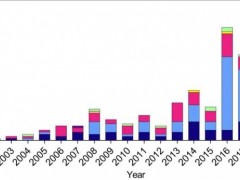
然而,国内方面,多家公司公布了TILs管线临床获批的好消息。整体而言,能够感受到TILs赛道的热度在持续上升并日趋白热化,国内研究者们也在不断突破创新。
1.百吉生物:BST02
2023年10月26日,百吉生物在实体瘤领域又一重磅产品BST02的I/II期临床试验申请获得美国FDA批准,用于治疗所有类型的肝癌,是全球首款进入临床阶段针对肝癌的TIL细胞治疗药品。
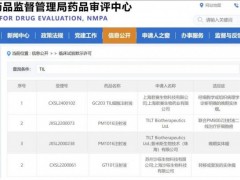
2.君赛生物:GC101
2022年4月24日,君赛生物自主开发的“自体天然肿瘤浸润淋巴细胞注射液(GC101 TIL)”(受理号:CXSL2200070)正式获得NMPA的临床试验默示许可。该产品是全球首个既不需要淋巴细胞清除也不需要IL-2输注的天然TIL细胞治疗产品。
GC101是君赛生物的首款TIL细胞新药品种,在前期研究者发起的临床研究(IIT)中,展现良好的安全性与有效性。2例受试者达到完全缓解(CR)疗效,3例受试者达到部分缓解(PR)疗效,CR持续时间已分别超过8个月与6个月,初步展示了GC101良好的安全性与有效性。
3.沙砾生物:GT101
2022年4月22日,中国国家药监局药品审评中心(CDE)官网显示,沙砾生物自主研发的GT101注射液(受理号:CXSL2200061)正式获得国家药品监督管理局(NMPA)的临床试验默示许可。值得一提的是,GT101是国内首个获批临床的肿瘤浸润淋巴细胞药物(TIL),具有里程碑式的意义!
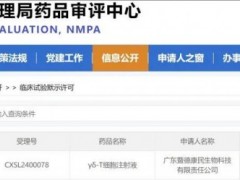
4.智瓴生物:ZLT-001
2023年1月28日,智瓴生物的ZLT-001注射液(受理号:CXSL2200552)正式获得国家药品监督管理局(NMPA)的临床试验默示许可,适应症为晚期复发或转移性宫颈癌,这是华南区首个获批临床的TIL药物,也是第三家在国内获批临床的TIL企业。
5.天科雅生物:HV-101
2023年1月29日,据CDE官网公示,天科雅生物医药科技有限公司提交的"HV-101注射液"获得临床试验默示许可,适应症为晚期复发或者转移性实体瘤(受理号:CXSL2200574)。
6.君赛生物:GC203
2024年2月6日,上海君赛生物自主研发的“GC203 TIL细胞注射液” 的新药临床试验(IND)申请获得国家药品监督管理局(NMPA)受理。
据无癌家园小编获悉,官方披露到,GC203为基因修饰TIL细胞药物,拟用于治疗晚期实体瘤。GC203是君赛生物第二款申请注册临床的TIL细胞新药,也是全球首个基于非病毒载体开发的TIL新药品种!第一款是之前无癌家园小编报道过的 GC101,同样也是用于治疗实体瘤的细胞新药。
与GC101一样,GC203无需清淋、无需IL-2注射联用,在普通病房便可完成整个治疗,预计单例患者便可节省15万+左右的配套临床费用,将大幅提升基因修饰TIL疗法的可及性。
据官方透露,在针对卵巢癌、宫颈癌、子宫内膜癌等妇科肿瘤的临床研究中,19例接受该候选产品治疗并可评估的晚期肿瘤患者中,肿瘤明显缩小,且长期缓解,疾病控制率(DCR)达84.2%,客观缓解率(ORR)为42.1%。让我们共同期待日后GC203将会给大家带来更多的惊喜!
7.沙砾生物:GT201
2023年7月11日,沙砾生物的第二款产品GT201,正式获得国家药品监督管理局的临床试验默示许可,成为国内首款进入注册临床试验的基因编辑型TIL药物。
GT201在体内外均表现出较传统TIL更强的增殖能力、肿瘤杀伤、细胞因子释放和更好的存续性,并可以降低对于IL-2的依赖性,从而克服传统TIL产品所面临的挑战,优化并提升传统TIL产品的功能和存续,并潜在降低临床应用中IL-2的使用剂量。此外,首个人体试验显示,GT201在多个晚期实体瘤患者体内均表现出良好的安全性,并展示出稳定的扩增和初步临床疗效。
8.沙砾生物:GT316
TILs的适应性细胞治疗在多种类型的实体瘤中表现出良好的治疗效果,并显著延长了晚期患者的生存期。然而,在制造过程中快速扩增后的最终TIL产品的 "易衰竭 "表型,以及肿瘤微环境(TME)中各种免疫抑制机制的存在,损害了TIL输注后的持久性和抗肿瘤功效。
而沙砾生物在2023年美国癌症研究协会(AACR)年会上,介绍了其下一代TIL疗法GT316,据报告称,该疗法能够解决TIL细胞在增殖过程中的衰竭,并保持疗效。
9.西比曼生物:C-TIL051
2022年10月,西比曼生物宣布FDA批准了公司新型TIL疗法C-TIL051的IND申请,适应证为PD-1抗体难治或复发的晚期非小细胞肺癌。
C-TIL051使用了西比曼生物专有的工艺,比传统制造方法生产的TIL更快、更有效地在人体内达到临床剂量。
从适应症布局看,多条管线对应多种适应症,覆盖黑色素瘤、非小细胞癌、宫颈癌、肺癌、头颈部鳞状细胞癌等广泛实体瘤癌种。
10.华赛伯曼:HS-IT101
2023年11月29日,华赛伯曼宣布,公司自主研发的首款TIL细胞1类新药——HS-IT101注射液(受理编号:CXSL2300599)用于治疗晚期实体瘤的IND申请获得NMPA临床试验默示许可。
HS-IT101是华赛伯曼自主研发的自体天然加强TIL产品,该产品是华赛伯曼首款获批进入临床的产品,预计在今年1月启动Ⅰ期临床试验。
11.蓝马医疗:LM103
2023年7月13日,国家药监局药品审评中心(CDE)官网显示,Medpark园内企业苏州蓝马医疗技术有限公司(以下简称:蓝马医疗)LM103注射液(TILs)正式获得国家药品监督管理局(NMPA)的临床试验默示许可。据无癌家园悉,这是国内TIL领域首个使用滋养细胞(Feeder)工艺的临床许可。
12.劲风生物:TILs疗法
2022年2月10日,劲风生物宣布其TILs疗法产品获得美国FDA批准进入临床一期。劲风生物成为国内首家TILs疗法产品获批进入临床的TILs疗法研发企业。
13.翊寿科技:自体肿瘤浸润淋巴细胞注射液
根据CDE官网,武汉翊寿科技和海南翊寿科技联合申报的1类新药“自体肿瘤浸润淋巴细胞注射液”已于2023年获批临床,拟开发用于肝癌等实体瘤的治疗。
14.卡替医疗:超强型TIL
2023年5月29日,卡替医疗的广谱抗癌细胞药物ScTIL——外周血来源的超强型类TIL细胞技术亮相2023年中关村论坛。
ScTIL技术是针对实体瘤的免疫细胞疗法,在外周血循环类TIL(cTIL)细胞的基础上负载靶向PD-L1的增强受体及CD19 CAR扩增因子,具有不限癌种、不限分期、不限肿瘤突变负荷的潜力和绝大多数肿瘤患者都适用的优势,且安全性和疗效较好。
15.毕诺济:BEN101
BEN101 注射液是专注于实体瘤领域的毕诺济(上海)生物技术有限公司自主研发的自体肿瘤浸润淋巴细胞(TILs)注射液,属于过继细胞疗法 (ACT),主要研究人群为晚期复发或转移性实体瘤(卵巢癌、宫颈癌、肾细胞癌和尿路上皮癌)。
小编有话说
目前,全球已经开展了TILs疗法针对转移性黑色素瘤、鼻咽癌、头颈部鳞状细胞癌、胆管癌、复发性或难治性卵巢癌、骨肉瘤、宫颈癌、卵巢癌、非小细胞肺癌、脑胶质瘤、胸膜间皮瘤等多种实体瘤的临床试验,TILs疗法在治疗包括转移性黑色素瘤、头颈部鳞状细胞癌、宫颈癌、非小细胞肺癌等多种实体瘤方面都展现出了临床价值。
此外,对于PD-1耐药的患者,接受TILs疗法也有显著疗效,无癌家园小编曾报道过关于TILs疗法联合PD-1让晚期转移性肺癌患者完全缓解的案例。
综上所述,TIL疗法在治疗实体瘤方面具有一些独特的优势,但仍面临一系列挑战。肿瘤免疫抑制微环境仍然是TIL治疗的主要障碍。此外,在有效肿瘤反应性 T 细胞的分离和扩增方面仍有相当大的改进空间,仍然需要探索替代联合疗法。
参考文献
1.https://www.fda.gov/news-events/press-announcements/fda-approves-first-cellular-therapy-treat-patients-unresectable-or-linkstatic-melanoma
2.https://aacrjournals.org/cancerres/article/84/6_Supplement/3605/740658/Abstract-3605-Phase-II-study-of-pembrolizumab-in
3.https://www.businesswire.com/news/home/20240409687216/en/Obsidian-Therapeutics-Presents-Positive-25-Week-Median-Study-Follow-Up-Safety-and-Efficacy-Data-from-First-in-Human-Study-of-OBX-115-in-Advanced-Melanoma-at-the-American-Association-for-Cancer-Research-Annual-Meeting
4.https://pubmed.ncbi.nlm.nih.gov/3264384/
5.https://www.ncbi.nlm.nih.gov/pmc/articles/PMC3131487/
6.https://www.iovance.com/
7.https://pubmed.ncbi.nlm.nih.gov/35727633/