CAR-T、TIL、TCR-T三种细胞免疫疗法上市的产品和免费的临床试验一览表
美国生物学家乔治•戴利曾说过:“如果20世纪是药物治疗的时代,那么21世纪就是细胞治疗的时代”!随着医学的不断进步,肿瘤免疫疗法也成为了继手术、放化疗后的第四类肿瘤治疗方法。其中,以CAR-T、TCR-T、TIL细胞疗法为代表的过继性T细胞疗法更是肿瘤免疫疗法中的“佼佼者”,近年来相继有多款产品获批上市,为实体瘤和血液肿瘤患者带来了新的希望与选择!下面全球肿瘤医生网小编就给各位癌友们,盘点一下目前已获批上市的CAR-T、TIL、TCR-T疗法,以及正在招募患者的临床试验,以供大家甄选!
CAR-T、TCR-T、TIL疗法:三足鼎立,各有所长
CAR-T细胞疗法:血液肿瘤克星
CAR-T细胞(嵌合抗原受体T细胞)疗法,是利用基因转导技术,在T细胞上安装一个名为“CAR”的“导航头”,改造后的T细胞可以精准识别并攻击肿瘤细胞,产生即时和长效的抗癌影响。目前国内外共有11款CAR-T产品获批,主要用于血液肿瘤的治疗。不过近年来,研究人员也在拓展CAR-T疗法的应用范围,将其用于实体瘤的治疗中,并取得了不俗的成绩。
TCR-T:实体瘤利器
“TCR-T细胞(T细胞受体工程化T细胞)疗法是通过基因工程技术,将抗原特异性TCR基因序列(α及β链),转移到T细胞中,使其特异性识别肿瘤抗原,并精准地杀死癌细胞。主要用于实体瘤的治疗,比如滑膜肉瘤、肝细胞癌、肺癌、难治复发性黑色素瘤、宫颈癌等,目前已有一款TCR-T产品获FDA批准上市,用于治疗滑膜肉瘤。
TIL疗法:取自肿瘤活检组织中的实体瘤黑科技
“TILs细胞(肿瘤浸润淋巴细胞)疗法是是从患者自身的肿瘤活检组织中,采集浸润的淋巴细胞,之后在体外进行扩增,并回输到患者体内的方法。相当于深入到敌军内部的免疫细胞敢死队,具有优越的肿瘤病灶浸润能力及低脱靶毒性,在治疗实体瘤(如黑色素瘤、肺癌、肝癌、乳腺癌、卵巢癌、宫颈癌等)方面具有独特的优势,目前已有一款治疗黑色素瘤的TIL疗法获批上市。这三种疗法的主要区别,详见下表:
▼CAR-T、TCR-T、TIL疗法对比
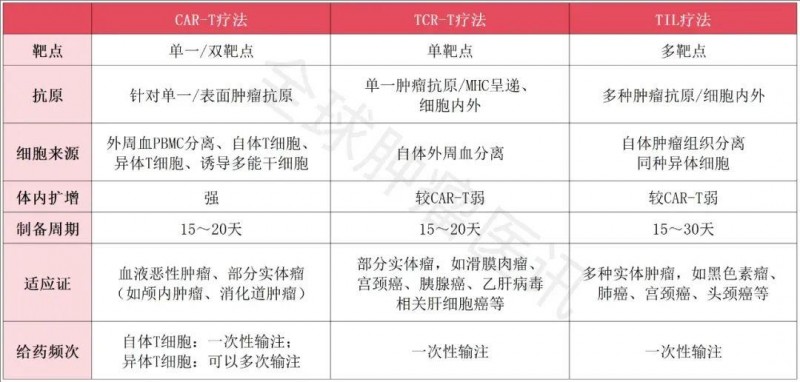
▲全球肿瘤医生网医学部整理汇总
CAR-T获批产品+临床招募一览表
已获批上市的11款CAR-T产品大盘点
目前国内外共有11款CAR-T产品获批上市,包括中国5款,美国6款。
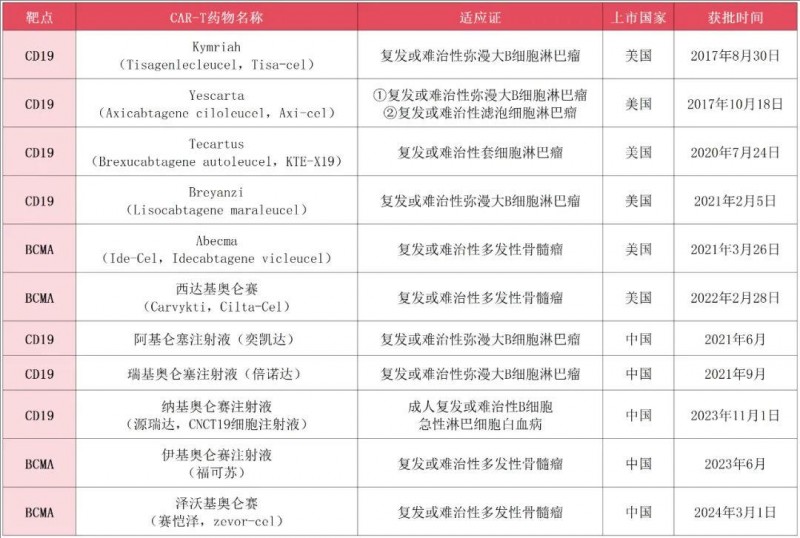
▲全球肿瘤医生网医学部整理汇总
1、Abecma
药物名称:Abecma(ide-cel,Idecabtagene vicleucel)。
上市时间:2024年4月4日。
研发公司:百时美施贵宝/蓝鸟生物公司。
药物介绍:Abecma是一种针对BCMA靶点的CAR-T细胞疗法,主要用于多发性骨髓瘤的治疗,它也是全球首个抗BCMA CAR-T细胞疗法!Abecma于2021年3月26日、2024年4月4日先后两次获美国食品药品监督管理局(FDA)批准,用于治疗复发/难治性多发性骨髓瘤、成年既往接受过≥2种治疗[的复发或难治性多发性骨髓瘤。3期KarMMa-3临床试验(NCT03651128)显示,它将疾病进展或死亡风险降低了51%!
2、西达基奥仑赛
药物名称:西达基奥仑赛(cilta-cel,Carvykti)
上市时间:2024年4月5日。
研发公司:传奇生物。
药物介绍:西达基奥仑赛是传奇生物和强生创新制药联合研发的一款靶向BCMA的CAR-T细胞疗法。2024年4月5日,获美国FDA批准,用于治疗成年复发或难治性多发性骨髓瘤(R/R MM)。它是首款获得FDA批准的国产CAR-T疗法!本次获批是基于3期CARTITUDE-4的临床研究(NCT04181827)的惊艳结果,完全缓解率(CR)高达73.1%!
3、伊基奥仑赛
药物名称:伊基奥仑赛注射液(福可苏®,Equecabtagene Autoleucel Injection)。
上市时间:2023年6月30日。
研发公司:驯鹿生物和信达生物。
药物介绍:伊基奥仑赛注射液是一款
全人源B细胞成熟抗原特异性CAR-T细胞,于2023年6月30日,获国家药品监督管理局(NMPA)批准上市,用于治疗复发/难治性多发性骨髓瘤(R/R MM),它是中国首款获批的BCMA CAR-T疗法!同时也是全球首款全人源BCMA靶向的CAR-T疗法!1/2期临床研究数据显示,总体缓解率(ORR)竟高达96.0%!
4、泽沃基奥仑赛
药物名称:泽沃基奥仑赛(zevor-cel,Zevorcabtagene Autoleucel,赛恺泽®,产品编号CT053)。
上市时间:2024年3月1日。
研发公司:科济药业。
药物介绍:泽沃基奥仑赛是一款自体BCMA靶向的CAR-T细胞产品,其新药上市申请于2024年3月1日,获国家药品监督管理局批准,用于复发或难治性多发性骨髓瘤的治疗。这是我国第五款上市的CAR-T细胞产品!同时也是国内第二款靶向BCMA的CAR-T产品!Ⅰ/Ⅱ期临床数据显示,78.6%的患者获得了完全缓解(CR)或严格完全缓解(sCR)!
5、Kymriah
药物名称:Kymriah(Tisagenlecleucel,Tisa-cel)。
上市时间:2017年8月30日。
研发公司:诺华制药。
药物介绍:Kymriah主要用于治疗复发或难治性弥漫大B细胞淋巴瘤(B-ALL),中位总生存期(OS)达10.5个月,完全缓解(CR)率超过60%!
6、Yescarta
药物名称:Yescarta(Axicabtagene ciloleucel,Axi-cel)。
上市时间:2017年10月18日。
药物介绍:Yescarta是一款针对CD19的转基因自体T细胞免疫疗法,用于治疗复发或难治性弥漫大B细胞淋巴瘤/滤泡细胞淋巴瘤,中位总生存期(OS)可达25.8个月。
7、Tecartus
药物名称:Tecartus(Brexucabtagene autoleucel,KTE-X19)。
上市时间:2020年7月24日。
药物介绍:TECARTUS是一种针对CD19的CAR-T细胞免疫疗法,用于复发或难治性套细胞淋巴瘤的治疗。2期ZUMA-3临床研究结果显示,完全缓解(CR)率达56%。
8、Breyanzi
药物名称:Breyanzi(liso-cel,利基迈仑赛,lisocabtagene maraleucel)。
上市时间:2024年3月15日。
研发公司:百时美施贵宝公司。
药物介绍:Breyanzi是一款针对CD19的转基因自体CAR-T细胞疗法。2024年3月15日,获美国FDA批准用于治疗成人复发或难治性(R/R)慢性淋巴细胞白血病(CLL)、小淋巴细胞淋巴瘤(SLL)。2024年5月30日,获美国FDA批准,用于治疗成年复发或难治性套细胞淋巴瘤(MCL)。
9、阿基仑赛注射液
药物名称:阿基仑赛注射液(奕凯达)。
上市时间:2021年6月1日。
研发公司:复星凯特。
药物介绍:阿基仑赛注射液是一款CD19 CAR-T产品,2021年6月22日在中国获批上市,用于治疗成人复发或难治性大B细胞淋巴瘤(r/r LBCL),它是中国首个以药品途径批准上市的CAR-T细胞治疗产品。
10、瑞基奥仑赛注射液
药物名称:瑞基奥仑赛注射液(倍诺达,relma-cel,JWCAR029)。
上市时间:2021年9月1日。
研发公司:药明巨诺。
药物介绍:瑞基奥仑赛注射液是一款靶向CD19的自体CAR-T治疗产品,于2021年9月1日在中国获批上市,用于治疗既往经过二线或以上系统性治疗后,复发或难治的大B细胞淋巴瘤。
11、纳基奥仑赛注射液
药物名称:纳基奥仑赛注射液(源瑞达®,CNCT19细胞注射液,Inaticabtagene Autoleucel Injection)。
上市时间:2023年11月8日。
研发公司:合源生物。
药物介绍:纳基奥仑赛注射液是一款靶向CD19的CAR-T细胞治疗产品,2023年11月8日在中国获批,用于治疗成人复发或难治性B细胞急性淋巴细胞白血病(r/r B-ALL)。它是中国首款治疗白血病的CAR-T细胞产品,治疗3个月总体缓解率(ORR)高达82.1%!
CAR-T临床招募一览表
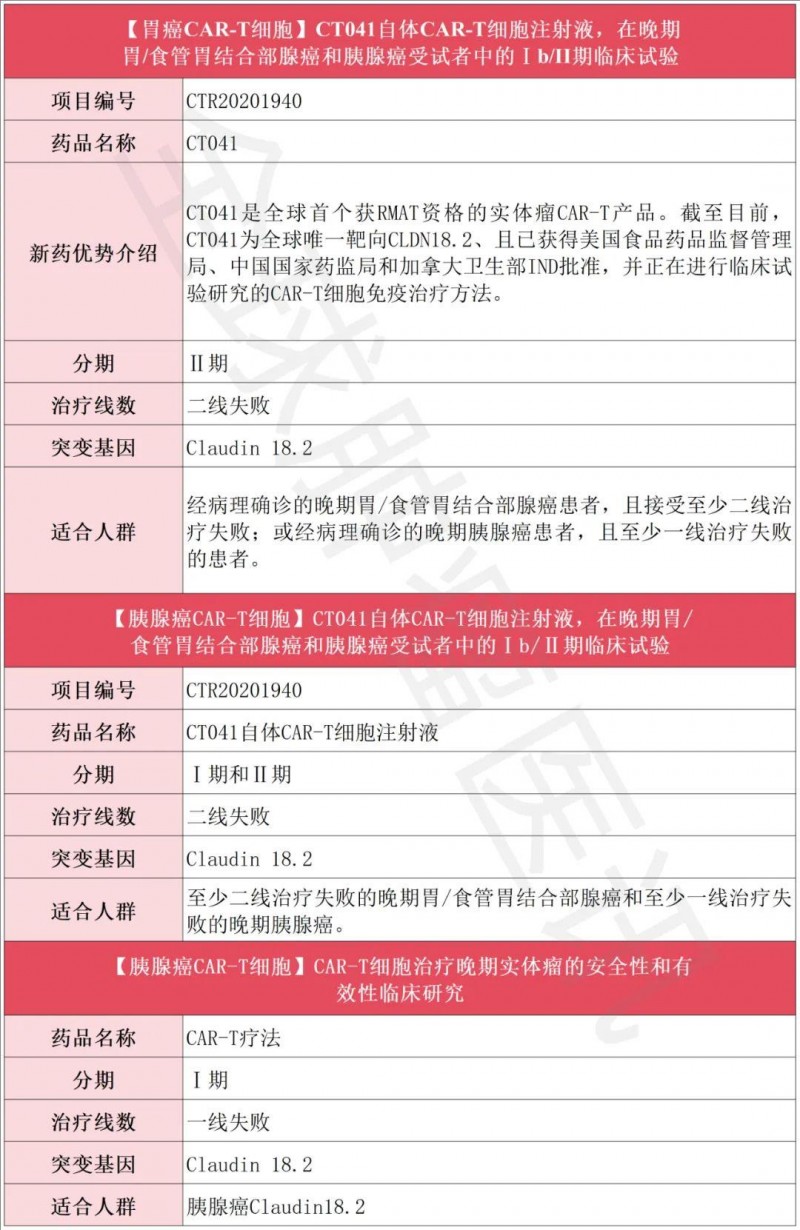
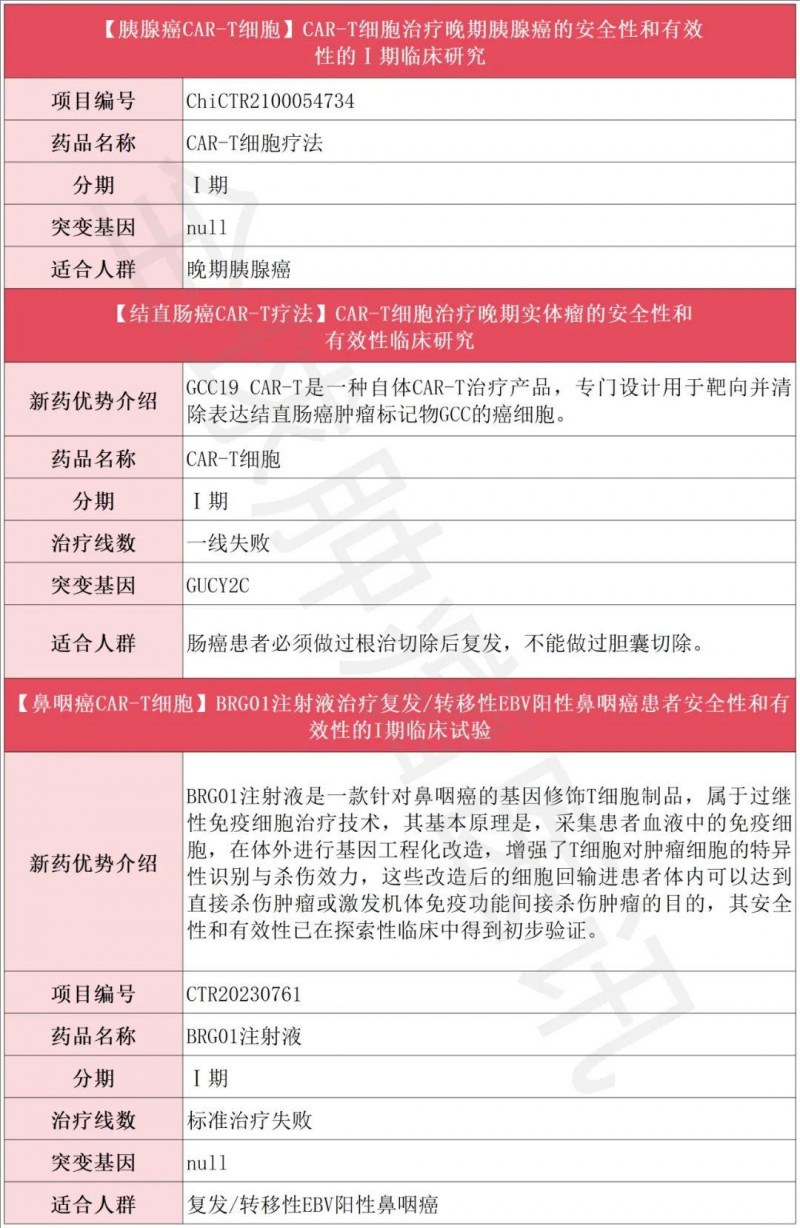
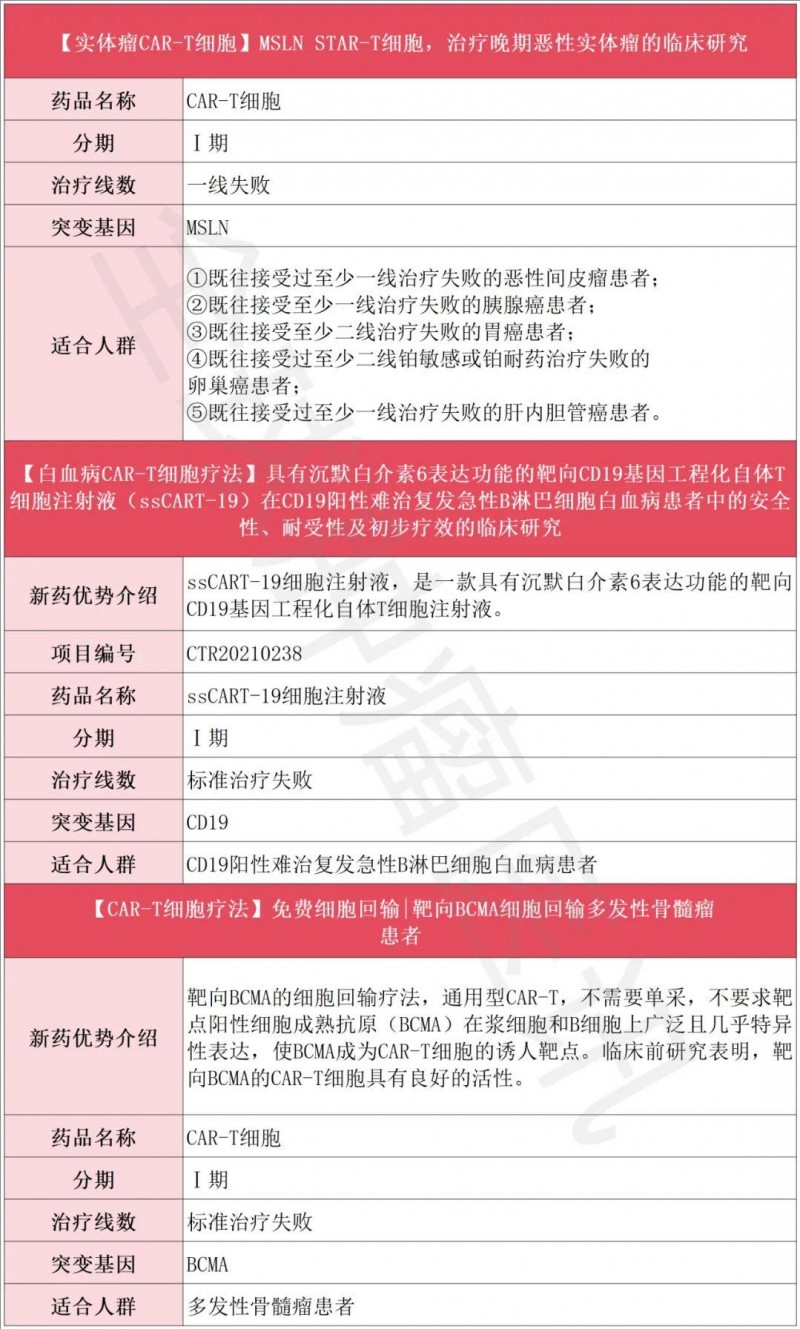
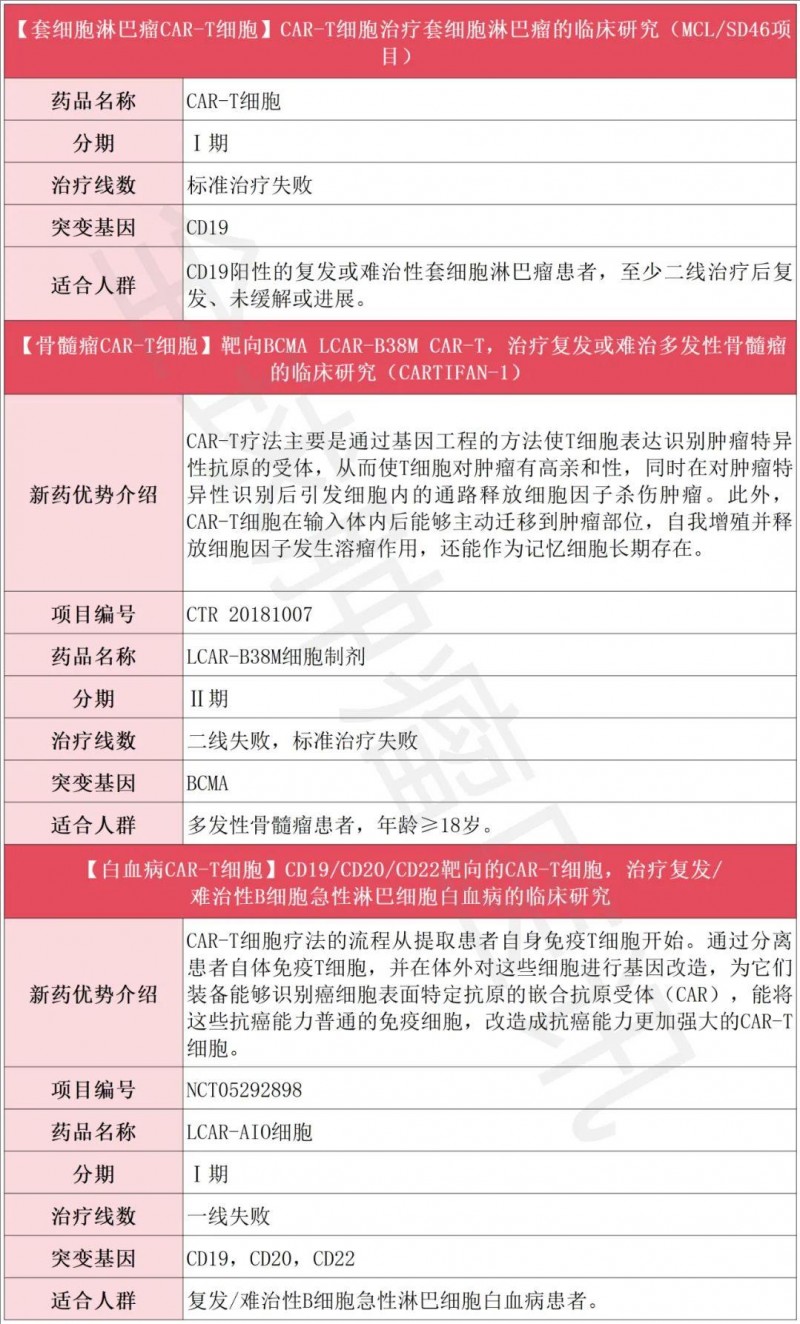
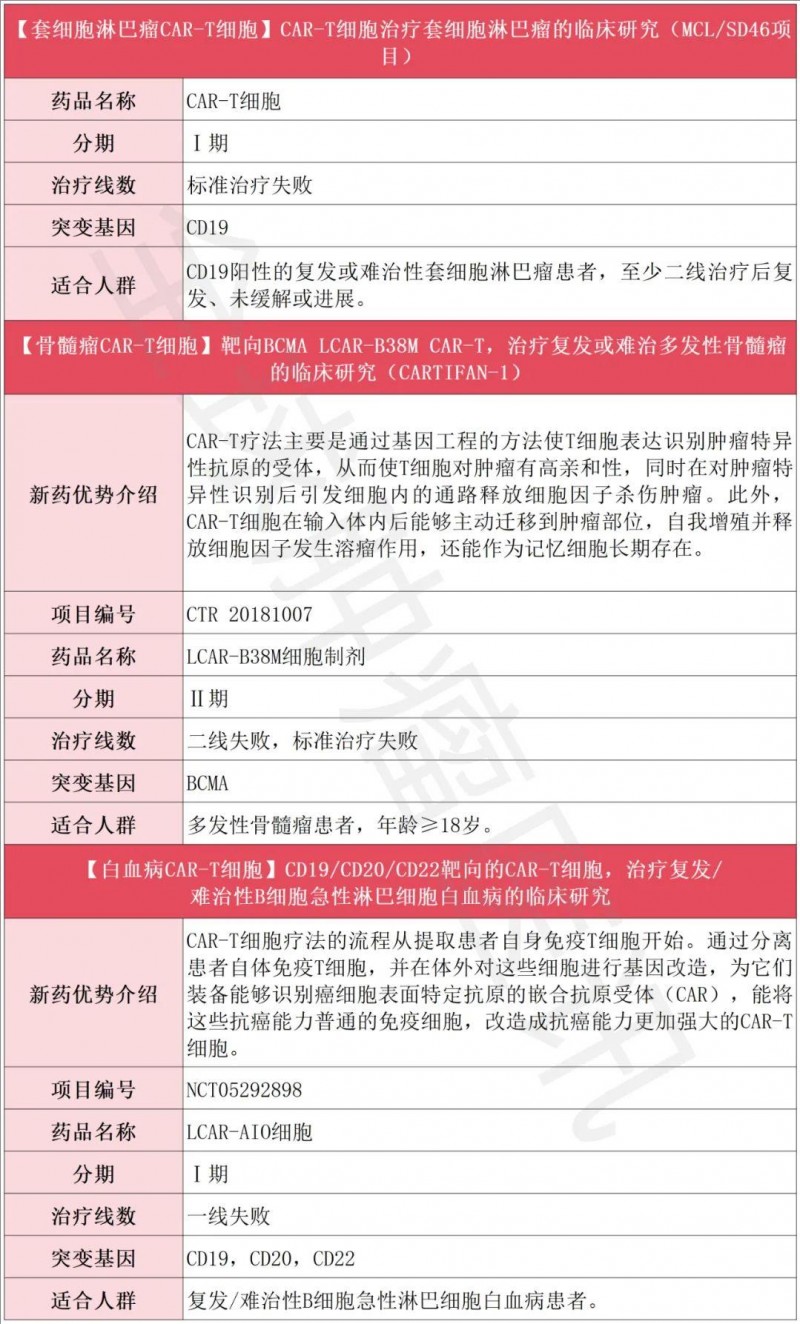
TCR-T获批产品+临床招募一览表
全球首款TCR-T产品——Afami-cel
1、Afami-cel
药物名称:Afami-cel(afamitrisgene autoleucel,TECELRA®)。
上市时间:2024年8月2日。
药物介绍:Afami-cel是一款针对MAGE-A4癌症抗原的自体TCR-T细胞疗法,2024年8月2日,获美国FDA批准用于成人不可切除或转移性滑膜肉瘤的治疗。它是首个获批上市的TCR-T疗法!也是十多年来首个针对滑膜肉瘤的新型治疗选择!本次获批是基于《柳叶刀》发表的2期临床研究的惊艳数据,近70%的患者在接受Afami-cel治疗后,生存期超过2年,这无疑是难治性肉瘤患者的巨大生存突破!
TCR-T临床招募一览表
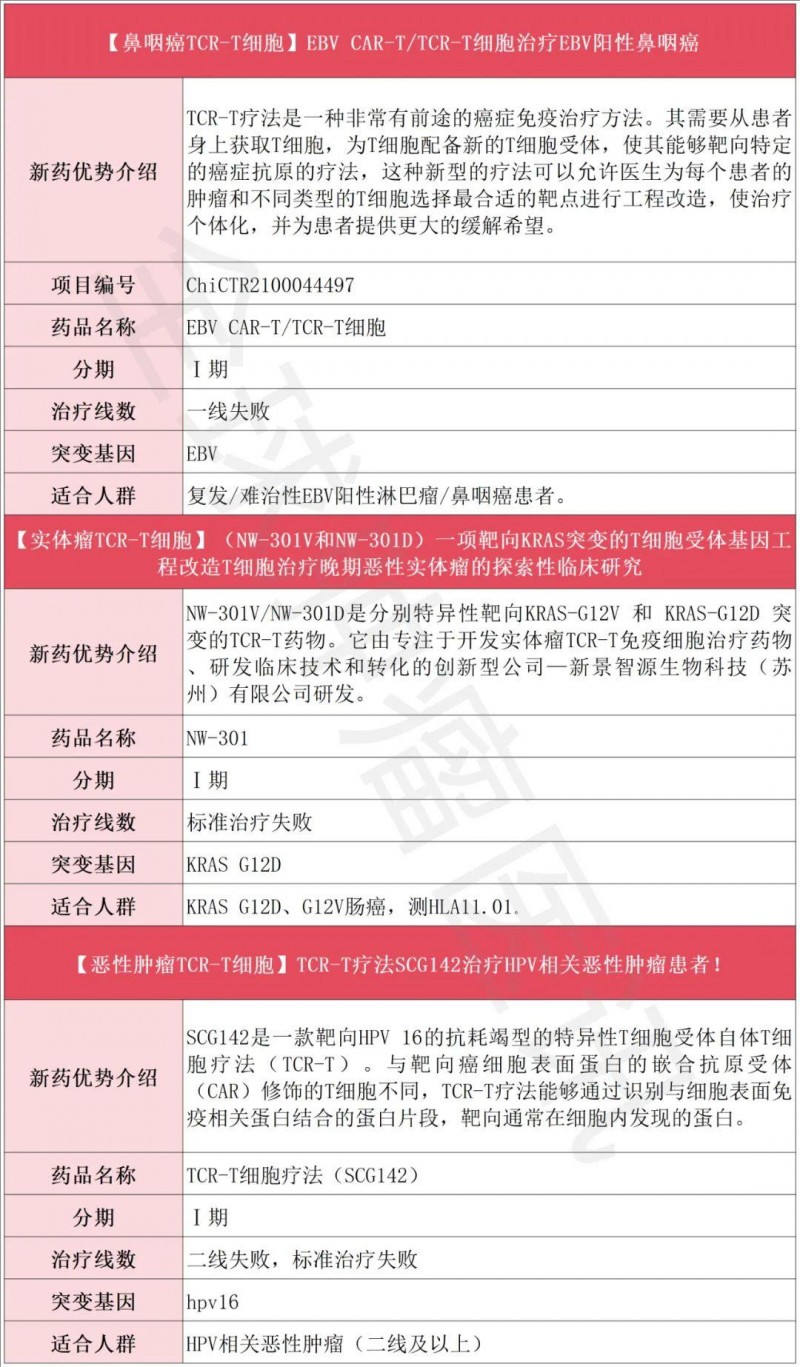
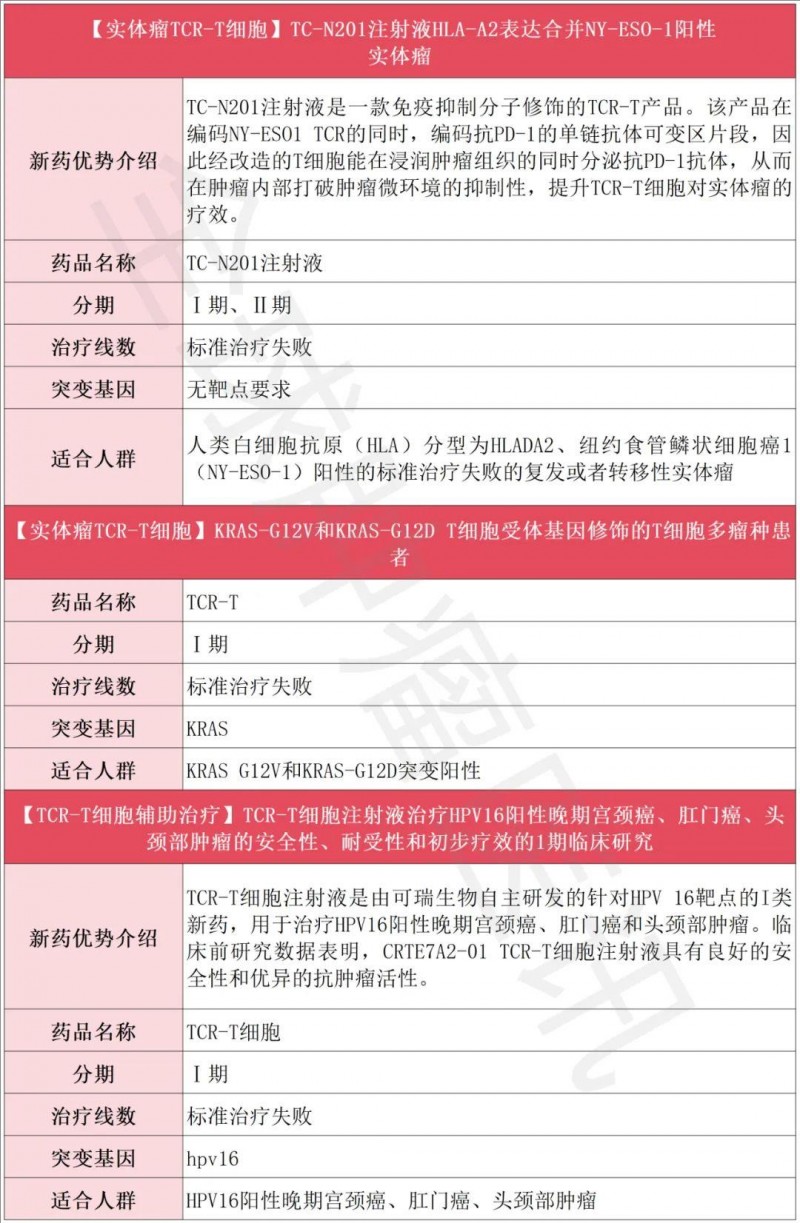
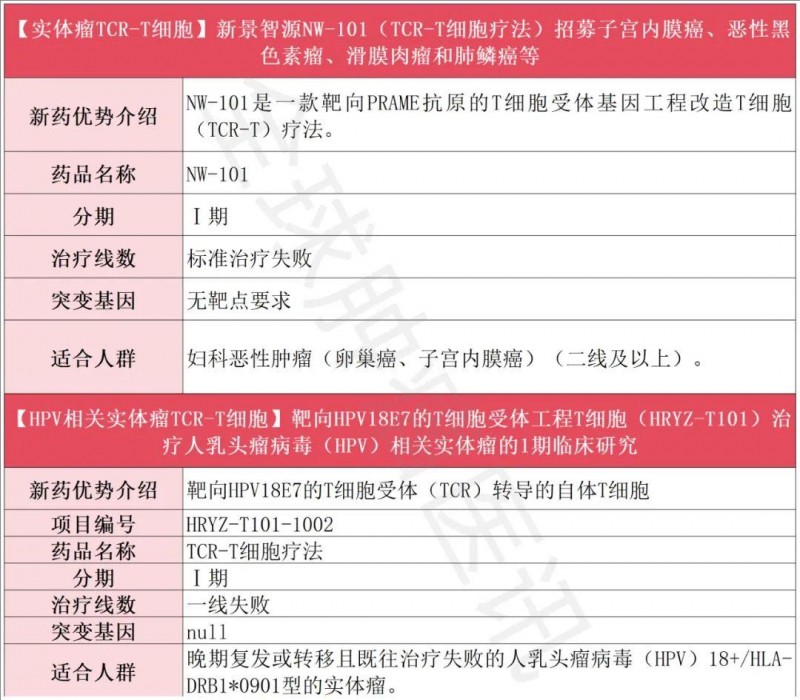
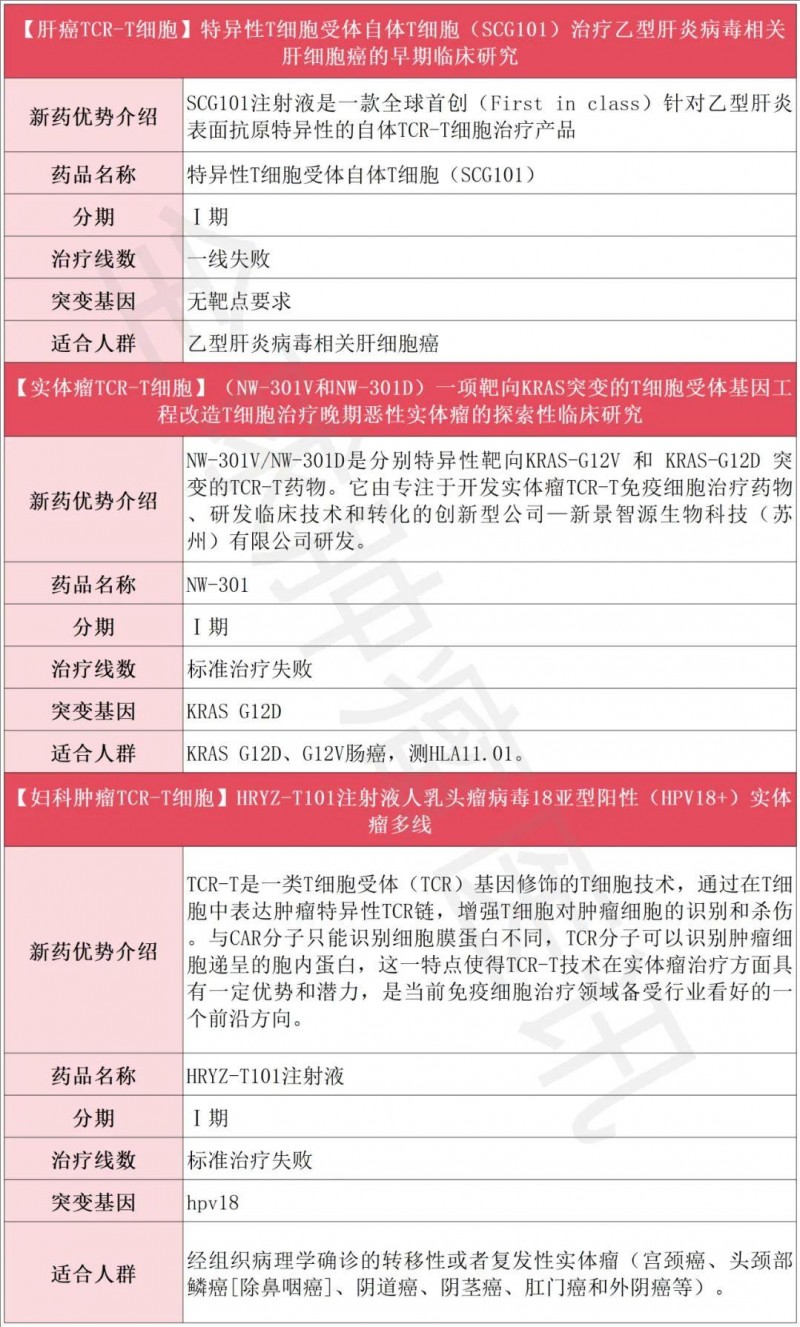
TIL细胞疗法获批产品+临床招募一览表
首款TIL疗法——Lifileucel
1、Lifileucel
药物名称:Lifileucel(LN-144,商品名Amtagvi)。
上市时间:2024年2月16日。
药物介绍:Lifileucel属于一款肿瘤浸润细胞疗法(TIL),2024年2月16日,获美国FDA批准,用于治疗既往接受过PD-1治疗的不可切除或转移性黑色素瘤。它是全球首款TIL细胞药物!同时也是目前唯一获得FDA批准的实体瘤TIL疗法!本次获批是基于2期临床试验结果,疾病控制率(DCR)达到惊人的77.8%!这意味着近80%的极晚期黑色素瘤患者,在Lifileucel治疗后,出现不同程度的肿瘤缩小或控制稳定!
TIL疗法临床招募一览表
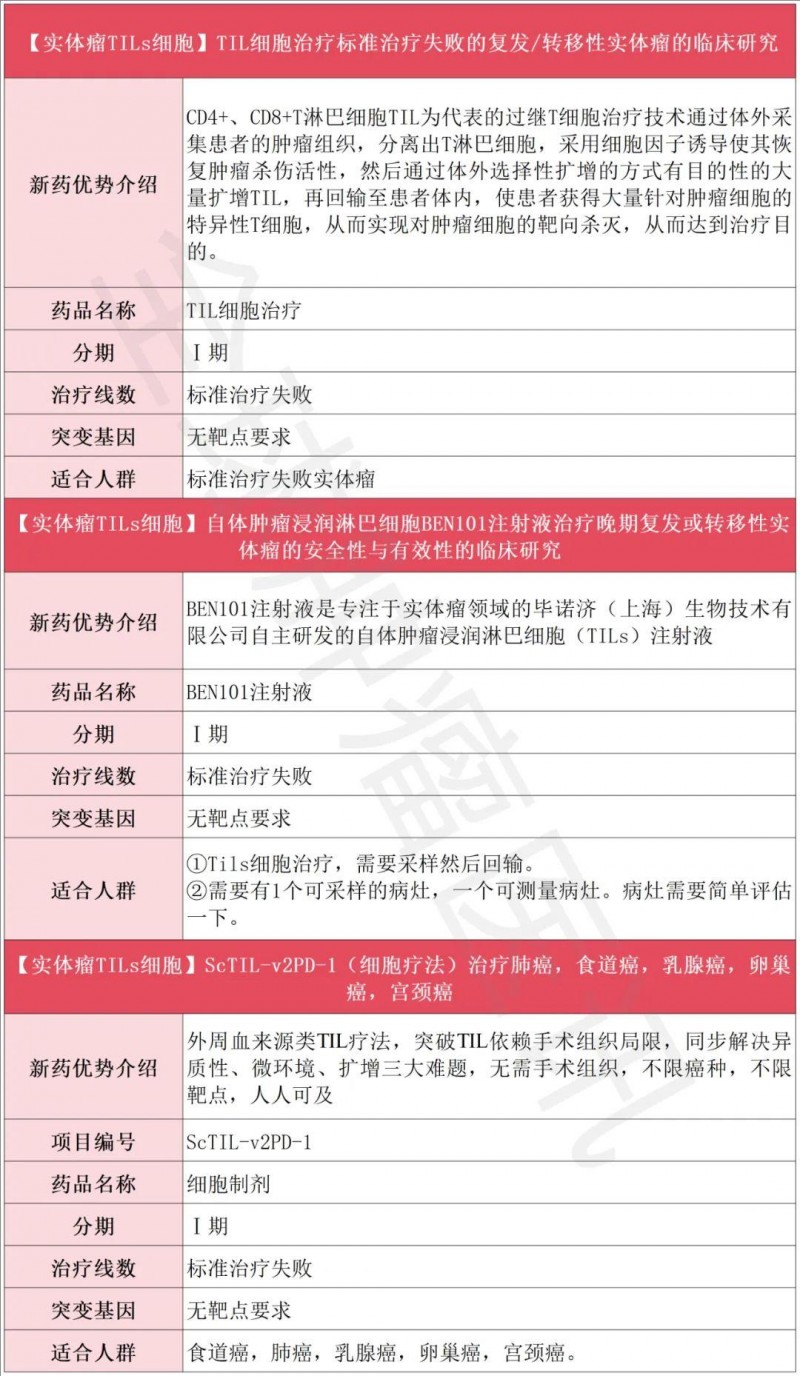
小编寄语
癌症治疗一直是困扰世界的难题,传统的手术、放化疗等抗癌方式,易出现复发或转移,因此迫切需要开发新型抗癌手段。随着医学技术的不断发展,癌症逐渐进入精准治疗的时代,以CAR-T、TCR-T、TIL细胞疗法为代表的免疫细胞疗法,主要通过调动人体的免疫细胞,精准识别并杀灭癌细胞,与此同时对正常细胞组织的损伤较小,颠覆了传统的抗癌模式!
值得欣慰的是,目前CAR-T、TCR-T和TIL这三种过继性T细胞疗法,都取得了突破性进展,相继有多款产品获批上市,为完全肿瘤患者带来了新的曙光!对目前治疗方案不满意,想寻求CAR-T、TCR-T、TIL疗法或其他国内外抗癌新技术帮助的患者,可先将近期病理报告治疗经历、出院小结、等资料,提交至医学部,进行初步评估或申请国内外抗癌专家会诊。
参考资料
[1]美国FDA官网
https://www.fda.gov/
[2]中国NMPA官网
https://www.nmpa.gov.cn/