370万天价的TILs细胞疗法到底是什么
癌症一直以来都是人类健康的巨大威胁,然而,随着医学科技的不断进步,一种名为TILs疗法的创新治疗方式正逐渐崭露头角,为癌症患者带来了新的希望。
一、TILs疗法的诞生与发展
TILs疗法的历史可以追溯到上世纪80年代末,由美国国家癌症研究所的Steven Rosenberg博士和团队首次提出并开展临床试验,经过多年的研究和探索,这一疗法在2024年取得了重大突破。
2024年2月16日,美国食品药品监督管理局(FDA)加速批准了全球首款TILs疗法——lifileucel(商品名:Amtagvi)上市,用于治疗接受过抗PD-1/PD-L1治疗后病情仍进展的晚期黑色素瘤患者,它的获批标志着T细胞疗法的一个重要里程碑,为实体瘤治疗开启了新纪元;但是这种疗法价格昂贵,定价为51.5万美元(约合370万元人民币),被标榜为“天价”,成为目前最昂贵的癌症免疫疗法!
二、TILs疗法的原理与优势
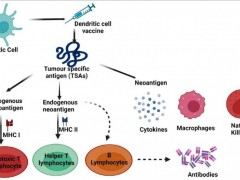
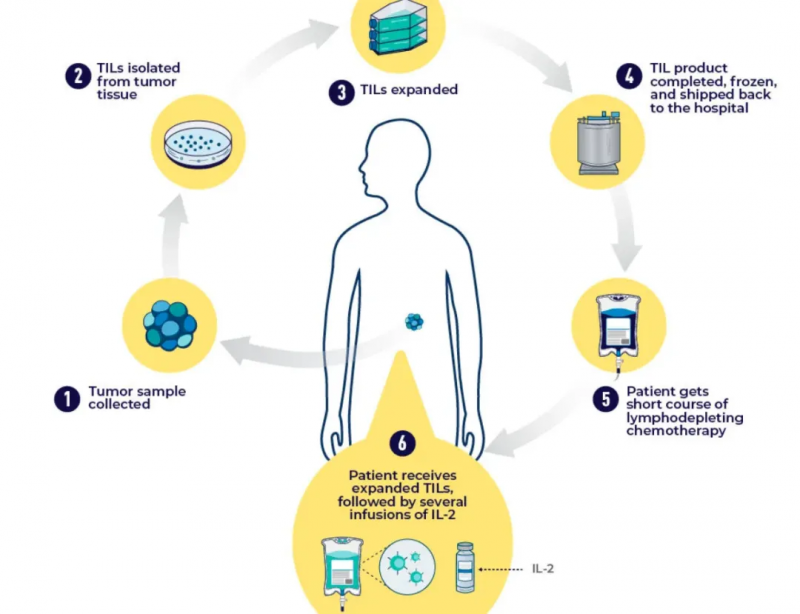
TILs疗法的核心在于从患者手术切除的肿瘤中提取出肿瘤浸润淋巴细胞(TILs),这些免疫细胞是一群存在于肿瘤组织内部的淋巴细胞,它们与肿瘤细胞长期交战,具备精准定位和杀伤肿瘤细胞的能力。
与CAR-T疗法不同,TILs疗法无需对免疫细胞进行基因工程改造,其细胞群本身就含有大量天然的、针对肿瘤特异性突变抗原的T细胞;在实验室中,将这些珍贵的免疫细胞进行培养扩增,可获得数十亿个战斗力增强的TILs细胞军团;当它们被重新输回患者体内后,会不断寻找并消灭癌细胞。
TILs疗法具有以下显著优势:
扩增至数十亿甚至上百亿的“活”细胞疗法:这些“活”的细胞能够持续起效,一旦体内再次出现癌细胞,它们便能迅速发起攻击。
高缓解率和长期效果:在C-144-01这个Ⅱ期临床试验中,平均经历过3线治疗方案的晚期黑色素瘤患者群体中,客观缓解率(ORR)达到了31.4%,疾病控制率(DCR)高达77.8%;特别值得关注的是,部分患者在接受治疗2年后,肿瘤持续缩小,最终达到完全缓解(CR);而且,缓解效果可长达10年之久,例如,一位全身扩散的晚期黑色素瘤患者,经过实验性的TILs疗法治疗后,肝脏、胰腺及皮下的40多个肿瘤全部消失,从2013年到2023年已无癌生活了10年!
“一针”消除肿瘤:类似于CAR-T疗法,TILs疗法是一种单次治疗,首先通过微创手术提取TILs细胞,然后在实验室培养和扩增,这一过程大约需22天,但整个流程可能耗时长达八周;治疗过程中,患者会接受化疗以清除自身免疫细胞,为新的TILs细胞腾出空间,回输后还会接受IL-2药物以进一步激活这些细胞。
三、TILs疗法在多种癌症中的应用进展
除了黑色素瘤,TILs疗法在其他多种类型的实体瘤上也展现出了良好的临床疗效:
宫颈癌:美国临床肿瘤学会(ASCO)年会上公布的数据显示,一项纳入27名标准治疗失败的宫颈癌晚期患者临床实验,接受TILs疗法后,疾病控制率为85%,客观缓解率为44%,完全缓解为11%。
肺癌:2022年5月的国外一项临床实验中,24名非小细胞肺癌患者接受PD-1耐药或者化疗失败后,进行TILs疗法一次,总体缓解率为21.4%,疾病控制率为64.3%,其中1位患者的肿瘤完全缓解,并实现无癌生存超2年。
乳腺癌:美国国家癌症研究院公布的TILs疗法对晚期乳腺癌的治疗效果显示,42位转移性乳腺癌患者中,67%出现了免疫应答,其中8位非常适合TILs疗法,最终6位接受了TILs疗法联合帕博利珠单抗,结果一半患者客观缓解,肿瘤明显缩小,其中一位患者肿瘤完全消失,目前已保持无癌状态五年。
此外,TILs疗法还在卵巢癌、头颈癌、肉瘤等多种癌症的临床实验中取得了不俗的进展,适应症广泛。
四、TILs疗法的挑战与应对
尽管TILs疗法前景广阔,但在实际应用中仍面临一些挑战:
细胞提取和扩增难度:从肿瘤组织中分离出具有特异性的T细胞操作难度较大,且部分晚期患者可能无法耐受手术,或者扩增过程中患者病情恶化而无法等到细胞回输。
免疫微环境影响疗效:如果分离出来的T细胞数量太少、抗癌活性差,病人也很难获益。
针对这些挑战,医学专家们正在努力研究解决方案,例如,一些企业致力于优化培养思路,模拟患者体内甚至肿瘤内部的环境,使细胞修复和扩增,以增强其适应能力,减少对外部因素的依赖。
五、国内TILs疗法的研究进展
我国在TILs疗法的研究方面也取得了积极成果,例如,上海君赛生物科技有限公司自主建立了DeepTILs®细胞扩增平台与NovaGMP®基因修饰平台,其研发的全球首款无需大剂量清淋、无需IL-2注射的天然TILs细胞新药GC101及全球首款非病毒载体基因修饰TILs细胞新药GC203,在治疗黑色素瘤、宫颈癌、子宫内膜癌、卵巢癌、肺癌、胰腺癌、脑胶质瘤等多个瘤种中展现出优异的安全性与临床疗效,其中7例晚期患者肿瘤被完全清除,获得CR疗效,且无瘤生存最久时间已近3年。
此外,沙砾生物的在研产品GT101是中国研发进展较快的TILs疗法,目前即将进入关键二期临床试验,预计于2025年底申报上市;其下一代在研产品GT201也已正式获得国家药品监督管理局的临床试验默示许可,成为国内首款进入注册临床试验的基因编辑型TILs药物。
西比曼生物科技的新型TILs疗法C-TILs051的临床试验申请也获得了FDA批准,适应症为PD-1抗体难治或复发的晚期非小细胞肺癌。
六、总结
TILs疗法的出现为癌症治疗带来了新的曙光,但仍需要更多的临床研究和实践来进一步验证其疗效和安全性,未来,随着技术的不断进步和研究的深入,我们有望看到TILs疗法在更多癌症类型中的应用,为更多患者带来福音。