今天医学圈儿会被这条新闻刷屏:FDA开启抗癌治疗新纪元——批准第一个基因疗法Kymriah上市!这是一项历史性的行动,使美国第一种基因治疗方法得以实现,为治疗癌症和其他严重和危及生命的疾病提供了新的途径!
诺华公司首席执行官约瑟夫·希门尼斯(Joseph Jimenez)表示:“五年前,我们开始与宾夕法尼亚大学合作,研究免疫细胞治疗癌症患者,我们非常自豪能成为癌症治疗历史时刻的一部分,并非常感谢我们的研究人员,合作者以及参与Kymriah临床计划的患者和家属。“作为对迫切需要新选择的儿童和年轻人的突破性免疫细胞治疗,Kymriah真正成为改善患者的结局和治疗癌症的方式。”
2012年,诺华公司和宾夕法尼亚大学(Penn)进行了全球合作,进一步研究,开发和商业化CAR-T细胞疗法,包括Kymriah,用于癌症的研究治疗。
费城儿童医院(CHOP)是首家调查Kymriah治疗领先单次试验的儿科患者的机构。
出色的临床数据
此次获得FDA批准是基于关键的开放标签,多中心,单臂II期ELIANA试验的结果,该试验是第一个全球儿童CAR-T细胞治疗登记试验,患者来自美国,欧盟,加拿大,澳大利亚和日本的25个中心。结果显示,63名罹患难治性或复发性B细胞前体ALL的儿童和青年在治疗的3个月内,CAR-T疗法带来的总体缓解率达到了83%。
关于ALL
ALL是淋巴细胞的一种癌症,一种参与身体免疫系统的白细胞。在ALL患者中,异常细胞在骨髓中聚集,阻止产生红细胞(携带氧气),其他类型的白细胞和血小板(凝血所需的部分血液)。因此,ALL患者可能出现贫血,更易发生感染和瘀伤或流血。
ALL占15岁以下儿童约25%的癌症诊断,是美国最常见的儿童癌症,尽管儿科/年轻成人B细胞ALL的结局总体改善,但复发或治疗难治的患者的有效治疗方案有限,预后差。患者经常进行多种治疗,包括化疗,放射治疗,靶向治疗或干细胞移植,但患者的五年生存率不到10%。迫切需要新的治疗方案。
关于Kymriah
美国FDA已经批准其CAR-T疗法Tisagenlecleucel(曾用名CTL019)上市。
商品名称: KYMRIAH
制造商: Novartis Pharmaceuticals Corporatio
适应症:用于治疗B细胞前体急性淋巴性白血病(ALL),且病情难治,或出现两次及以上复发的25岁以下患者。
Kymriah是一种创新的免疫细胞疗法,是一次性治疗。Kymriah在其嵌合抗原受体中使用4-1BB共刺激结构域来增强细胞的扩增和持久性。
制备流程:
Kymriah将在新泽西州Novartis Morris Plain使用每个患者使用自己的细胞制备。治疗需要先从个体患者的体内提取出T细胞,并在生产中心进行遗传改造。在那里,这些T细胞会被引入全新的嵌合抗原受体(CAR),使T细胞有能力直接靶向并杀伤带有CD19抗原的白血病细胞。当这些T细胞改造完成后,就会被输注回患者体内,进行治疗。
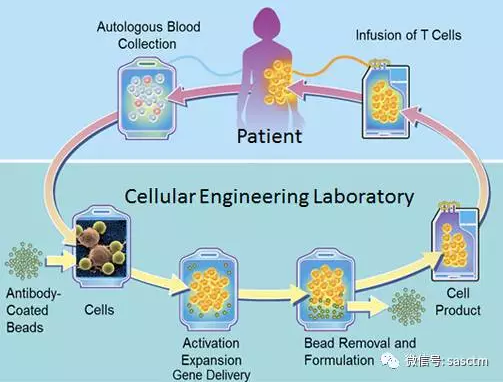
Kymriah除了T细胞以外,可能存在部分其他单核细胞,如NK细胞、B细胞等。Kymriah制剂处方如下:
|
成分 |
体积比例 |
|
Plasma-Lyte A |
31.25% |
|
5%葡萄糖/0.45%氯化钠 |
31.25% |
|
葡聚糖40(LMD)/5%葡萄糖 |
10% |
|
25%人血白蛋白 |
20% |
|
DMSO |
7.5%
|
Kymriah用药剂量:
-
50kg以下,0.2-5*106 个CAR阳性T细胞/kg体重,静脉注射;
-
50kg以上,0.1-2.5*108个CAR阳性T细胞/kg体重,静脉注射。
疗程包括首先进行淋巴细胞清除化疗:氟达拉滨(30mg/m2,静脉注射,每天一次,连续4天)联合环磷酰胺(500mg/m2,静脉注射,开始注射氟达拉滨时每天一次,连续2天)。淋巴细胞清除化疗完成后的2-14天内,静脉注射Kymriah。
Kymriah给药:给药前准备:
Kymriah解冻后可在室温(20-25℃)保存30分钟,因此需在患者治疗准备全部完成后确定解冻时间。
-
给药前准备好托丽珠单抗及必要急救设备;
-
给药前30-60分钟先给患者术前用药对乙酰氨基酚和苯海拉明或者其他H1抗组胺药物;
-
由于Kymriah是自体T细胞疗法,包装袋是病人专用的。给药前应确认袋子上患者信息;
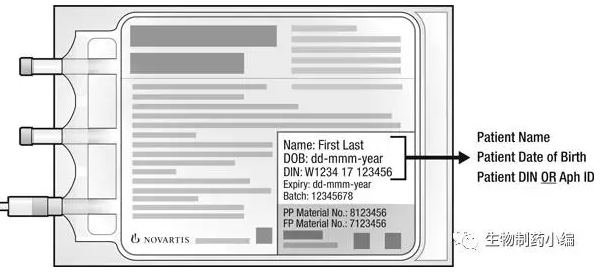
-
注射前要检查包装袋是否有破损,如有破损,不要给药。拨打诺华电话1-844-4KYMRIAH;
-
如包装袋有泄露,应转移到其他无菌袋中,避免污染;
-
37℃水浴或者干法解冻,知道无可见冰。切勿在37℃保存,一旦放置在室温条件(20-25℃),应在30分钟内给药;
-
肉眼观察解冻后有无细胞团,小的细胞团在手动轻摇后可消失,如果细胞团不消失,请勿给药。拨打诺华电话1-844-4KYMRIAH。
-
再次确认包装袋上患者信息;
-
10-20ml/min的速度静脉注射,患者年龄小可适当降低。包装袋体积在10-50ml
-生理盐水冲洗注射用管路;
-注射包装袋内全部液体;
-10-30ml生理盐水冲洗包装袋,确保尽可能多的细胞注射到患者体内。
|
CRS严重程度 |
应对措施 |
|
前驱症状: Low-grade的发热、疲劳、厌食
|
观察,避免感染,如中性粒细胞减少给予抗生素,对症治疗 |
|
明显的CRS: 高热、缺氧、轻微低血压
|
退烧药、给氧、静脉输液和/或低剂量升压药物(如有必要) |
|
危及生命的CRS: 使用升压药物血液动力学仍不稳定; 不断恶化的呼吸困难, 快速的临床恶化进展。 |
高剂量或多次升压药物、给氧、机械通气及其他必要措施。
给药托利珠单抗: 30kg以下,12mg/kg,超过一小时时间内静脉注射给药; 30kg以上,8mg/kg,超过一小时时间内静脉注射给药(最大剂量800mg) |
|
难治性CRS: 使用前述方法12-18小时内无改善或恶化 |
高剂量或多次升压药物、给氧、机械通气及其他必要措施。
2mg/kg甲泼尼龙起始剂量,随后2mg/kg每天给药,直到不再需要升压药物,迅速减量。
如果24小时内激素无响应,重复给药托利珠单抗: 30kg以下,12mg/kg,超过一小时时间内静脉注射给药; 30kg以上,8mg/kg,超过一小时时间内静脉注射给药(最大剂量800mg)。 如果第二次托利珠单抗24小时内不响应,考虑第三次给药托利珠单抗或寻求其他应对CRS的治疗措施。 |

▲2012年首个接受CAR-T治疗的儿童患者Emily,至今没有复发(图片来源:Washington Post)

▲首批接受CAR-T治疗的成人患者Bill,至今没有复发(图片来源:Time)

▲2年前接受CAR-T治疗的Layla(左),至今没有复发(图片来源:The Independent)

▲2年前接受CAR-T治疗的Kaitlyn,至今没有复发(图片来源:Time)
1、如何获得此基因疗法,什么医疗机构提供?
目前,仅有五家参与该基因治疗临床试验机构(癌症中心)提供此治疗方案。尚未在所有肿瘤治疗中心开展。预计年底前,诺华将在美国协助开设35家癌症治疗中心提供此疗法。
2、治疗费用是多少?
这是最尴尬的地方。已公布的治疗费用市场价是47.5万美元,约合320万元人民币!(相当于北京五环外100平米单元房价)。就是那句话,治疗越精准,费用也越天价!对于普通患者只好望药兴叹,但也不用灰心,目前,除了CAR-T,仍有许多FDA已批准的抗癌新疗法可以帮助癌症患者延长生存期,提高生活质量,详情可登录或登录全球肿瘤医生网咨询。
3、开创先例:若治疗有效收钱,无效免费
诺华制药希望与美国联邦医保机构就治疗费用探讨一种创新方案。采用该治疗方法一个月内,若患者癌症毫无改善,将免费用。这将开创先例:治疗收费依据治疗效果而确定。
4、该血液病属于罕见癌症
根据临床试验验证该基因治疗方法对25岁以下患者,包括儿童、青少年等患有B细胞急性淋巴细胞白血病有效。预测美国每年仅有600位患者适用于此种疗法,此疾病仍属罕见癌症之一。
5、明确疗效与致命不良反应同在
两年前,人们认为此类基因治疗方法仍属科幻。今天已经成为开启抗癌新纪元的“金钥匙”。在临床试验中,83%的血癌患者有明确疗效。这是目前任何抗癌方法所没有过的。
该治疗方法同样也伴随着致命风险和不良反应。FDA要求特别标注出细胞因子释放综合征等致命不良反应。机体会对体外处理过的免疫细胞产生特殊免疫反应。其他不良反应还包括高烧、神经系统损失等。