时间:2022-06-30 11:03 编辑:全球肿瘤医生网
肿瘤新药临床试验,不管什么癌种、不管有没有基因突变的广谱抗癌药临床试验招募正在进行中
相信很多患者都有过类似的担忧,如果正在使用的药物或方案耐药、没有其它治疗方案了,该怎么办?甚至有的时候,因为过于担忧耐药,患者会舍不得使用一款药物,明明有了突变也不接受靶向治疗,或者自行中断药物使用、自行延长用药间隔,希望通过这些方法来避免耐药(我们不建议这样做!)。
这一次呢,基因药物汇给大家讲几款,目前正在招募多线耐药患者的,不限癌种、不限突变的新药。
HDAC抑制剂
HDAC的全称是组蛋白脱乙酰酶。在癌细胞中,HDAC的过度表达,会使原本应当松弛的核小体变得紧密,导致部分基因的表达下调,例如一些肿瘤抑制基因。
通过药物抑制HDAC的作用,能够改善上述情况,并通过肿瘤抑制基因的功能,达到诱使癌细胞凋亡等目的。
这样的作用效果导致了,HDAC抑制剂成为了一种在部分血液系统肿瘤和实体瘤当中都有良好潜力的特殊靶向治疗药物,做到了更大意义上的不限癌种,且选择性较强、不良反应少。
目前临床上已经有5款HDAC抑制剂获批上市,适应症集中于T细胞淋巴瘤、骨髓瘤和乳腺癌。整体来说,疗效比较稳定。
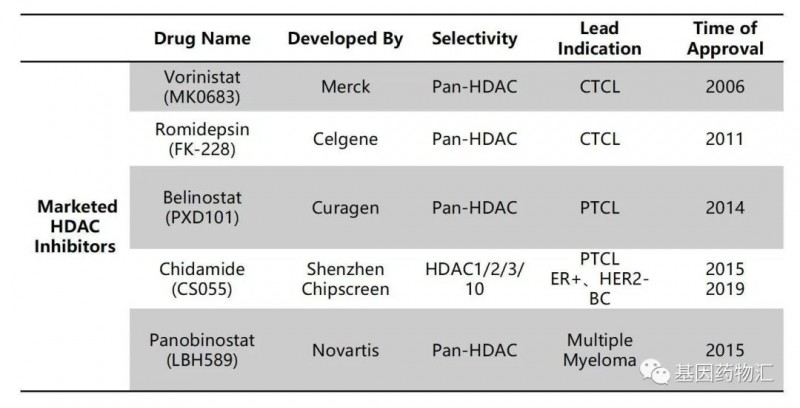
由于不同靶点的药物的偏向性(化疗药物也会有相似的偏向性),大部分HDAC抑制剂都容易产生心脏毒性。这也是新型药物进行结构优化的一大主题,正在招募的这款同靶点新药在这一方面做出了改进。
主要纳入标准:
1、年龄18岁,性别不限;
2、经组织学或细胞学确诊的,经标准治疗后进展或目前无标准治疗可用的,晚期/转移性恶性实体瘤或淋巴瘤;
3、根据RECIST v1.1标准,至少有1个可测量的靶病灶(用于评估疗效),需该病灶未经过放疗,淋巴瘤适用Lugano 2014标准;
4、ECOG评分0~1分;
5、当前预期生存期不少于12周。
具体纳入及排除标准大家可以咨询基因药物汇了解详情。
Fascin蛋白抑制剂
在癌细胞的生理过程当中,Fascin蛋白抑制剂对于癌细胞的迁移、侵袭和转移至关重要。不过呢,目前还没有针对这一靶标的药物获批上市,目前正在招募的这款DC05F01(NP-G2-044)最初由诺华研发,后被北京双鹤润创引进国内,是临床首款相关药物。
发表于《Cell Reports》杂志上的论文指出,在使用小鼠进行的临床前研究结果证实,小分子的Fascin蛋白抑制剂能够阻断肿瘤的侵袭和转移,提升小鼠的整体存活率。尤其是在与PD-1/PD-L1抑制剂联合应用时,效果非常显著。
从数据上来说,与接受免疫球蛋白G(IgG)治疗的对照组小鼠相比,单独接受DC05F01治疗的小鼠中位总生存期增加了约29%,使用免疫检查点抑制剂方案(PD-1单抗联合CTLA-4抑制剂)的小鼠增加了约27%;而使用DC05F01联合免疫检查点抑制剂方案的小鼠,中位总生存期增加了约105%!
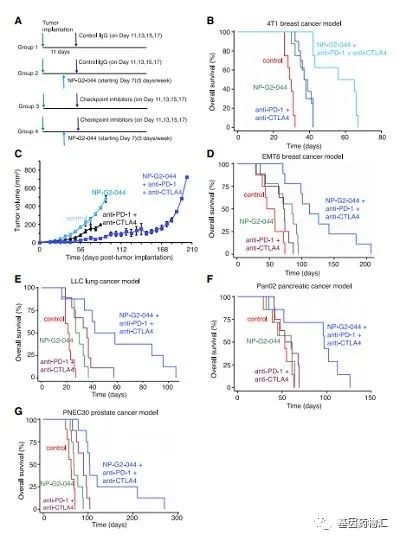
目前这款药物正在进行临床试验招募,主要纳入标准:
1、年龄18岁,中国男性或女性;
2、经组织学和/或细胞学确诊的局部晚期或转移性实体瘤患者,难治性或经标准治疗失败,或无标准治疗方案,或现阶段不适用标准治疗;
3 、根据RECIST v1.1标准,至少有1个可测量的靶病灶(用于评估疗效);
4、当前预期生存期不少于3个月;
具体纳入及排除标准大家可以咨询基因药物汇了解详情。
化疗药物
其实提到不限癌种不限突变,大家首先想到的可能是化疗药。和靶向药物相比,化疗药物的功能更简单直接,主要利用不同的细胞对于药物的敏感性不同来施予治疗。
举例来说,增殖旺盛的细胞对于化疗的敏感性高于增殖缓慢的细胞,幼稚细胞(分化程度较低的细胞)对化疗的敏感性高于成熟细胞(分化程度较高的细胞)。癌细胞的增殖旺盛,自身分化程度又比较低,这样的敏感性差异,成为了化疗发挥抗肿瘤效果的基础。
在实体瘤的治疗当中,有靶向药物可选的时候,化疗药物几乎不可能成为首选。但是仍然有大量的患者,由于没有必需的基因突变或指标,遗憾地与靶向治疗以及免疫治疗无缘。
此时,化疗的重要性就凸显了出来。
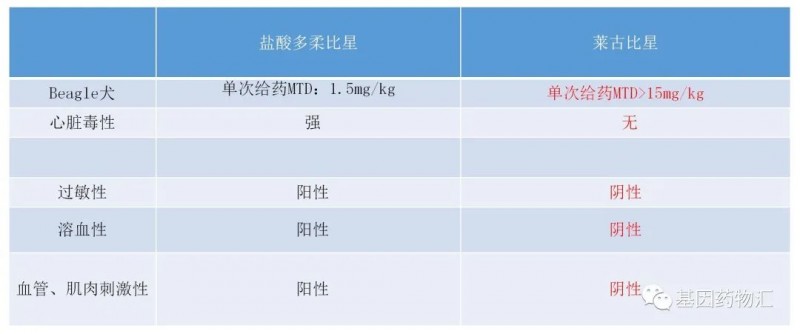
注射用莱古比星是一种新型的蒽环类化疗药物,将6-马来酰亚胺基团(EMC)与四肽氨基酸基团(ALA-ALA-ASN-LEU)连接,并与多柔比星相偶联。
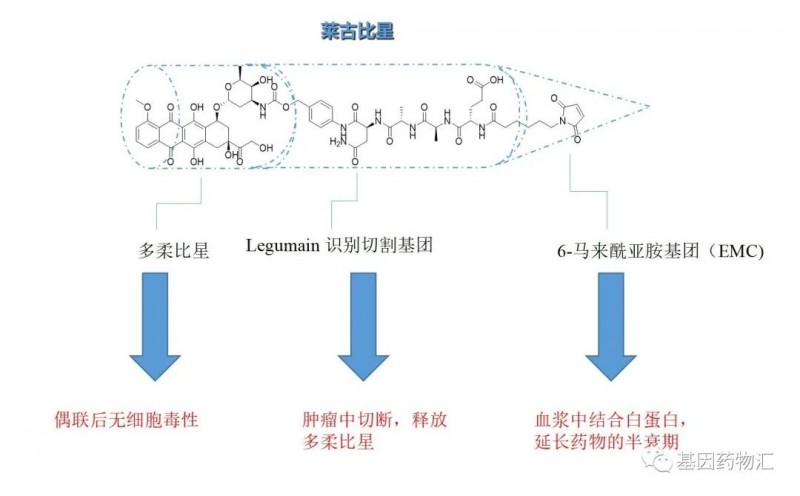
与多柔比星相比,莱古比星对于正常细胞的伤害更小,造成的心脏毒性、过敏性、溶血性及血管与肌肉刺激性更小,安全性更高。
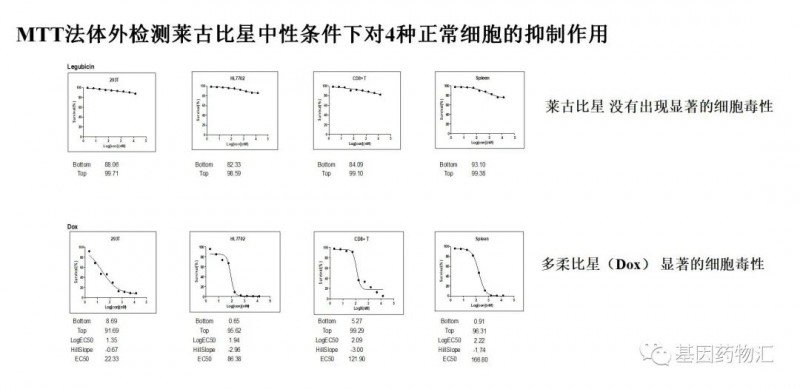
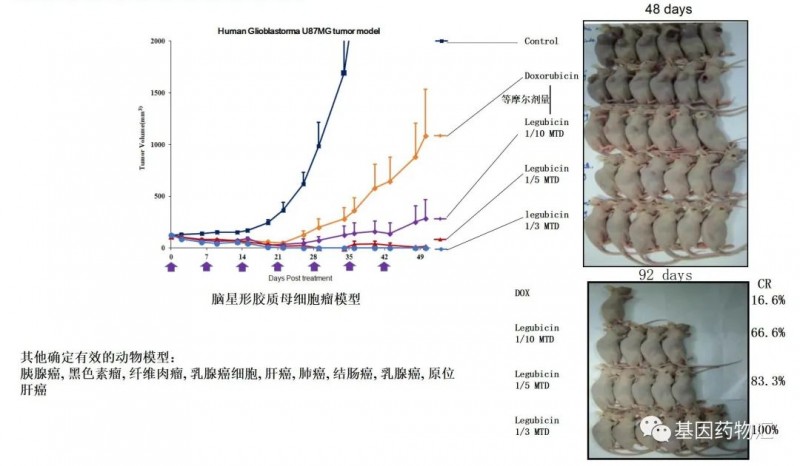
而在针对脑星星胶质母细胞瘤小鼠模型的研究中,采用莱古比星治疗,在有效药物等含量的情况下,莱古比星的疗效比多柔比星更强。
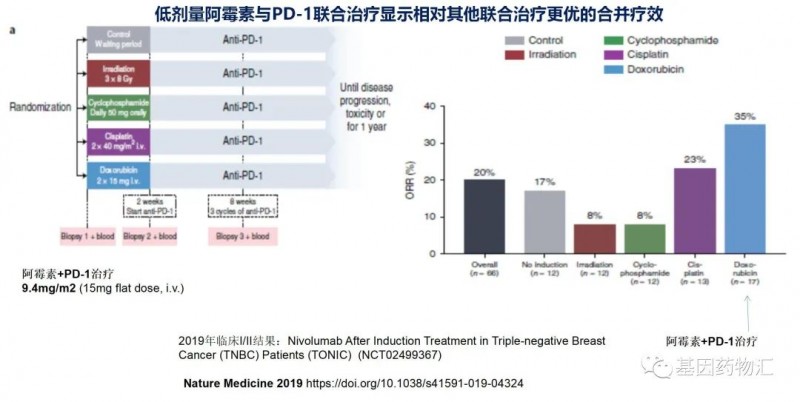
参考2019年发布的临床研究结果,多柔比星与PD-1联合应用,比其他联合用药方案的疗效更加显著,因此,研究者设计了莱古比星联合PD-1药物与多柔比星联合PD-1药物的疗效对比试验。
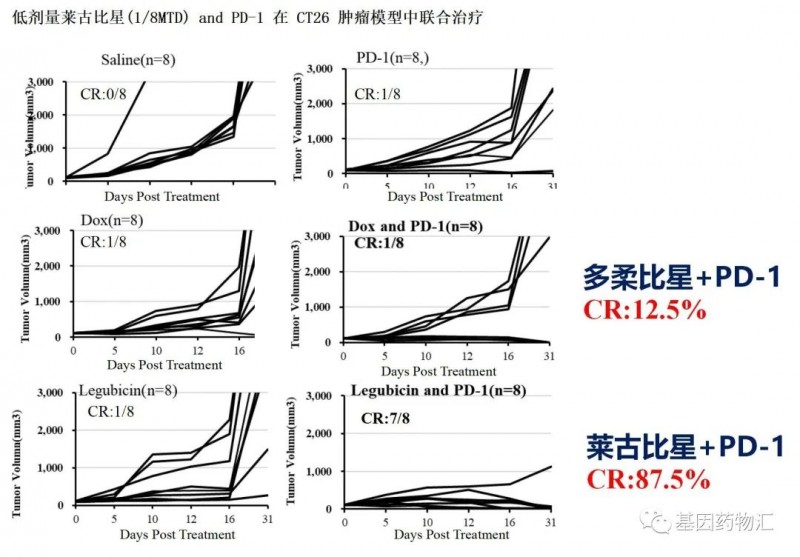
在小鼠模型中的研究结果显示,多柔比星+PD-1治疗的完全缓解率为12.5%,莱古比星+PD-1则是达到了87.5%。
也就是说,莱古比星联合治疗方案的完全缓解率达到了多柔比星的7倍!
目前,莱古比星已经被认定为化学1类新药,并获得了国家药品监督管理局的临床试验批准(2018L02645),允许进行临床试验。
主要纳入标准:
1、年龄18~75岁(含两端),男性或女性;
2、根据RECIST v1.1标准,至少有1个可测量的靶病灶(用于评估疗效);
3、ECOG评分0~1分;
4、当前预期生存期不少于3个月。
具体纳入及排除标准大家可以咨询基因药物汇了解详情。
本网站新闻资讯、文章、研究数据、治疗案例均来自于国内外医学论文,所涉及到的新药、新技术有可能还处于临床研究阶段,患者不能作为治疗疾病的依据。癌症治疗目前尚无治愈手段,患者需要在医生的指导下,在医院接受正规治疗或参加新药新技术临床试验。