非小细胞肺癌免疫治疗,非小细胞肺癌RET抑制剂Selpercatinib(LOXO-292)
RET融合存在于大约2%的非小细胞肺癌(NSCLC)、10-20%的乳头状甲状腺癌(PTC)和其他类型甲状腺癌、以及其他癌症(如结直肠癌)亚组中;RET点突变存在于大约60%的甲状腺髓样癌(MTC)中。
RET融合及RET点突变癌症主要依赖于RET激酶的激活来维持其增殖和存活,这种依赖性通常被称为“致癌基因成瘾”,使得这类肿瘤对靶向RET的小分子抑制剂高度敏感。
RET抑制剂-Selpercatinib(LOXO-292)
药物名称:Selpercatinib(LOXO-292)
生产厂家:礼来
优先审批时间:2020年1月30日
FDA预计裁定时间:第三季度
2020年1月30日,FDA授予selpercatinib,也就是大名鼎鼎的LOXO-292,适应症为晚期RET融合阳性非小细胞肺癌、RET突变型甲状腺髓样癌(MTC)和RET融合阳性甲状腺癌的患者。预计FDA将在2020年第三季度会对新药申请做出决定。这意味着,如果一切顺利,这款药物将于今年7-9月份获批上市!也意味着,有RET基因融合的患者将迎来全新的希望!
此次优先审批是基于I / II LIBRETTO-001试验的数据,在入组非小细胞肺癌队列有105例经过重度治疗的RET融合患者以及34例未经治疗的RET融合患者的疗效数据。
105经过重度治疗的患者,是指一半的患者至少接受过3个全身性抗肿瘤治疗方案,这些患者全都接受过含铂双药化疗,多数接受过免疫治疗以及其他RET靶向药治疗,可以说是临床上已经放弃的患者。
这款药究竟有多好呢
对于如此晚期的患者,总的客观缓解率(ORR)达到68%,疾病控制率达94%,并且对药物的平均反应持续时间也非常持久,长达20.3个月,中位无进展生存期为18.4个月。更值得一提的是,这款药物对于脑转的效果也非常惊人,客观缓解率高达91%,在11例可测量的脑转移患者中,有10例患者响应,包括2例完全缓解(CR)和8例部分缓解(PR)。
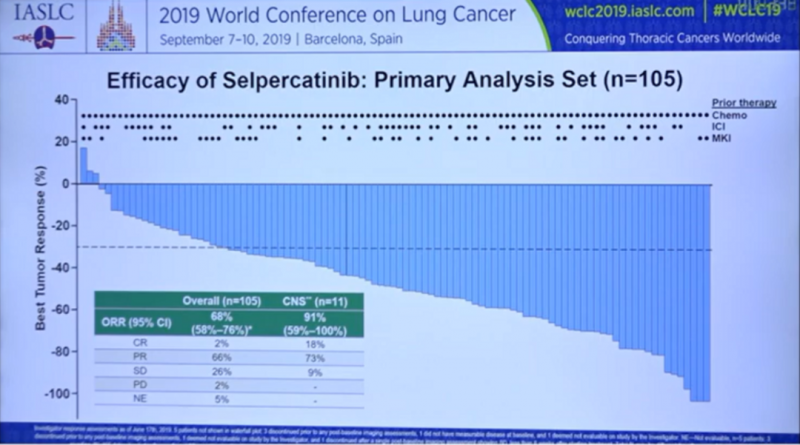
这张柱状图清晰的显示了LOXO-292卓越的临床效果。每个柱子代表一位患者,一共105位患者,柱子向下代表肿瘤缩小,可以看到大部分患者的肿瘤都得到了有效控制。
而在34例初治的的患者中,客观缓解率(ORR)高达85%,疾病控制率达到了94%。
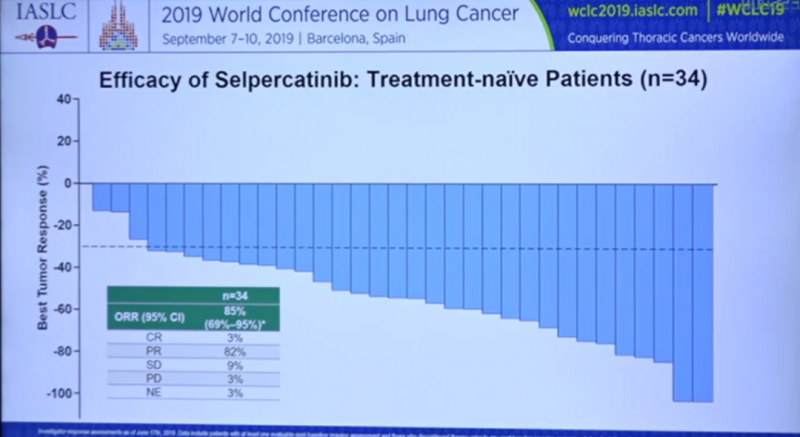
此外这款药物的安全性和耐受性良好,在入组LIBRETTO-001试验的531名患者中,有15%与治疗相关的不良事件(TRAE),包括腹泻,高血压等,大部分为1级和2级。有1.7%的患者因副作用停止了selpercatinib的治疗。
由此数据可以看出,LOXO-292疗效显著优于目前已获批的多靶点RET靶向药(如卡博替尼,凡德他尼等),与在研的RET靶向药BLU-667(Pralsetinib)相比疗效也不相伯仲,或将成为RET阳性患者的一线推荐方案。
Selpercatinib究竟是何方神圣
Selpercatinib是一种高度选择性和有效的口服研究药物,可用于治疗RET激酶异常突变的癌症患者。
RET激酶的基因组改变包括融合和点突变,这导致RET信号过度活跃从而让癌细胞生长不受控制。据统计,在非小细胞肺癌里面,大约1%-2%的患者有RET基因融合,在甲状腺髓样癌中超过60%的患者有RET基因突变,在乳头状甲状腺癌中10%的患者有RET基因融合。
所以大家做过多基因检测的患者,可以先看看是否有这个RET基因突变或者融合,一旦这款药物上市,大家就有新希望啦!(如果需要解读报告可以登录全球肿瘤医生网医学部)
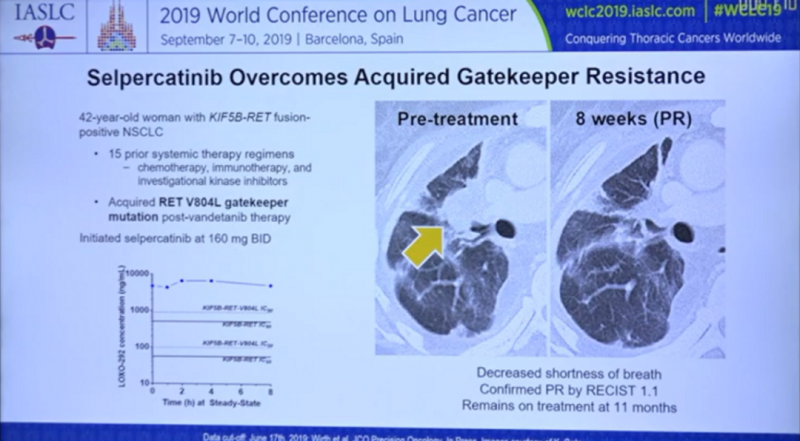
比如这位患者,先前经过化疗,免疫治疗和靶向治疗共15轮治疗,后来基因检测发现除KIF5B-RET融合外还出现RET V804L突变,接受Loxo-292治疗8周后疾病出现迅速缓解,截至案例发表时已持续治疗11个月仍在继续接受治疗。
Selpercatinib研究数据
此次RET融合靶向药申请是基于I/II期临床研究LIBRETTO-001的数据。该研究是评估一种RET抑制剂治疗RET改变癌症患者的最大规模临床研究。结果显示,Selpercatinib在先前未接受治疗(初治)和先前已接受过治疗(经治)的RET突变甲状腺髓样癌(MTC)患者中的ORR分别为59%和56%。之前公布的NSCLC队列数据显示,Selpercatinib在初治、经治RET融合阳性NSCLC患者中的ORR分别为85%、68%;此外,Selpercatinib是第一个显示出强大中枢神经系统(CNS)活性的RET靶向药,针对脑转移病灶,CNS ORR高达91%。
2019年12月,礼来启动了Selpercatinib的2项III期试验:LIBRETTO-431试验用于治疗初治RET融合阳性NSCLC患者,LIBRETTO-531用于治疗初治RET突变MTC患者。每项试验将招募400例患者。
Selpercatini审批历程
2020年1月29日:Selpercatinib新药申请获得FDA优先审查
2019年9月29日:Selpercatinib治疗RET突变甲状腺癌的阳性数据
2019年9月9日:Selpercatinib(LOXO-292)治疗经过大量预处理的RET融合阳性非小细胞肺癌中,客观应答率达到68%,并且持久耐用
2018年10月15日:Loxo肿瘤学宣布获得美国食品和药物管理局的突破性疗法称号,用于治疗RET融合阳性甲状腺癌的LOXO-292
2017年5月10日:Loxo肿瘤学宣布第一位患者的高度选择性RET抑制剂LOXO-292进入1期临床试验。







































 首页
首页 咨询
咨询 方舟新药
方舟新药 营养商城
营养商城