


三阴性乳腺癌治疗,多款重磅三阴乳腺癌药物,三阴性乳腺癌药物新药破除难治魔咒
三阴性乳腺癌是乳腺癌中最少见的类型,大概只占10%,但这是最让人头痛的一类。一方面,它激素受体或HER2都是阴性,因此内分泌治疗和HER2靶向治疗对它都无效,一般只能靠化疗药物,效果不理想。另一方面,它又恰巧是所有乳腺癌中最恶性的一种,发展迅速,容易转移和复发。40岁以下的乳腺癌患者只占患者总数的5%,但由于这类患者里三阴性比例最高,因此整体复发率比40岁以上患者要高。
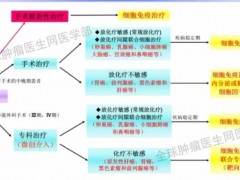
虽然三阴性乳腺癌(TNBC)目前仍然难以治疗,但是精准医学指导下的乳腺癌靶向和免疫治疗已成为大势所趋,一波巨浪已经改变了三阴性乳腺癌(TNBC)的治疗前景,基于三阴乳腺癌的分子分型,已经有获批的靶向和免疫治疗药物,还有一些临床试验结果非常振奋人心,其包括抗PD-L1抗体,PARP抑制剂和新型的抗体-偶联药物,可有效改善三阴乳腺癌患者的预后。
1、免疫检查点抑制剂
2019年3月8日,美国FDA加速批准罗氏旗下GENETECH公司研发的PD-L1单抗药物阿特珠单抗(Atezolizumab)联合化疗(白蛋白紫杉醇)一线治疗无法切除的局部晚期或转移性PD-L1阳性的三阴性乳腺癌(TNBC),这是三阴性乳腺癌首个获批的免疫疗法。
结果显示,阿特珠单抗显著降低疾病进展或死亡的风险40%,中位无进展生存期分别为7.2个月 vs. 5.5个月。在PD-L1阳性人群中,联合治疗组中位PFS为7.5个月,对照组为5个月,差异有显著性。在12.9个月的随访中,PD-L1阳性患者的中期分析显示,总生存显著延长(25.0个月vs. 15.5个月),结果令人鼓舞。
需要注意的是,PD-L1的状态在三阴乳腺癌患者的一线治疗决策中起着重要作用,在开始一线治疗之前一定要先进行PD-L1检测。如果大家不清楚检测流程可以直接登录医学部或扫描文末二维码在线咨询。
2、抗体偶联药物
目前,已有多种新的抗体-偶联药物(ADCs)被证实用于已经过多种治疗的转移性乳腺癌患者时仍能获得很高的缓解率。正在研发的这些抗体中,大部分以三阴性乳腺癌(TNBC)的细胞表面标志物TROP-2、LIV1、HER2和HER3作为靶点。
01.疾病控制率45%!Sacituzumab Govitecan成为三线主力
sacituzumab govitecan(IMMU-132),一种新型抗体 - 药物偶联物,由SN-38(伊立替康的活性代谢产物)与靶向滋养层抗原-2(Trop-2)的人源化单克隆抗体偶联组成。Trop-2在许多上皮癌中过度表达,并且与侵袭性肿瘤生长和低存活率相关。[它]在超过95%的三阴性乳腺癌中过度表达,因此它是一种在三阴乳腺癌中普遍表达的抗原,sacituzumab govitecan能够将更高剂量的化疗药物输送到癌细胞,同时帮助保护正常细胞。
2016年2月,FDA授予了IMMU-132突破性药物地位,因为它挑战了史上最难治的肿瘤之一—三阴乳腺癌,而且是多线治疗失败的患者,一半以上的患者接受过5种药物的治疗,临床控制率还达到惊人的70%。
在本次大会上,IMMU132更新了针对三阴乳腺癌的临床数据:作为三线治疗方案,IMMU132的无进展生存率高达33.3%,疾病控制率高达45%,74%的患者至少出现过一次肿瘤缩小!
临床设计:
108位三阴乳腺癌患者,59%的患者至少用过4种药物治疗之后失败。
结果显示:IMMU132的无进展生存率高达33.3%,疾病控制率高达45%,而且74%的患者至少在一次CT检测中发现了靶病灶缩小;一旦有效,IMMU132的疗效持续时间7.6个月;所有患者的无进展生存期5.5个月,中位生存期高达12.7个月。
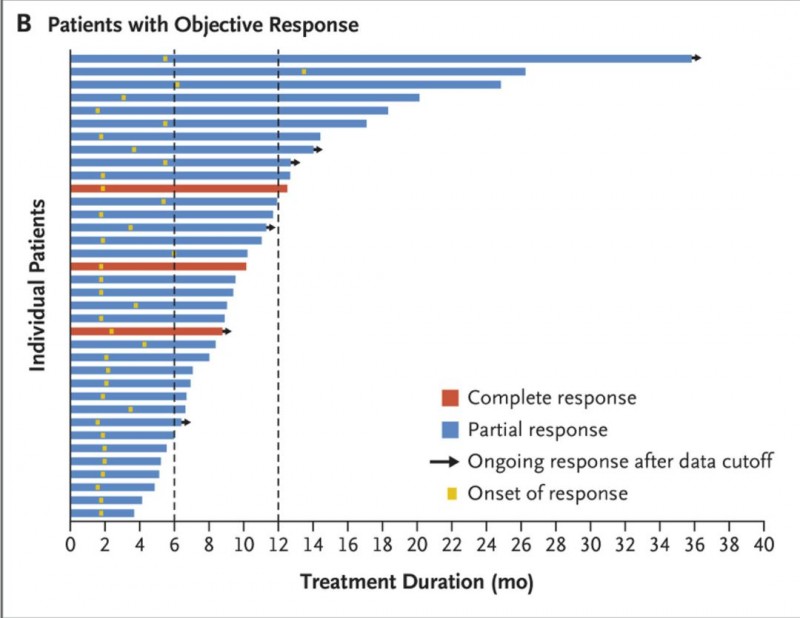
这张图从治疗开始到疾病进展的客观反应,截至数据发表时,有6名患者持续缓解。垂直虚线表示在6个月和12个月时的反应,这对于转移性三阴性乳腺癌患者有意义重大额改善。
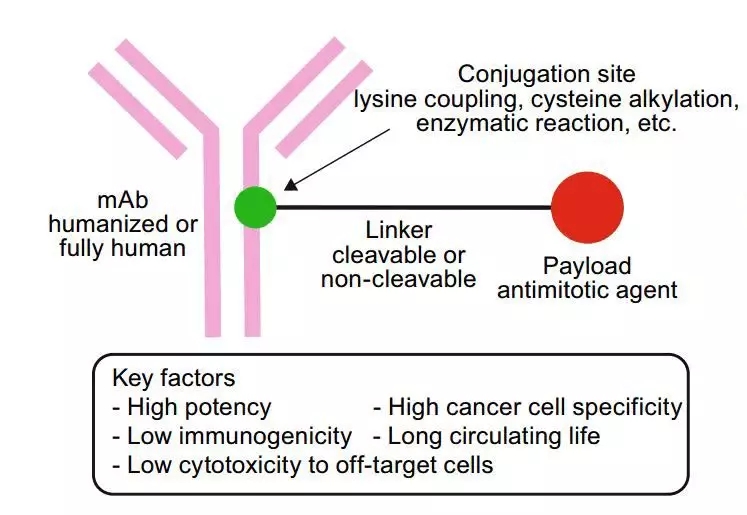
108例转移性三阴性乳腺癌患者的无进展生存期
不良反应:
3级以上副作用主要包括中性粒细胞减少(39%),白细胞减少(16%),贫血(14%)和腹泻(13%)。
基于这些研究结果,2019年12月,FDA接受了Sacituzumab govitecan的生物制剂许可证申请(BLA),同意将其用于转移性TNBC患者的治疗,且这些患者在接受本药物治疗前需要接受过至少2次转移性疾病的治疗。
针对Sacituzumab govitecan的第三阶段的ASCENT试验(NCT 02574455)目前也正在进行中,计划与现阶段转移性TNBC患者的常规治疗疗效进行比较。该试验已经招募到了529例患者,预计将于2020年报告结果(NCT 02574455)。目前,若Sacituzumab govitecan的BLA成功获得批准,那么该药物很有可能加速上市,我们共同期待这款药物能够早日进入临床改善三阴性乳腺癌患者的预后。
02.Ladiratuzumab Vedotin
Ladiratuzumab vedotin(SGN-LIV1A)是由一种抗LIV-1受体通过可由蛋白酶裂解的连接物连接到微管破坏剂组成的抗体偶联药物。
一项将Ladiratuzumab vedotin与PD-1抑制剂Pembrolizumab(Keytruda)联合治疗局部晚期或转移性TNBC患者的Ib/II期研究结果显示,对于26名患者进行评估,联合治疗的ORR为54%(95%CI,33.4%-73.4%)。值得一提的是,根据研究人员报告,超过90%的患者肿瘤大小有一定程度的下降。
目前Ladiratuzumab vedotin的联合用药效果仍然在Ⅰ/Ⅱ期研究中进行评估。这项研究计划纳入97例患者,预计完成日期为2020年5月(NCT 0310957)。我们期待它即将公布的新结果。
什么是抗体偶联药物
介绍到这里,很多并有可能还不知道什么是抗体偶联药物,在这里给大家科普下,抗体偶联药物(Antibody–drug conjugates (ADCs))可以定义为药物前体,抗体能够识别表达肿瘤抗原的靶点,并通过连接子与细胞毒素的“弹头”偶联形成针对肿瘤细胞的靶向递送系统,通俗的说,就是一支箭后面带了两个重磅炸弹,箭头瞄准靶标,炸弹炸毁靶标。在理想状态下,该药物前体在系统给药时不具有毒性,而当ADC药物中的抗体与表达肿瘤抗原的靶细胞结合、整个ADC药物被肿瘤细胞内吞后,小分子细胞毒素组分将以高效活性形式被足量释放,从而完成对肿瘤细胞的杀伤。
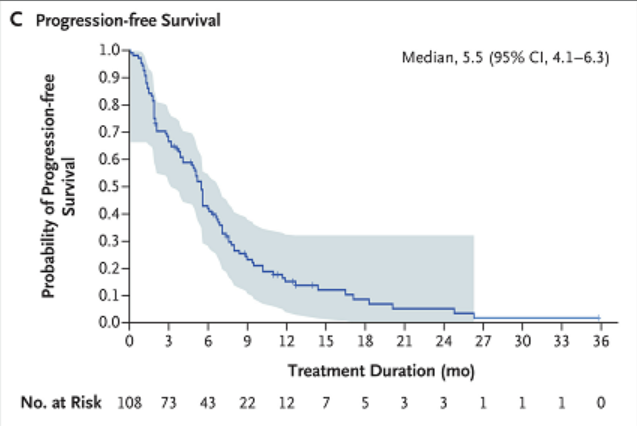
图1. 抗体偶联药物结构模式
那么其实可想而知,一个理想的ADC药物需要四个部分的完美结合:
·抗体(靶点)的选择:针对肿瘤特异(相关)性抗原,较高的表达水平,良好的内吞效率、良好的抗原亲和力、无免疫原性、药物可及性;·连接臂的选择:血液循环中保持稳定,在细胞内快速解体,高效释放毒物;·连接方式:定点偶联,产生均一的抗体偶联物;·毒素分子:一般要求毒素毒性足够强,达到单使用使IC50<1nmol;足够的水溶性及血清中的稳定性;毒物的作用靶点位于细胞内。
3、PARP抑制剂
大约20%·25%的三阴性乳腺癌患者存在胚系BRCA突变,这部分患者可能会获益于PARP抑制剂。OlympiAD和EMBRACA试验
OlympiAD和EMBRACA试验
2018年1月,FDA批准olaparib(奥拉帕尼 Lynparza)用于治疗转移性BRCA基因突变型HER2阴性乳腺癌。如果接受过内分泌治疗或不适合进行内分泌治疗,那么BRCA 阳性患者可考虑进行olaparib治疗。
在2018年10月,FDA批准了talazoparib(他拉唑帕尼Talzenna)用于有害或疑似有害生殖系BRCA突变,HER2阴性局部晚期或转移的患者乳腺癌。
Veliparib和BROCADE3试验
在BROCADE3(NCT02163694)中,将509例先前治疗过的转移性三阴性乳腺癌的BRCA阳性患者随机分配为2:1,接受veliparib加卡铂/紫杉醇或安慰剂加卡铂/紫杉醇。结果显示:veliparib组的PFS中位数为19.3个月,而安慰剂组为13.5个月。在3年时,veliparib组的PFS为26%,而安慰剂组为11%。
因此,对于BRAC突变HER2阴性的进展期三阴性乳腺癌患者,接受veliparib更能获益。
4、新辅助治疗
2020年2月27日《新英格兰医学杂志》发表的一项研究显示,针对三阴性乳腺癌患者,采用免疫疗法可以大大降低疾病复发的风险。
这项代号为KEYNOTE-522的国际试验招募了来自21个国家181个医学中心,1174名II期和III期三阴性乳腺癌患者,2/3的患者接受了 的化学疗法联合免疫治疗药物pembrolizumab(派姆单抗,keytruda),以在手术前缩小肿瘤。1/3的患者仅接受了化学疗法加安慰剂。手术后,患者继续接受单独的免疫疗法或安慰剂。
结果显示:
选取第一批602例患者作为研究对象,pembrolizumab组(401例)和安慰剂组(201例)的病理完全缓解率分别为64.8% vs 51.2%。即使是PD-L1表达的亚组,pembrolizumab组仍旧优于安慰剂组。
第二次中期分析首次进行无事件生存评估,中位随访15.5个月,两组入组患者均未达到中位无事件生存。
pembrolizumab组784例患者中有58例(7.4%)发生无事件生存事件,而安慰剂组390例患者中有46例(1.8%)发生无事件生存事件。在18个月时,pembrolizumab组的无事件生存率为91.3%,而安慰剂组为85.3%。
在新辅助治疗阶段,pembrolizumab组中76.8%的患者发生与治疗相关的≥3级不良事件,而安慰剂组中发生不良事件的比例为72.2%。与治疗相关的严重不良事件分别为32.5%和19.5%。
5、破除难治魔咒,三阴乳腺癌迎来全新生存希望
当前研究发现这些抗体药物结合物的无进展生存率为30%到40%,能否将其提高到50%、60%、70%、80%,并进一步改善转移性乳腺癌患者的预后,是全球科学家正在研发的重点,相信在不久的将来,免疫,靶向及新型抗体偶联药物在晚期三阴乳腺癌患者中应用价值将会更加清晰,或将重新定义并规划乳腺癌的治疗格局,为中国乳腺癌患者提供更多治疗选择。
2. 备注【癌种】申请方舟援助计划


患者咨询电话:400-666-7998

全球肿瘤医生网提醒患者:国内细胞免疫治疗技术,包括cart细胞,树突细胞疫苗,NK细胞
TILs细胞,TCR t细胞治疗癌症疫苗等技术均处于临床试验阶段,未获准在医院正式使用。国内患者可以参加正规临床试验,在医生的监管下使用,全球肿瘤医生网不推荐患者贸然尝试任何医疗机构和研发机构的收费治疗。
本网站新闻资讯、文章、研究数据、治疗案例均来自于国内外医学论文,所涉及到的新药、新技术有可能还处于临床研究阶段,患者不能作为治疗疾病的依据。癌症治疗目前尚无治愈手段,患者需要在医生的指导下,在医院接受正规治疗或参加新药新技术临床试验。

-

-
肿瘤电场疗法——被FDA批准治疗复发性胶质母细胞瘤等
目前电场疗法已被FDA批准用于治疗复发性胶质母细胞瘤、新诊断的胶质母细胞瘤以及恶性胸膜间皮瘤,并且在目前在六大实体肿瘤包括非小细胞肺癌 详细»
-

-
临床试验中心——每一个新药都是一份希望
提供癌症临床试验招募信息、抗肿瘤新药受试者招募信息。 详细»
-
-
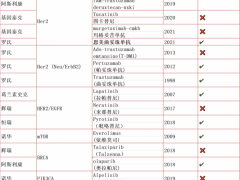
乳腺癌新药,2023年中美两国获批上市的乳腺癌靶向和免疫治疗药物有哪些
仅2023年一年,就有8款乳腺癌明星药物在中美两国分别获批上市(美国上市4款、中国上市4款),这无疑为乳腺癌,尤其是晚期耐药的患者,带来了新的希望和选择! 详细»
-
-
乳腺癌预防复发,美国启动癌症疫苗联合杀手T细胞的临床实试验
多款能够预防乳腺癌复发的癌症疫苗横空出世! 详细»
-

-
4类三阴性乳腺癌新药为患者带来长期生存
随着医学技术的发展,越来越多的新药、新技术在这个适应症上展现出了独特的治疗效果。 详细»
-

-
乳腺癌心理问题及护理措施
乳腺癌患者们承担的心理压力,远远比我们所想象中的要更大。 详细»
-

-
两款乳腺癌新药T-DXd和Elacestrant即将分别在中美两国上市
近年来对于治疗乳腺癌的新药国内外研发火热,给乳腺癌的治疗提供更精准的方案。 详细»
-

-
直播预告|2023年2月10日北京大学肿瘤医院乳腺肿瘤内科主任医师-邸立军教授:2022-2023年度乳腺癌靶向免疫治疗盘点及展望
2023年2月10日,全球肿瘤医生网特别邀请国内知名乳腺癌专家,北京大学肿瘤医院乳腺肿瘤内科主任医师-邸立军教授为大家详细解读2022-2023年度乳腺癌靶向免疫治疗盘点及展望。 详细»
-
-
2022-2023年乳腺癌抗癌白皮书,截止到2022年底获批上市的乳腺癌靶向和免疫治疗药物有哪些,2023年知道期待的乳腺癌新药新技术有哪
根据您的情况,全球肿瘤医生网生成您的2022年终乳腺癌新药报告和2023年最新进展,无论您处在胃癌治疗的哪个阶段,这份报告都将给您带来全新的生存机遇! 详细»
-

-
乳腺癌的早期症状和前兆有哪些
大多数癌症在早期都没有明显的临床症状,乳腺癌也是,很多患者发现自己患病往往是体检或者筛查发现的。 详细»































 首页
首页 咨询
咨询 方舟新药
方舟新药 营养商城
营养商城