2020年晚期肺癌治疗美国新方法晚期患者也能活过5年
肺癌在中国不论是发病率还是死亡率,排名都是第一,一旦被确诊得了晚期肺癌,大家往往认为被判了死刑,无药可救了。在2020年,非小细胞肺癌新药的进展和获批都呈现井喷状态,特别是靶向药和免疫治疗领域产生了范式转变,每一项成功的数据都为晚期癌症患者的生存带来了更多的选择和希望。
肺癌的靶向治疗-新靶点,新药物,新希望
与化疗相比,靶向治疗让晚期患者的无进展生存期显着增加。此前对于常见突变靶点EGFR,ALK,ROS1和BRAF突变并接受靶向治疗的患者,反应率约为50%至80%,总体存活时间对比化疗增加到18个月和38.6之间,而在初次靶向治疗耐药之后继续使用二代三代或者是免疫治疗,仍然能为生命继续续航。近两年,肺癌领域涌现出了众多新兴靶点,比如RET,MET,NTRK等,2020年,针对这些靶点上市的新药又给晚期患者燃起了新的希望。
FDA目前批准的肺癌靶向药

1、RET--首款获批上市的靶向药Selpercatinib和十五年幸存者
在肺癌的常见靶点中,大家对EGFR,ALK,KRAS,ROS1这些基因比较熟悉,而RET基因在肺癌中仅有1%-2%的患者存在RET基因融合,多为与KIF5B基因的融合,也就是说RET基因和KIF5B基因融合在一起,形成了一个新的基因,这种基因的出现会让癌细胞不受控制的恶性增值。
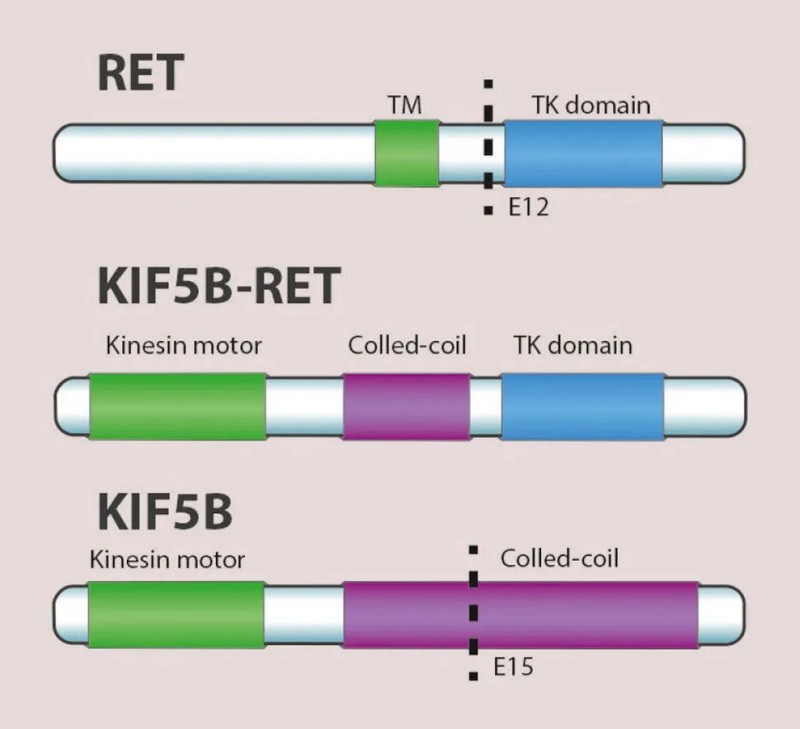
而Selpercatinib是一种高度选择性和有效的口服研究药物,专门针对于RET激酶异常突变的癌症患者。
这款药物之所以被誉为传奇抗癌药,是因为这款药物的无进展生存率超高,而且是对既往接受过铂类化疗和PD-1治疗后进展的非常晚期的患者,临床数据显示对于105例经过至少三种全身性治疗的晚期患者,总的客观缓解率(ORR)还能达到64%,其中81%的患者持续应答≥6个月。
Selpercatinib治疗案例
比如,梅利莎(Melissa Crouse)退休前是一名中学老师,现在是一名15年的肺癌幸存者。

2005年,51岁的梅丽莎克劳斯即将开始新的生活,因为她的孩子已经去上大学了。然而不幸的是,她被诊断患有肺癌,这让她感到非常意外,因为她从不吸烟,并且酷爱运动。手术切除了部分左肺,当时基因检测只能检测EGFR,结果是阴性的。于是她只能进行了化疗。但在2009年,她的肝脏又出现了癌症,从那以后她几乎尝试了所有的疗法,包括放疗和质子。
幸运的是,梅丽莎去拜访了曾在麻省总医院工作的著名肺癌肿瘤学家Jeffrey Engelman博士后,对她的肿瘤重新进行了ROS1和MET等生物标志物的综合检测,并发现她竟然存在RET融合。她在麻省总医院的主治医生建议她马上去纪念斯隆·凯特琳(Mean Sloan Kettering)参加开展的RET新药临床试验,并介绍了Alex Drillon博士,当时这款药物只有代号,叫做LOXO-292,这让克劳斯的肿瘤迅速萎缩。
“我现在感觉比现在好多了,”克劳斯说。她可以自己去商店购物,帮她的女儿照看五岁的孙女。

2020年5月8日,传奇抗癌药LOXO-292加速获批上市了,同时也有了自己的大名-Retevmo,不得不说,这款对于RET基因融合的患者有着显著疗效的广谱抗癌药将给病友们带来全新的选择和希望。
Retevmo也是首个被批准专门用于治疗携带RET基因变异的癌症患者的精准疗法。
2、MET--缓解率达68%!首款MET抑制剂卡马替尼上市
卡马替尼作为一种口服的高选择性小分子MET抑制剂,于2020年5月6日被美国FDA批准上市。最重要的是,卡马替尼(Tabrecta、capmatinib、INC280)是FDA批准的针对局部晚期或转移性MET 14跳跃突变的非小细胞肺癌(NSCLC)患者的首款靶向药。
METex14突变是公认的致癌驱动因素。诺华与Foundation Medicine合作,正在开发针对卡马替尼的伴随诊断剂,用于肿瘤组织和液体活检,将包括在FoundationOneCDx以及即将推出的Foundation Medicine液体活检平台中,目前正在接受FDA审查。
这款药物不管是对于初治的患者还是既往接受过化疗的患者,疗效都是非常显著,在II期临床研究GEOMETRY mono-1中,共97例患者入组:
(1)在初治患者(28例,先前没有接受过治疗)中,总缓解率(ORR)为67.9%,疾病控制率(DCR)为96.4%,中位缓解持续时间(DOR)为11.14个月,中位无进展生存期为9.69个月。
(2)在经治患者(69例,先前已接受过治疗,88.4%含铂化疗)中,总缓解率ORR为40.6%,疾病控制率(DCR)为78.3%,中位缓解持续时间DOR为9.72个月,中位无进展生存期为5.42个月。
(3)约有一半的脑转移患者对capmatinib应答(13人中有7人;54%)。在这些患者中,有4例完全消除了脑部病变(31%),颅内疾病控制率DCR为92.3%(12/13)。
3、KRAS-AMG510首次攻破堡垒,国内临床试验即将招募
作为人类癌症中最常出现突变的致癌基因-KRAS基因,从最初发现至今的30多年里,还没有一款直接针对KRAS突变的靶向药物。
而在2019年,针对KRAS这一靶点的抑制剂AMG510终于攻破了这一堡垒,疾病控制率达100%!让”不可成药“的魔咒将成为历史。
首次人体试验,Ⅰ期临床研究(NCT03600883),29例KRAS G12C突变实体瘤可供评估,其中10例非小细胞肺癌,19例肠癌等实体瘤。 重点是,在10例NSCLC患者中,ORR创下史上新高,达到50%,而疾病控制率更是满分100%!对于无药可用的KRAS突变NSCLC患者,AMG510将来来逆转奇迹!5例部分缓解的患者仍在继续服药中(7.3-27.4周),最长的已经超过27周。
一位为55岁男性NSCLC患者,既往尝试了几乎所有的治疗方案,(包括化疗、厄洛替尼、PD1、dasatinib、M3541)均以失败告终,后用AMG510(360mg),肿瘤缩小了67%,并且在用药18周时达到完全缓解,病灶已经消退到无法测量。
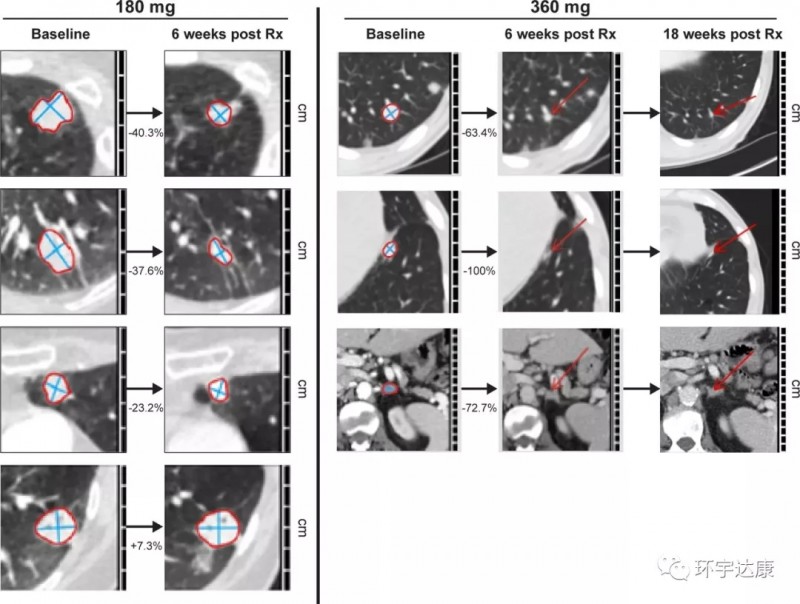
好消息是,这款有望攻克KRAS的抗癌新星已经来到中国,即将正式开展临床试验。3月9日,CDE(国家药监局药品审评中心)官网公布,安进公司研发的KRAS G12C抑制剂AMG 510临床申请获药审中心承办,意味着将在不久后开始招募国内晚期肿瘤患者,全球肿瘤医生网将会密切关注,及时为大家提供招募信息。想参加的患者可以登录全球肿瘤医生网医学部了解入组详情。

肺癌的免疫治疗-让更多的晚期患者获得“免死金牌”
近两年,免疫检查点抑制剂无疑是最成功的肿瘤免疫疗法之一,已经改变了NSCLC的治疗前景。目前获批用于肺癌的四大PD-1/L1将晚期肺癌不到5%的五年生存率一下提高到16%,翻了整整3倍,让不少患者乃至医生为之振奋。免疫疗法正在逐渐成为治疗晚期非小细胞肺癌的“特效”药物。目前FDA已经批准了四款免疫检查点抑制剂用于非小细胞肺癌的治疗。2020年,免疫治疗进军肺癌治疗的脚步依然没有减慢,加速上市了众多新的疗法,给更多的患者带来“免死金牌”
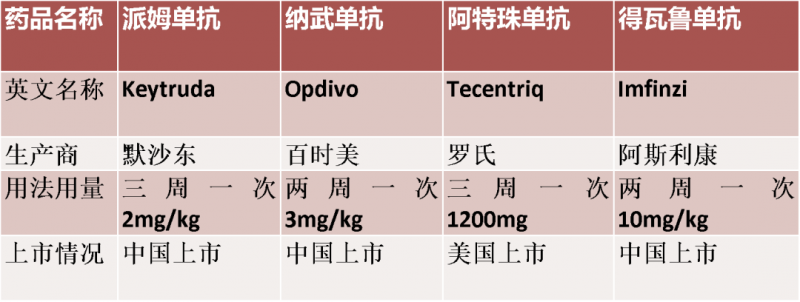
1、免疫黄金组合O+Y跻身肺癌一线治疗
5月15日,百时美施贵宝(BMS)公司宣布,美国食品和药物管理局(FDA)已经批准PD-1免疫检查点抑制剂Opdivo(欧狄沃,nivolumab,纳武利尤单抗)联合CTLA-4抑制剂Yervoy(伊匹木单抗,ipilimumab,易普利姆玛)及有限疗程的含铂双药化疗用于一线治疗无EGFR基因突变和ALK融合的转移性或复发性非小细胞肺癌(NSCLC)。
这一喜讯表明Opdivo与低剂量Yervoy联合一定疗程的化疗,能够在一线治疗中为非小细胞肺癌患者带来生存获益。这款联合疗法将让NSCLC患者无论PDL1表达高低,都可以做到去化疗。调整后的双免疫方案毒性也低于化疗。
2、T药单药提前获批,非小细胞肺癌再添一线新疗法
5月19日,罗氏(Roche)宣布,美国FDA批准其重磅PD-L1抑制剂Tecentriq(atezolizumab)上市,作为一线单药疗法,治疗PD-L1高表达,且无EGFR或ALK基因突变的晚期非鳞状和鳞状非小细胞肺癌(NSCLC)患者。这是Tecentriq在非小细胞肺癌领域获得的第四个适应症。
阿特珠单抗(Atezolizumab)是一种单克隆抗体,可靶向PD-L1蛋白。阿特朱单抗与肿瘤细胞和肿瘤浸润性免疫细胞上表达的PD-L1结合,阻断其与PD-1和B7.1受体的相互作用。通过抑制PD-L1,可以激活T细胞消灭肿瘤细胞。
目前,Tecentriq已经在中国获批上市(阿替利珠单抗,商品名泰圣奇),联合化疗用于一线治疗广泛期的小细胞肺癌。
肺癌的生物免疫治疗-初现光芒
近两年,免疫检查点抑制剂无疑是最成功的肿瘤免疫疗法之一,但不尽人意的是,PD-1仅对20%~30%的患者起效,如何让更多的患者能够获益于免疫治疗,如何进一步提升免疫治疗的无进展生存率是肿瘤学家们现在和未来积极探索的方向。
1、PD-1耐药有救了!TILs疗法再为生命续航
在过继性细胞免疫治疗领域,除了血液肿瘤中家喻户晓的CAR-T细胞疗法,实体肿瘤中最具潜力的当属TILS(肿瘤浸润淋巴细胞)疗法。去年的ASCO会议上,基于TILS细胞的创新型疗法LN-145和LN-144(Lifileucel)在治疗宫颈癌和黑色素瘤的临床结果一经公布,就引起了医学界的广泛关注,其中黑色素瘤中的TIL治疗具有持续数十年的完全应答(CR)的潜力,这种长期的作用归功于记忆T细胞的持久性。
肺癌是全球发病和死亡最高的癌症,尽管近年来靶向和免疫治疗发展已经让肺癌越来越趋于慢性病的治疗,但是对于一些患者来说,当最后的保底药物PD-1发生耐药后,仍让患者们感到恐慌。
美国时间4月27日,在今年的AACR会议上,一项由美国癌症中心莫菲特癌症研究中心(H. Lee Moffitt )开展的基于TIL细胞治疗的Ⅰ期临床结果公布:在12名可评估的非小细胞肺癌患者中,TIL疗法可达到25%的总缓解率,其中两名患者达到持久的完全缓解。
尽管这项研究规模很小,但还是令肿瘤学家们感到振奋,因为这些患者都是临床上已经接受过PD-1(Opdivo)治疗后病情进展的晚期患者,这些患者可以说是山重水复疑无路,最为难治的患者群体了。
当从这些患者体内的肿瘤病灶中提取出抗癌能力超强的TILs细胞,并在体外扩增培养成数十亿有着精准杀伤能力的免疫大军,回输到体内作战时,大部分患者在首次TIL治疗后进行 CT扫描就开始出现明显的肿瘤消退。
这项试验共有32名患者参加,最终有16名患者接受TILS治疗,其中12名患者可以评估。在平均随访1.4年时,3名患者病情缓解,其中两名完全患者,并且已超过一年。另一名患者的缓解即将得到确认。
大部分患者在接受TILs治疗后,肿瘤病灶都有所缩小,在接受治疗后的第一次CT扫描时,肿瘤病灶直径平均缩小38%!
因此,在PD-1治疗后,TILs疗法仍具有令晚期转移性非小细胞肺癌达到持久缓解的能力,这是非常了不起的,期待这款疗法能加大研究,早日获批上市,为晚期患者的生命持续续航!
2、客观缓解率翻倍!NK+PD-1成为阻击非小细胞肺癌的王炸组合
除了T细胞外,人类自然杀伤NK细胞也会表达PD-1,并且也具有延长晚期NSCLC患者生存的潜力,那么,将PD-1和NK联合起来会不会组成抗癌的王炸呢?
近日,这个设想由国内的研究团队率先实锤,并发表在国际顶级期刊《The Journal of Clinical Investigation》上。值得一提的是,此研究是目前所知的国内第一个研究派姆单抗和NK细胞输注联合使用的安全性和有效性试验,派姆单抗联合NK细胞在先前接受过治疗的PD-L1+晚期非小细胞肺癌患者中提高了生存率。
这项研究的结果非常振奋人心,输注扩增的NK细胞后,患者的NK细胞数量显着增加,抗癌效果倍增。
肺癌疫苗探索时代-将肺癌变成慢性病成为可能
如果有一种癌症疫苗能够成功触发强烈的免疫应答并且在适合的人群中使用,就可以显著改善肺癌存活。临床研究显示,三种正在研究的肺癌疫苗如tecemotide,TG4010和belagenpumatucel-L暂时不符合主要终点。癌症疫苗的历史经历了许多失败,但癌症疫苗的研发一直是医学研究领域激烈探索的热点。
那么,究竟有没有一种可以预防和治疗肺癌的疫苗呢?
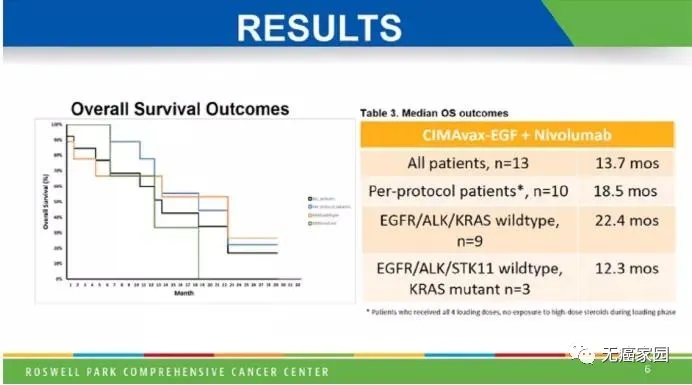
1、古巴EGF疫苗联合O药延长生存期至13.7个月
古巴EGF疫苗(CIMAvax-EGF)是一种比较古老的肺癌治疗性疫苗,先前的III期临床研究结果显示晚期NSCLC一线化疗结束后以古巴疫苗维持治疗,中位OS为12.43个月,优于化疗的9.43个月。
此次会议上报道了古巴EGF疫苗联合O药治疗NSCLC的I期研究结果。该研究纳入13例患者,大部分患者PD-L1表达为0。结果显示,古巴EGF疫苗联合O药之后患者可以更快达到足够的抗EGF效果,4剂古巴EGF疫苗联合O药后100%的患者抗EGF抗体滴度> 1:4000,而在以前的研究中单独使用古巴EGF疫苗时为56%。
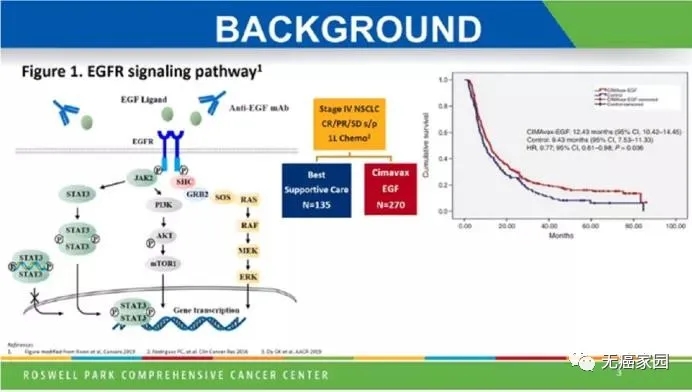
13例患者的中位OS为13.7个月,优于Checkmate 057研究中O药单药治疗PD-L1<10%患者的9.9个月。而完成4剂古巴EGF疫苗注射的10例患者中,中位OS达到18.5个月。
此外,EGFR/ALK/KRAS阴性的9例患者中位OS达22.4个月,而EGFR/ALK/STK11阴性KRAS阳性的3例患者中位OS为12.3个月。这似乎与Checkmate 057研究相反,联合治疗时KRAS阴性患者总生存期获益更大。
2、新型肺癌疫苗TedopiⅢ期试验数据公布,竟能破解PD-1耐药
2020年4月1日,OSE Immunotherapeutics公司宣布其新型抗癌疫苗Tedopi在非小细胞肺癌的Ⅲ期临床试验(代号为Atalante 1)取得了阳性结果,入组的所有患者在免疫检查点抑制剂(PD-1)耐药或失败后,二线或三线使用Tedopi疫苗,一年的总生存率达到46%,远超预设的25%!
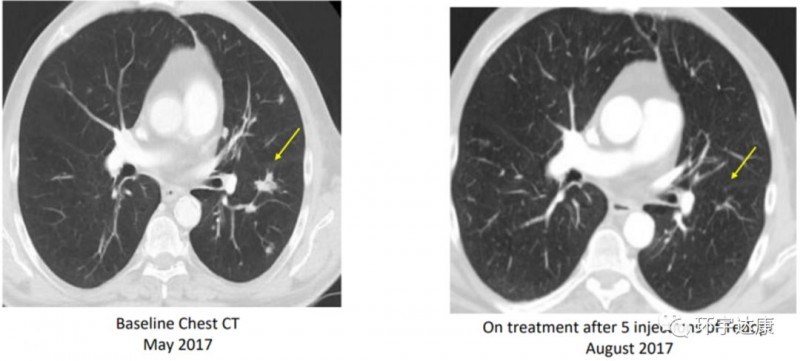
一位54岁的晚期肺癌患者在经过5次的新型肺癌疫苗注射后,肿瘤就迅速萎缩(从39毫米降至23毫米),截止报道时,生存期已经超过20.6个月,目前仍在随访中。
美国抗癌黑科技-电场疗法登录中国
电场疗法是一种低频率,低强度的电场技术,它会精准的破坏处于快速分裂期的癌细胞。
2020年5月113日,美国抗癌黑科技肿瘤电场疗法-Optune通过了在中国获得的临床研究豁免资格,正式被国家药品监督管理局(NMPA)批准上市!用于治疗组织学证实的复发性多形性胶质母细胞瘤(GBM)的成年患者(22岁或以上),以及与替莫唑胺联合治疗新诊断胶质母细胞瘤。
同时,它也有了自己掷地有声的中文大名--爱普盾。
另外还有几个好消息宣布:
1.电场疗法将在2020年完成一线胃腺癌的2期中试临床试验的注册;
2.向中国提交恶性胸膜间皮瘤的临床豁免申请;
3.2020年下半年公布针对非小细胞肺癌患者的3期关键性LUNAR试验的中期结果。
这意味着,全球发病率和死亡率最高的肺癌也可能被电场疗法斩获,也期待电场疗法对于中国高发难治性的胃癌能有确切的临床数据。
瑞士温特图医院癌症中心的医学肿瘤学主任Miklos Pless在2010年欧洲医学肿瘤协会(ESMO)上发表了重要数据:在瑞士的四个中心进行一项单臂二期临床研究,招募了42名患有局部晚期和转移性的NSCLC(IIIb-IV期)患者,这些患者先前化疗失败,每天接受TTF治疗12个小时,并联合使用培美曲塞(爱宁达,礼来公司),直到病情恶化。
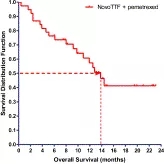
结果显示:
1.接受TTF联合培美曲塞治疗组相比单独培美曲塞治疗平均存活时间为13.8 vs 8.3个月;
2.联合治疗一年生存率为57%,单独培美曲塞治疗只有30%;
3.当TTF联合培美曲塞治疗,无进展的存活时间增加了一倍多,达到了22-28周,单独培美曲塞治疗仅为12周!
4.唯一报告的TTF治疗不良反应是在治疗位轻微到中度的皮肤刺激。
目前,肺癌电场疗法的三期临床试验([ LUNAR试验 ]-NCT02973789)已经正式开展,旨在测试电场疗法(TTFields)与免疫检查点抑制剂或多西紫杉醇联合用于非小细胞肺癌(NSCLC)患者的二线治疗的安全性和有效性。该试验预计招募534名患者,目前正在欧洲、美国和加拿大多个中心招募患者,想了解招募详情的患者可以登录全球肿瘤医生网医学部()。
写给病友的话
今天给大家分享的这些药品和技术不是想说某种治疗有多神奇,而是想告诉广大的肺癌病友,随着医学的发展,我们离”无进展生存“的那一步会越来越近,大家一定要坚定信心,在正规的治疗方案后,结合近年来的抗癌技术综合治疗,强调多学科协作,个体化处理的原则,根据不同患者的身体状况、肿瘤部位、侵及范围、有无黄疸、肝肾及心肺功能状况,有计划、合理的综合应用现有的诊疗手段,并采取积极的措施预防癌症的复发和转移,才能提高五年生存率,战胜癌症。最后祝大家也能像上面的几位患者一样,成功跨过一个又一个五年!
我们也能感受到,在药品审评审批制度改革以来,国内新药上市速度已大幅提升。相信随着医药改革、医学研究和无数患者与医疗工作者的共同推动,肺癌患者今后会越来越好,带着这个美好的祝愿,希望社会越来越好,希望医疗越来越好!







































 首页
首页 咨询
咨询 方舟新药
方舟新药 营养商城
营养商城