肿瘤药物筛选方法,3D类器官培养模型及其应用
它来了,它来了,因疫情而停摆数月的肿瘤中心学术沙龙活动,它又重新回来啦。2020年7月13日晚,中心迎来了疫情后的第一次学术沙龙。本期嘉宾是蒋明教授(浙江大学遗传研究所,国家青年千人计划获得者),主题是“3D类器官重建前肠相关疾病及其应用”。聚焦学术前沿,关注新兴技术,就让我们回顾一下这期的内容吧。


主讲人简介

蒋明,浙江大学“百人计划”研究员,博士生导师,浙江大学遗传学研究所/浙江大学附属儿童医院双聘研究员。研究方向主要聚焦于前肠起源的器官,包括食管和肺的干细胞在器官发育及相关疾病中的功能。主要研究不同的干细胞参与损伤后修复以及在肿瘤形成过程中的作用,并且深入了解其分子机制,为疾病的临床诊断和治疗奠定坚实的理论基础与科学依据。同时深入探究参与胚胎发育,器官生成,干细胞动态平衡及机关疾病的信号通路。以第一或者共同通讯作者在Nature,Journal of Clinical Investigation,PNAS和Development等杂志发表了多篇论文。
蒋教授开篇就类器官的概念对我们做了简要的介绍。类器官(Organoids)是在过去十多年间发展的新兴体外细胞培养技术,属于三维(3D)层面,与常规的2D细胞培养相比,此类体外培养系统包括一个自我更新干细胞群,能形成与对应来源器官拥有类似的空间组织并能够重现对应器官的部分功能。在2017年,该技术还被Nature Method杂志评为生命科学领域的年度技术。
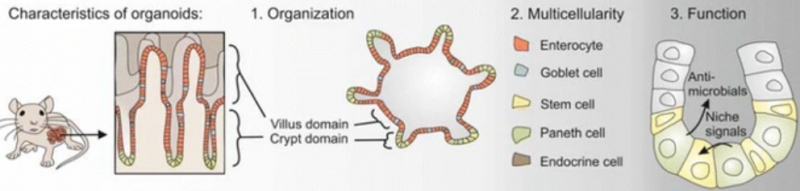
培养皿中的“微器官”
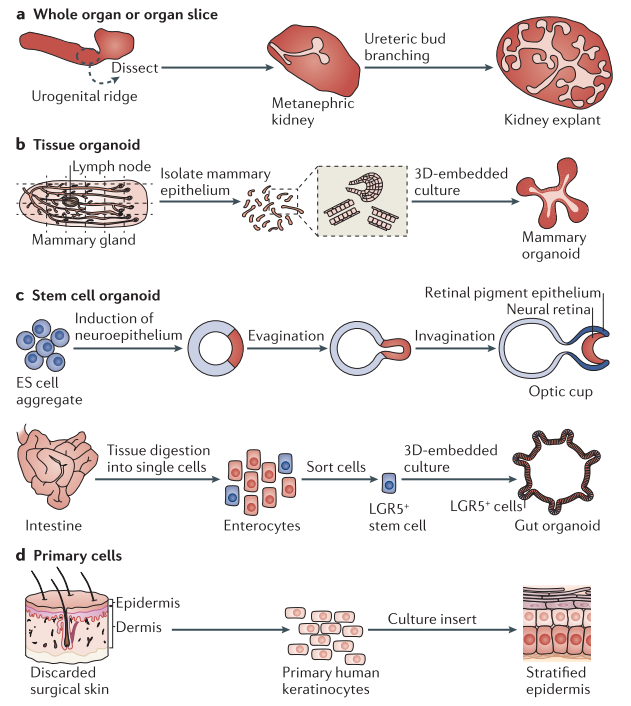
类器官建立流程图
相对于传统细胞培养,类器官具有更接近生理细胞组成和行为、更稳定的基因组、更适合于生物转染和高通量筛选等优势,而与动物模型相比,类器官模型的操作更简单。因此该技术在组学分析,疾病模型重建,药物筛选,新药研发等领域都有独特的应用价值。
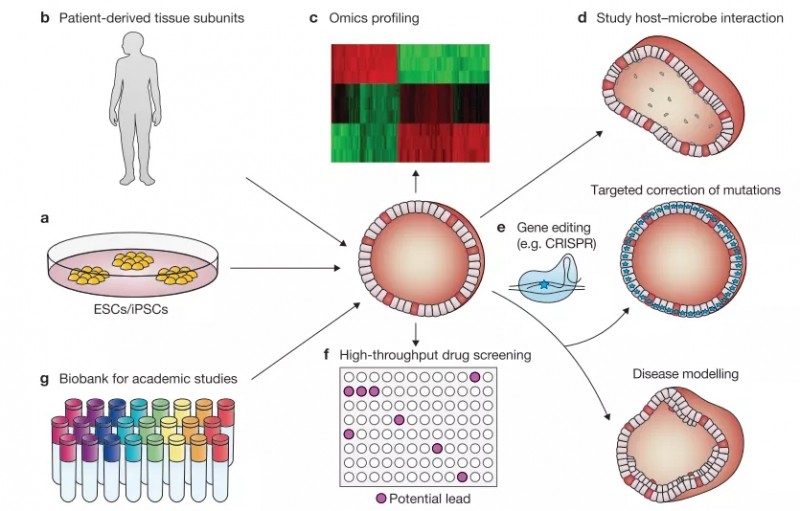
类器官的应用
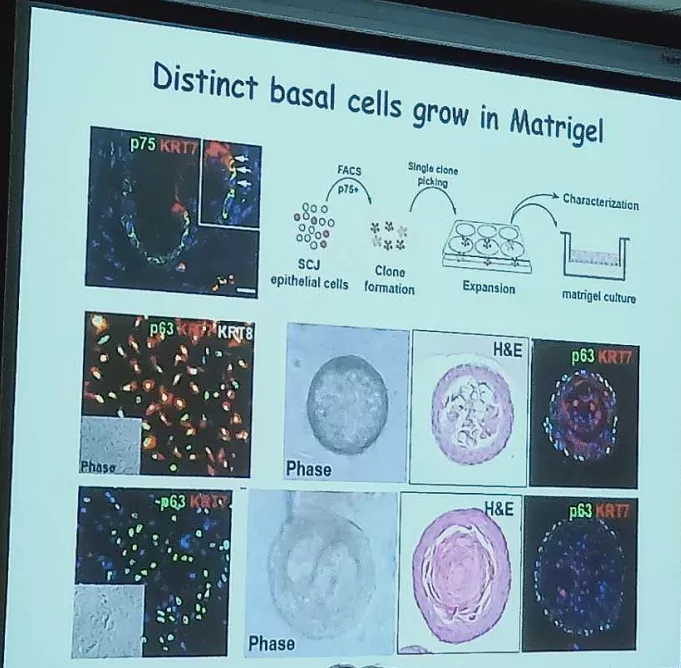
蒋教授团队也成功利用类器官培养出Barrett食管模型,并在此基础上证明消化道鳞状-柱状交界处的基底细胞群是过渡上皮祖细胞的来源。当特定分子异位表达时,这些过渡性基础祖细胞可分化为肠样上皮(包括杯状细胞),从而促进Barrett食管的化生。相关研究结果已发表于nature杂志。
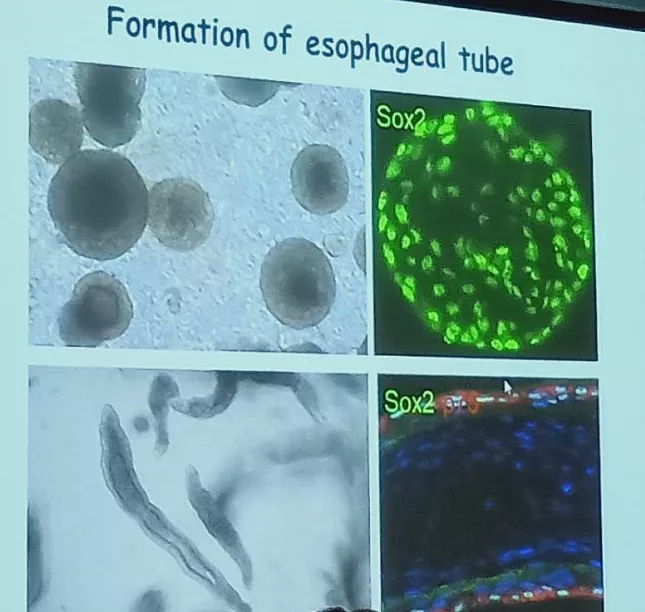
随后,蒋教授也畅谈了类器官技术在肿瘤研究领域的应用。目前在肿瘤研究领域比较新兴的技术包括全基因组测序(WGS),循环肿瘤DNA(ctDNA),循环肿瘤细胞(CTSs),人源性肿瘤组织异种植模型(PDTX),人源性肿瘤组织类器官模型(PDTO)等。针对PDX模型与PDO模型,蒋教授也做了详细的比较。同时蒋教授也为我们展示了团队培养成功的食管鳞癌,乳腺癌,胃癌等3D类器官模型。

当然,目前的类器官技术仍在发展中,其在肿瘤中的应用尚存在诸多的挑战性。包括如何模拟肿瘤的微环境,如何与免疫细胞共培养等仍是目前面临的挑战。同时由于肿瘤存在异质性,目前也并不是所有的肿瘤都能成功构建类器官模型。
参考文献:
1. Fatehullah A, Tan SH, Barker N. Organoids as an in vitro model of human development and disease. Nat Cell Biol. 2016;18(3):246-254.
2. Shamir ER, Ewald AJ. Three-dimensional organotypic culture: experimental models of mammalian biology and disease. Nat Rev Mol Cell Biol 2014;15:647-664.
3.Bartfeld S, Clevers H. Stem cell-derived organoids and their application for medical research and patient treatment. J Mol Med (Berl). 2017;95(7):729-738.
4.Jiang M, Li H, Zhang Y, et al. Transitional basal cells at the squamous-columnar junction generate Barrett's oesophagus. Nature. 2017;550(7677):529-533.
内容来源:浙大一院肿瘤中心 作者:汪旭孟







































 首页
首页 咨询
咨询 方舟新药
方舟新药 营养商城
营养商城