CD115,巨噬细胞集落刺激因子1受体CSF1R基因突变,CSF1R抑制剂
随着分子靶向治疗研究的进展,越来越多的新靶点、新靶向药物加入了这个抗癌的“大家庭”当中。每个靶点各有特点、每款药物各有所长,今天小汇要为大家介绍的,是一个常于肿瘤相关巨噬细胞中过表达的基因,CSF1R基因。
CSF1R:肿瘤相关巨噬细胞中过表达的基因
CSF1R的全称是集落刺激因子1受体,也被称为巨噬细胞集落刺激因子受体或CD115。最初,科学家在阿尔兹海默氏病和脑损伤后的小胶质细胞中发现了CSF1R基因表达水平的异常升高。
CSR1R基因
随着研究的深入,科学家们逐渐发现,除了一些炎性疾病,CSF1R突变还与乳腺癌、慢性粒细胞白血病等众多类型癌症的发生相关。同时,CSF1R还经常过量表达于肿瘤相关巨噬细胞中。
天生的免疫细胞,一朝沦落肿瘤"帮凶"
尽管巨噬细胞属于免疫细胞的一种,但在某些条件下,它们也会成为肿瘤发展的“帮凶”。许多研究都已经证实,存在于肿瘤组织中的巨噬细胞,在病灶血管生成、癌细胞的侵袭与转移、免疫抑制及耐药等方面,都发挥了促进作用。
但是,为什么巨噬细胞能被癌细胞“策反”呢?
人体的巨噬细胞属于先天免疫阶段,主要分为两种类型,M1和M2。这两类巨噬细胞的激活途径不同,具备的功能也完全不一样。
M1型巨噬细胞通过干扰素-γ与脂多糖或肿瘤坏死因子激活,为巨噬细胞激活的“经典”途径。这类巨噬细胞具备促进炎性反应和抗肿瘤(细胞毒性)的功能,是一类能够杀伤癌细胞的“正义”免疫细胞。
而M2型巨噬细胞则是通过白介素(IL)-4进行“替代”激活,反而具有完全相反的抗炎作用,能够抑制炎性反应,并修复受损的组织。
炎性反应又叫炎症反应,是机体对抗外伤、出血、感染或其它侵害时激发的生理反应,是先天免疫系统为移除有害刺激或病原、促进修复而触发的保护措施。M2型巨噬细胞能够抑制这种反应,其结果,就是为癌细胞的增殖和扩增创造了适宜的环境。
换句话说,在肿瘤病灶中被“养大”的巨噬细胞,凭着自己免疫细胞的身份,处处都在为癌细胞服务。而绝大多数情况下,人体免疫系统根本无法判断出它们的“叛变”,只能任由癌细胞在这部分巨噬细胞的帮助下“逍遥法外”。
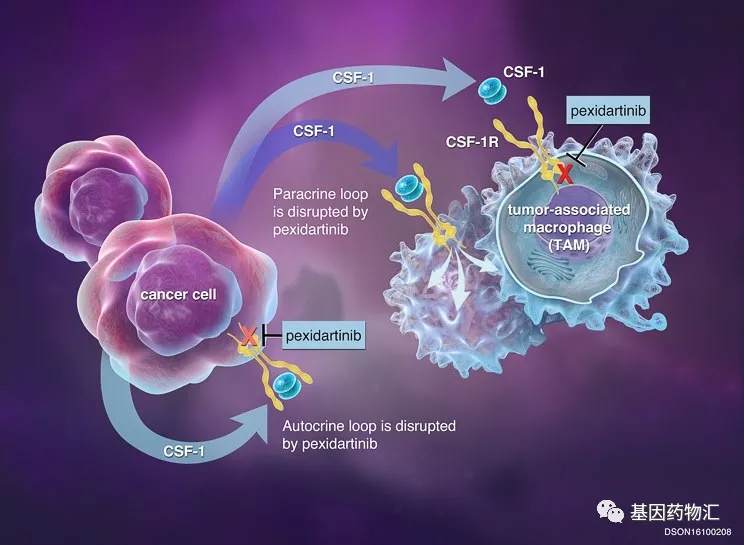
CSF1R抑制剂,给巨噬细胞一记"清醒巴掌"
CSF1R所介导的信号通路在单核吞噬细胞(尤其是巨噬细胞)的分化与生存中具有重要的作用。由于在肿瘤相关巨噬细胞中CSF1R普遍存在严重的过表达,因此CSF1R抑制剂能够比较有针对性地,给这些“叛变”了的巨噬细胞一记“正义的铁锤”。
包括已经获批和临床在研药物在内,目前临床上的CSF1R抑制剂数量不少,包括已经获批用于腱鞘巨细胞瘤的Pexidartinib(TURALIO),正在临床试验的PLX7486、ARRY-382、Edicotinib(JNJ-40346527)、BLZ945、AMG820、IMC-CS4及lacnotuzumab(MCS110)、C019199片等,当然,还有研究不太成功的Emactuzumab和Cabiralizumab等。
Pexidartinib,腱鞘巨细胞瘤的首款新药
Pexidartinib
2019年8月2日,FDA批准了第一三共制药所研发的Pexidartinib(TURALIO),用于治疗症状性腱鞘巨细胞瘤成年患者。这些患者存在因疾病导致的严重功能性障碍,且无法通过手术进行改善。
该批准基于ENLIVEN研究(NCT02371369)的结果,纳入患者均为不适合手术切除的症状性腱鞘巨细胞瘤患者。其结果显示,接受治疗25周后,接受了Pexidartinib治疗的患者整体缓解率38%,其中完全缓解率为15%,部分缓解率为23%;而接受安慰剂治疗的患者,缓解率为0。
腱鞘巨细胞瘤是一种非常罕见的局部侵袭性肿瘤,每年的发病率约为11/100万。这类肿瘤通常发生于患者手指和手部的关节滑膜及剑鞘,少见于足趾部,平均发病年龄仅30岁,女性多见。疼痛、肿胀、运动功能受限、血性关节积液及进行性软骨损伤是腱鞘巨细胞瘤的主要症状表现。
长期以来,腱鞘巨细胞瘤的治疗以手术切除为主。弥漫型腱鞘巨细胞瘤(约占10%)术后易复发,但反复进行手术可能导致复发率进一步上升,并导致患者关节受累、功能下降。
最严重的腱鞘巨细胞瘤,患者软骨或骨质受到破坏,可能需要接受关节置换或截肢治疗。
Pexidartinib是首款应用于腱鞘巨细胞瘤的靶向药物。对于复发风险高、却不适合接受手术的患者来说,这一疗法的问世可以说是一项“零的突破”,为患者带来了接受治疗的可能。
目前,Pexidartinib的Ⅲ期临床研究(NCT02371369)正在进行,广泛覆盖包括中国中心在内的全球40余个中心。而Pexidartinib的各类联合用药方案,如Pexidartinib+艾日布林(Eribulin,一种可用于治疗乳腺癌及脂肪肉瘤的药物)治疗乳腺癌、Pexidartinib+紫杉醇治疗卵巢癌、Pexidartinib+派姆单抗治疗多种实体瘤、Pexidartinib+得瓦鲁单抗治疗结直肠癌及胰腺癌等,同样在筹备或进行阶段。
PLX7486
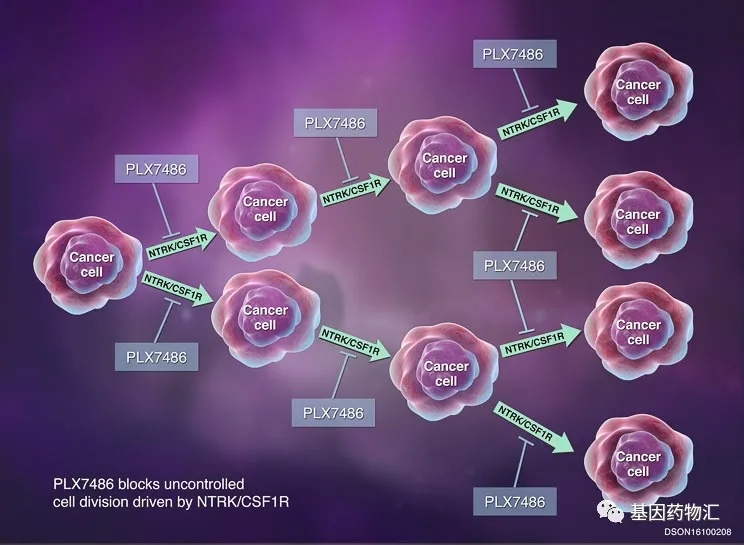
PLX7486与Pexidartinib同为Plexxikon研发,目前正在进行Ⅰ/Ⅰb期临床试验(NCT01804530),研究其治疗NTRK或CSF1R驱动的恶性肿瘤的疗效。
C019199片
C019199片是一款由我国药企福建海西新药创制自主研发的创新药物,已经于近期获得国家药品监督管理局批准,正在进行Ⅰ期临床试验(CTR20202045),用于治疗结直肠癌、黑色素瘤、胰腺癌及腱鞘巨细胞瘤。局部晚期或转移性的患者,若标准治疗失败、无标准治疗方案或无法接受标准方案治疗,可以考虑参加本项临床试验。
希望申请参加试验的患者,可以将病例资料发送至招募中心邮箱(doctorjona0404@gmail.com)进行申请,或联系全球肿瘤医生网医学部(400-666-7998)详细咨询。






































 首页
首页 咨询
咨询 方舟新药
方舟新药 营养商城
营养商城