PD-L1、TGFß(TGF贝塔)双靶点抑制剂新药M7824(Bintrafusp Alfa)客观缓解率近90%
Bintrafusp alfa(M7824)可同时阻断PD-1-PD-L1和TGFR2-TGFβ信号通路,解除免疫抑制,双双恢复机体免疫杀伤能力,理论上讲,该双功能融合蛋白具有优于传统PD-1/PD-L1单抗的临床获益。
临床前研究已经证实了PD-L1和TGFβ途径之间可能存在互补作用,还显示出M7824(非抗PD-L1抗体)具有逆转癌细胞的间充质化和增强对化疗反应的能力,它的双重抑制可增强抗肿瘤活性。
通用名:bintrafusp alfa
研发代号:M7824
靶点:PD-L1、TGFß
厂家:Merck(默克)
2020年3月,《胸腔肿瘤杂志》发布了一项I期临床研究,评估了M7824治疗非小细胞肺癌(NSCLC)患者的有效性和安全性。
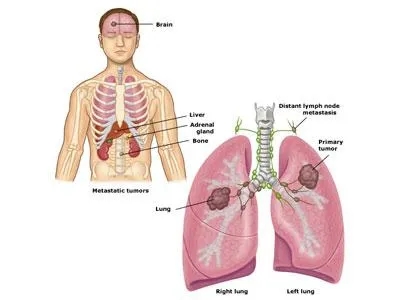
临床数据
这项NCT02517398的扩展队列,是一项正在进行的一期开放标签试验,共纳入了80例既往接受铂类化疗后疾病进展且未接受过免疫治疗的晚期NSCLC患者。
所有患者按照1:1进行随机分组,分别接受500mg或1200mg的M7824治疗,每2周一次。该研究的主要研究终点为最佳总体缓解(BOR),主要通过客观反应率(ORR)。
入组人群特征为:半数为亚裔患者;72.5%为PD-L1阳性,16.3%为PD-L1高表达(≥80%);78.8%的患者既往接受过一线治疗。
研究数据显示:中位随访时间为51.9周,所有患者的客观缓解率(ORR)为21.3%,部分缓解(PR)为21.3%,疾病稳定(SD)为16.3%,疾病进展(PD)为48.8%;疾病控制率(DCR)为40%;总生存期(OS)为13.6个月;中位无进展生存期(PFS)为2.6个月,12个月的PFS率为20.1%;中位缓解持续时间(DOR)为14.1个月。
两组(500mg剂量组 VS 1200mg剂量组)的ORR为17.5% VS 25.0%,PR为17.5% VS 25.0%,SD为12.5% VS 20.0%,PD为55.0% VS 42.5%;DCR为32.5% VS 47.5%;中位OS为10.9个月 VS 15.6个月,12个月的OS率为44.6% VS 65.5%;中位PFS为1.4个月 VS 4.0个月;中位DOR为14.1个月 VS NR(not reached未达到),由此可见1200 mg的剂量对患者效果更佳,因此也被定为II期研究的推荐剂量。
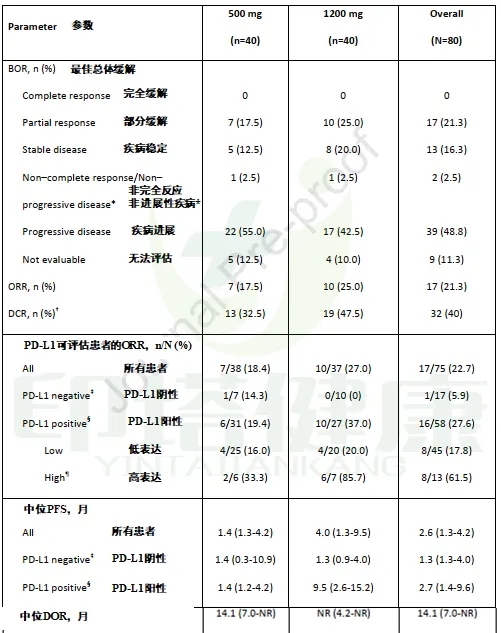
图注:M7824治疗接受铂类化疗后疾病进展且未接受过免疫治疗的晚期NSCLC患者临床数据
PD-L1可评估患者的总体ORR为22.7%;PD-L1阴性患者的ORR为5.9%;PD-L1阳性患者的ORR为27.6%;PD-L1低表达患者的ORR为17.8%;PD-L1高表达患者的ORR为61.5%。
两组(500mg剂量组 VS 1200mg剂量组)PD-L1可评估患者总体ORR为18.4% VS 27.0%;PD-L1阴性患者的ORR为14.3% VS 0%;PD-L1阳性患者的ORR为19.4% VS 37.0%;PD-L1低表达患者的ORR为16.0% VS 20.0%;PD-L1高表达患者的ORR为33.3% VS 85.7%。
在1200mg剂量组中,PD-L1表达阳性和高表达患者的PFS分别达到9.5和15.2个月,12个月的PFS率也提升为35.4%和68.6%。PDL1表达阳性和高表达患者的OS均未达到。
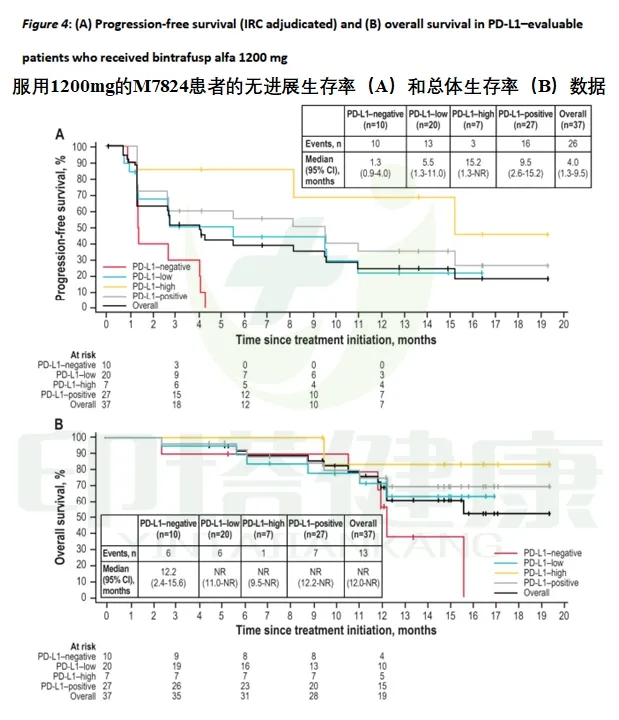
图注:1200mgM7824治疗接受铂类化疗后疾病进展且未接受过免疫治疗的晚期NSCLC患者的PFS和OS
不良反应
治疗相关不良反应(TRAEs)发生率为69%;3级或3级以上的不良反应发生率为29%;8例(10%)因不良反应导致停药,未发生与治疗相关的死亡事件。
常见的不良反应为瘙痒、黄斑皮疹、食欲差、虚弱、皮疹、恶心、甲状腺功能减退、天冬氨酸转氨酶增加、丙氨酸转氨酶增加、口腔炎等。
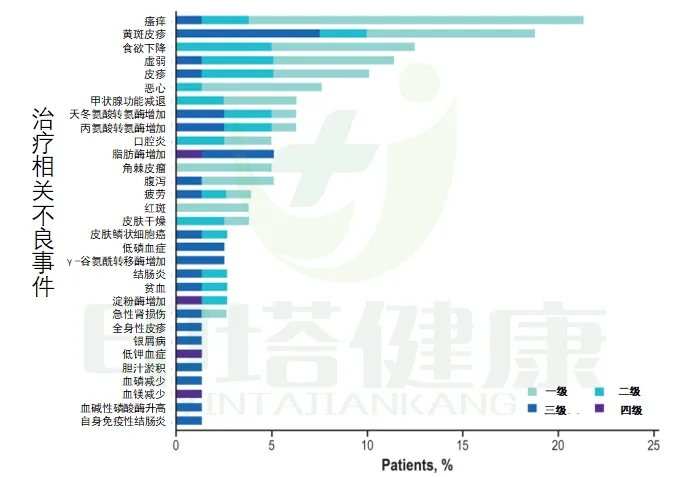
图注:M7824治疗接受铂类化疗后疾病进展且未接受过免疫治疗的晚期NSCLC患者不良反应
小结
M7824在非小细胞肺癌患者中具有令人鼓舞的疗效和可管理的耐受性!
参考来源:https://www.jto.org
文章来源:yintahealth 全球好药资讯







































 首页
首页 咨询
咨询 方舟新药
方舟新药 营养商城
营养商城