2021年世界肺癌大会(WCLC),五款抗肺癌新药,肺癌最新药物震撼登场
世界肺癌大会(WCLC)是世界上最大的致力于肺癌和其他胸部恶性肿瘤的多学科肿瘤学会议,每届都有来自全球100多个国家的7,000多名专业人士参会,共同探讨肺癌和其他胸部恶性肿瘤的最前沿治疗进展。由于疫情的影响,第21届世界肺癌大会(WCLC 2020)一再推迟,终于在2021年1月28日至31日以线上虚拟会议的形式顺利举行!

2021,五款肺癌重磅新药登场,点亮生命之光
今年的会议上又公布了肺癌治疗的各种最新的数据,璀璨夺目。给肺癌患者带来全新的治疗选择和希望。全球肿瘤医生网医学部第一时间为大家整理了5大新药重磅研究进展,在抗癌的道路上为您点亮希望之光。

01、ROS1融合新突破!TPX-0005创下客观缓解率86%最高记录
在本次世界肺癌大会上,最振奋人心的新药之一就是ROS1融合阳性抗癌新药Repotrectinib(瑞波替尼,代号TPX-0005),其最新的2期研究TRIDENT-1的中期数据公布,客观缓解率高达86%!也是基于此,2020年12月8日,美国食品药品监督管理局(FDA)授予Repotrectinib(代号TPX-0005)突破性疗法指定,有望加快对Repotrectinib的审批上市。下面我们一起来看看这项研究的惊艳数据。
这项研究的代号为TRIDENT-1,在截止至2019年7月22日的第一阶段数据显示,未接受过TKI治疗的ROS1阳性患者的客观缓解率高达91%。
此次公布的是截至2020年7月10日第二阶段最新的中期数据,结果表明:
1.初治ROS1阳性非小细胞肺癌患者,客观缓解率达到86%;
2.经过TKI及化疗的非小细胞肺癌患者,客观缓解率达到40%;
3.经过TKI但未接受化疗的ROS1阳性非小细胞肺癌患者,客观缓解率达到67%;
4.NTRK阳性TKI经治的晚期实体肿瘤患者,客观缓解率达到50%。
这项数据非常振奋人心,也使Repotrectinib有潜力成为ROS1或NTRK阳性肿瘤患者的同类最佳治疗方案,包括TKI初治和TKI经治患者。
repotrectinib在ROS1-TKI初治和耐ceritinib的患者中的临床活性看完数据后我们再来分享两个文献中报道的案例。
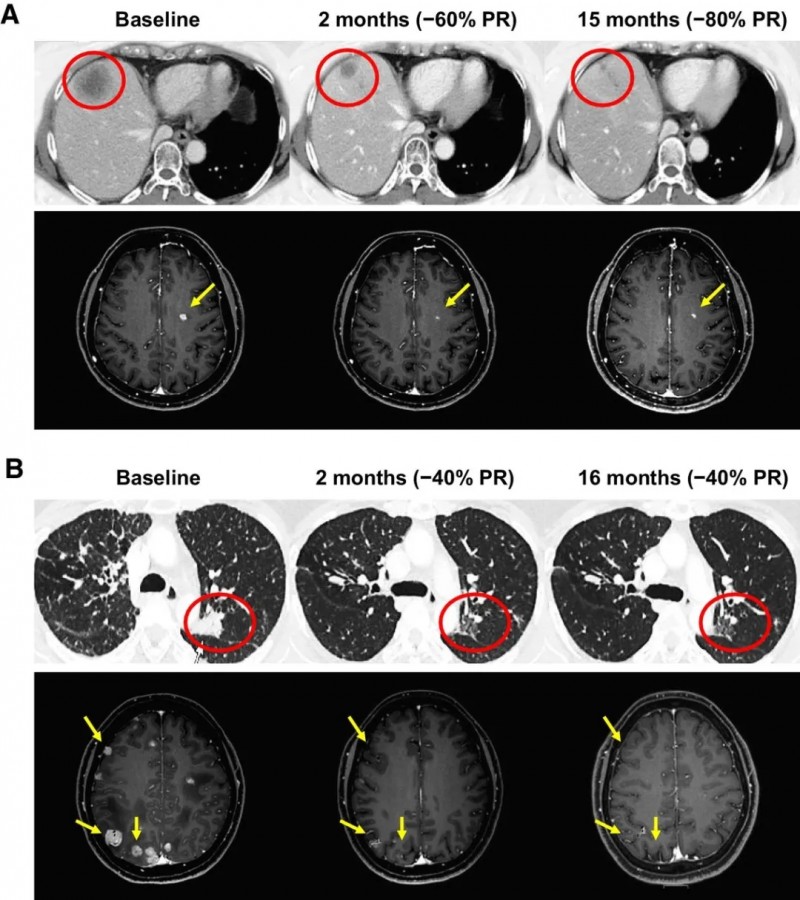
(A)第一位是初治的ROS1+患者,69岁的M女士在确诊为非小细胞肺癌后出现肝转移和多发性脑转移,经过基因检测后发现存在CD74-ROS1重排,于是M女士参加了I期repotrectinib试验,在每天接受一次40 mg repotrectinib治疗后15个月,肿瘤已经缩小了80%!(PR(-80%)),截至文献发表时,M女士已经持续缓解20月。
(B)另一位ROS1+患者在克唑替尼治疗后出现复发,复查时发现脑部有多个无明显症状的脑转移病灶,于是开始接受每天40–240 mgrepotrectinib治疗,在16个月时,肿瘤缩小了40%(PR(−40%))。
因此,不管是初治还是经治,这两位为患者的持续缓解时间都超过了15个月。
Repotrectinib(瑞波替尼,代号TPX-0005)是美国TP Therapeutics公司研发的第二代ALK/ROS1/TRK抑制剂,也是新一代的广谱抗癌药,临床证实其效力比克唑替尼高90倍。并且能够克服多种对其它TKI产生抗性的基因突变,杀死携带ROS1或NTRK基因融合的多种肿瘤细胞,因而有潜力治疗ROS1阳性的非小细胞肺癌,具有惊人的入脑效果。除此之外,它还对ROS1、NTRK和ALK阳性的实体瘤显示出强大的抗癌活性。我们期待这款药物能早日获批上市。
好消息是,目前这款广谱抗癌药已经来到国内,正式招募携带ROS1融合基因的非小细胞肺癌的这意味着,国内的患者也有机会免费接受国际抗癌新药的治疗。
申请流程:
需要申请临床试验的患者需将基因检测报告、病理报告提交至全球肿瘤医生网医学部进行初步评估,我们的专家将为您全面分析解读检测报告,一个工作日内电话联系推荐新药及用药方案,并匹配适合入组的临床试验项目。
02、即将上市!EGFR20外显子插入突变迎来新药Amivantamab
非小细胞肺癌EGFR突变靶向药的研发和上市一直是所有癌症里最多的,而EGFR ex20ins属于常见突变型中相对罕见的难治亚型,约占所有EGFR突变肺癌的10%,使用目前临床已获批的各类EGFR抑制剂疗效并不理想。
在今年的肺癌大会上,一款新药Amivantamab(JNJ-6372,JNJ-61186372)打破僵局,或将成为EGFR20外显子插入突变患者的首款上市靶向药。Amivantamab于2020年3月获得了FDA突破性指定,并且10月在中国进入了突破性治疗药物的批准程序;2020年12月,这款药物已经向FDA提交了申请,如果一切顺利,Amivantamab将于预计将于2021年上半年正式上市!
在本届WCLC上,研究者公开了来自CHRYSALIS研究(NCT02609776)的EGFR ex20ins队列的最新结果。让国内患者振奋的是,该队列中共81例患者,其中49%的患者为亚洲人。
结果显示,中位随访6.5个月,所有患者的整体缓解率为36%,均为部分缓解,临床获益率73%;中位缓解持续6.8个月,中位无进展生存期8.3个月,中位总生存期22.8个月。
03、反转!Mobocertinib治疗EGFR20ins突变效果显著
除了JNJ-6372,本次世界肺癌大会上公开的Ⅰ/Ⅱ期EXCLAIM试验(NCT02716116)扩展队列的研究结果,新药Mobocertinib(TAK-788)治疗EGFR ex20ins患者也取得了显著的疗效。
研究共纳入了96例患者,其中49%的患者曾接受过超过2线全身方案治疗。
结果显示,在所有用药剂量的亚组中,中位治疗6.5个月时,患者的整体缓解率为23%;中位缓解持续时间尚未达到,中位无进展生存期为7.3个月。
而在曾接受过铂类化疗的患者中,整体缓解率为26%;中位无进展生存期7.3个月,12个月无进展生存率33%。
2020年4月28日,FDA授予Mobocertinib(TAK-788)突破性治疗指定,用于EGFR ex20ins突变型非小细胞肺癌的治疗。这款新药的疗效,对于这部分难治患者来说,是一份全新的希望。
Mobocertinib是一种有效的小分子靶向药,专门设计用于选择性靶向EGFR外显子20插入突变。Mobocertinib已经在2020年4月获得FDA突破性疗法的认可,用于EGFR exon20插入突变型,铂类化疗后疾病进展的转移性NSCLC的患者。在2020年10月,mobocertinib在中国也获得了突破性疗法指定。
Amivantamab和Mobocertinib均有望为EGFR ex20ins患者带来治疗突破。与Mobocertinib相比,Amivantamab距离上市显然更近一步。
除了这两款“外国药”,我国自主研发的新药也取得了一定的进展。如我国药企自主研发、用于治疗EGFR ex20in突变型患者的人源化EGFR单克隆抗体创新药物JMT-101。
JMT-101属于进行了相关结构优化的第二代抗体药物,对糖基化末端进行了相关修饰,相比目前已获批的西妥昔单抗等,药物亲和力提高了近6倍,抗肿瘤活性明显提升。
目前,这款药物在结直肠癌的治疗中已经取得了比较理想的试验数据,根据2020年ASCO上公布的数据,接受JMT101联合联合mFOLFOX6治疗的患者,客观缓解率达到57.1%,疾病控制率更是达到了100%。
近期,JMT-101治疗多种实体瘤的Ⅰ期临床试验已经陆续开始。其中,治疗非小细胞肺癌的Ⅰb期试验正在招募患者。存在EGFR 20号外显子插入突变(包括重复突变)的ⅢB或Ⅳ期非小细胞肺癌患者 ,在经过初治或一线治疗失败后,可以尝试这款新药的治疗。
有需求的患者可以联系全球肿瘤医生网医学部进行咨询,或将基因检测报告、诊断报告的电子版或清晰照片发送至新药招募中心邮箱(doctor.huang@globecancer.com)进行申请。
04、新型抗体偶联药物DS-1062治疗转移性NSCLC曙光初现
TROP2是一种跨膜糖蛋白,在许多癌症类型中过度表达。在非小细胞肺癌患者中,有高达64%的腺癌和高达75%的鳞状细胞癌中观察到TROP2表达,通常这类患者总生存期和无病生存期较差,临床上一直没有有效的药物。
DS-1062使用一种可以在肿瘤附近被选择性切割的四肽链接子将靶向TROP2的单克隆抗体与一种拓扑异构酶抑制剂连接在一起。
在本次世界肺癌大会上,一款新型的抗体-药物偶联物(ADC)达托单抗deruxtecan(Dato-DXd; DS-1062)打破瓶颈,显示出了令人鼓舞的抗肿瘤活性和可控的安全性,可用于TROP2阳性的晚期或转移性非小细胞肺癌(NSCLC)患者。
本次大会公布了DS-1062的1期TROPION-PanTumor01积极的试验结果。总计159名晚期或转移性NSCLC患者接受了不同剂量的DS-1062(4 mg/kg, 6 mg/kg或8 mg/kg)的治疗。这些患者都是已经接受过3种以上的前期治疗,包括含铂化疗(94%)或免疫疗法(84%)的极晚期患者。在中位随访时间为7.4个月时,客观缓解率(ORR)在21%~25%之间,疾病控制率在67%~80%之间,中位无进展生存期在4.3个月和8.2个月之间。
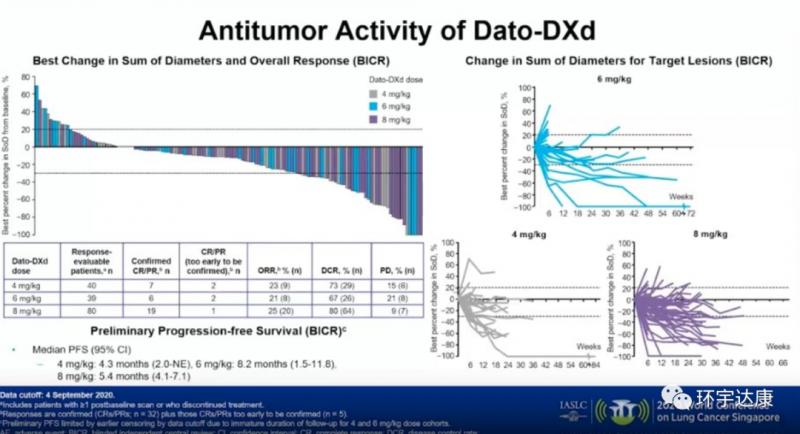
值得一提的是,有2例接受4 mg / kg剂量的患者,2例接受6 mg / kg剂量的患者和1例接受8 mg / kg剂量的患者达到完全或部分缓解,还需要进一步的随访确认。
05、疾病控制率高达80.6%,AMG510击败史上最难治靶点KRAS
KRAS是最臭名昭著的突变之一,因为几十年前研究人员就已经将KRAS确定为癌症的重要治疗靶点,从发现这一靶点至今的30年里,还没有一款直接针对KRAS突变的靶向药物获批。因此,人们一直认为它是一种“不可摧毁的”蛋白质,这种蛋白质缺乏明显的靶点可以让小分子药物可以结合并损害其功能。
经过三十年的研究,AMG 510成为第一个达到临床阶段的KRAS G12C抑制剂!

2020年12月8日,FDA授予Sotorasib(AMG510)突破性疗法称号,用于治疗KRAS G12C突变的局部晚期或转移性非小细胞肺癌。这是KRAS突变非小细胞肺癌适应症中首款获得突破性疗法指定的新药,标志着基于KRAS突变的非小细胞肺癌靶向疗法,正式翻开了一个全新的篇章。
而在本次世界肺癌大会上,公布了AMG510最新的CodeBreaK 100的第二阶段队列研究结果,数据非常振奋人心。
这项试验纳入了124例既往接受过化疗和/或免疫疗法疾病进展的KRASG12C突变的晚期非小细胞肺癌患者。
结果显示:客观缓解率(ORR)为37.1%,其中包括3例完全缓解和43例部分缓解,疾病控制率为80.6%。中位反应持续时间为10个月。
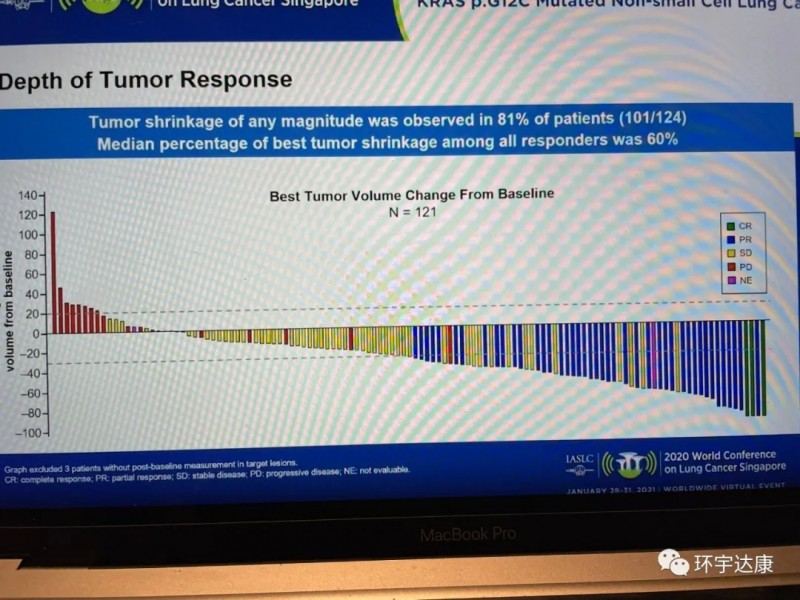
AMG510可能成为第一个针对KRAS基因突变而批准的靶向药。美国FDA已授予AMG510“快速通道”状态,用于先前经治的KRAS G12C突变的非小细胞肺癌。我们期待这一药物能尽快上市,给KRAS突变的患者带来救赎!
我们生活在肺癌治疗的分子革命中,越来越多的癌症患者通过一代一代的靶向药和免疫治疗药物获得了更长的生存期,甚至把肿瘤吃没了。进入靶向免疫治疗时代,每个患有肺癌的患者都应该通过基因检测,PD-L1,TMB分析,获得更多用药方案指导。我们已经了解了很多关于肺癌的分子遗传学以及如何将它转化临床治疗决策。未来还将有更多。
所以,你还在等什么,快去看看你的基因检测报告有没有这些可能带来生存奇迹的信息吧(需要解读报告或咨询基因问题,可以致电全球肿瘤医生网医学部400-666-7998或加入肺癌医患交流群获得更多知识和帮助)。
参考资料:
https://www.onclive.com/view/amivantamab-shows-encouraging-activity-in-egfr-exon-20-positive-nsclc







































 首页
首页 咨询
咨询 方舟新药
方舟新药 营养商城
营养商城