实体瘤是什么意思,广谱抗癌药是什么意思,不限癌种的肿瘤药物临床试验90%的患者都有机会尝试
靶向药物资讯看得多了,很多患者都遇到过“实体瘤”和“广谱抗癌药”这些说法。但以小汇最近得到的反馈,仍有许多患者对于这种定义方式感到迷茫,很难判断自己是否符合“实体瘤”的标准,或者能否尝试那些“广谱抗癌药”的临床试验。
“实体瘤”究竟是什么?它是指某一种癌症,还是指某一类癌症?
哪些药物有潜力成为“广谱抗癌药”?它们有什么特点?
面对一项以实体瘤为适应症的广谱抗癌药临床试验,患者应该如何判断它是否适合自己?
什么是"实体瘤"
实体瘤是一种因分类而诞生的概念。临床上,肿瘤有实体瘤(实体肿瘤)和非实体瘤(液体肿瘤)之分。
其中,液体肿瘤即血液肿瘤,包括白血病、淋巴瘤。这类肿瘤在所有的恶性肿瘤中占比接近10%。
实体瘤则是指起源于实体器官的肿瘤,包括常见的肺癌、乳腺癌、结直肠癌、肝癌等等。可以说,上至头颈、下至肢端,除了起源于血液、骨髓等血液组织的肿瘤以外,都可以归作实体瘤,占到了所有肿瘤的90%以上。
通常情况下,通过影像学检查如X线、CT、B超等,或初诊等检查方式,也可以探查到实体瘤患者体内(也有在体外的)有形的肿块,即实体病灶。
换句话说,对于癌症患者们来说,只要不属于血液肿瘤,就有机会尝试实体瘤的临床试验项目。
什么是广谱抗癌药
实体瘤适应症,有时候也被称为“不限癌种”,所有非血液系统的肿瘤均被纳入其中。而这些获批了实体瘤适应症,或有潜力用于各类实体瘤治疗的药物,被称为广谱抗癌药。
提到广谱抗癌药,许多患者都会想到两款经典的NTRK抑制剂拉罗替尼和恩曲替尼。但事实上,真正首先拿下实体瘤适应症的,是免疫治疗药物派姆单抗。
2017年,FDA首次批准了派姆单抗的实体瘤适应症,用于微卫星不稳定性高(MSI-H)或错配修复障碍(dMMR)、且无其它治疗选择的实体瘤患者。自此,这部分已经尝试过各类治疗手段无效的患者,终于有了一种“兜底”的方案。
至2019~2020年,两款NTRK抑制剂先后获得FDA批准上市,适应症均为NTRK融合突变阳性的实体瘤,在患者中掀起了一阵“广谱抗癌”的热潮。从医生到患者、从业者,每个人都盼望着这些“不限癌种”的治疗药物,能够成为癌症治疗的另一个突破口。
"实体瘤"适应症的药物,为患者带来了哪些变革
靶向治疗以及免疫治疗药物的诞生,代表着癌症精准治疗时代的开启,意味着人们对于癌症的治疗手段的认知,正式从器官和细胞的层面发展到了分子层面,创造了一种全新的癌症分类模式。原本不同的癌症,由于相同的驱动基因突变,可以被归于同一类。而广谱抗癌药的诞生正是这种分子层面研究不断发展的成果,为药物的研发与管理开创了全新的局面。
而对于癌症患者们来说,广谱抗癌药的问世带来的最大变革就在于,不论患者的原发部位是哪里,都能从这些药物的治疗当中获益,不必再等待每一个适应症逐步获得批准。
尤其是对于一些“小癌种”来说,由于患者数量少、临床试验项目少,原本等待一款新药上市遥遥无期,现在却可以因为“实体瘤”适应症而得到一款“救命药”了。
"广谱抗癌"意味着所有癌症患者都可以用吗
事实上,“不限癌种”并非没有任何限制,患者想要使用这些药物,仍然需要满足一些限制条件。以派姆单抗为例,根据FDA批准的适应症,能够在末线使用派姆单抗治疗的仅有MSI-H和dMMR的患者,若患者这两项指标均不达标,那么仍然难以从派姆单抗治疗中获益。
同样的,两款被誉为“治愈系”靶向药物的拉罗替尼和恩曲替尼,也只能适用于NTRK融合突变阳性的实体瘤患者。
所以“实体瘤”适应症,其实是在满足部分筛选条件的前提下,不限制患者肿瘤原发部位的一类适应症。
为什么只有部分药物的适应症是"实体瘤"
为什么只有一部分药能成为“广谱抗癌药”,这些药有什么独特之处?这个问题要从两个方面解释。
一方面,对于靶向治疗药物来说,这款药物的靶标必须是一个可能存在于多类癌症当中的驱动基因突变。这种突变的发生率整体可能并不高,如NTRK突变在所有实体瘤患者中仅有约1%,但广泛分布于17类癌症中,因而具备广谱抗癌的潜力。
另一方面,这款药物需要在临床试验中被证实对于各类癌症患者均有效果,才能真正获得批准上市。
有哪些正在招募实体瘤患者的临床试验项目
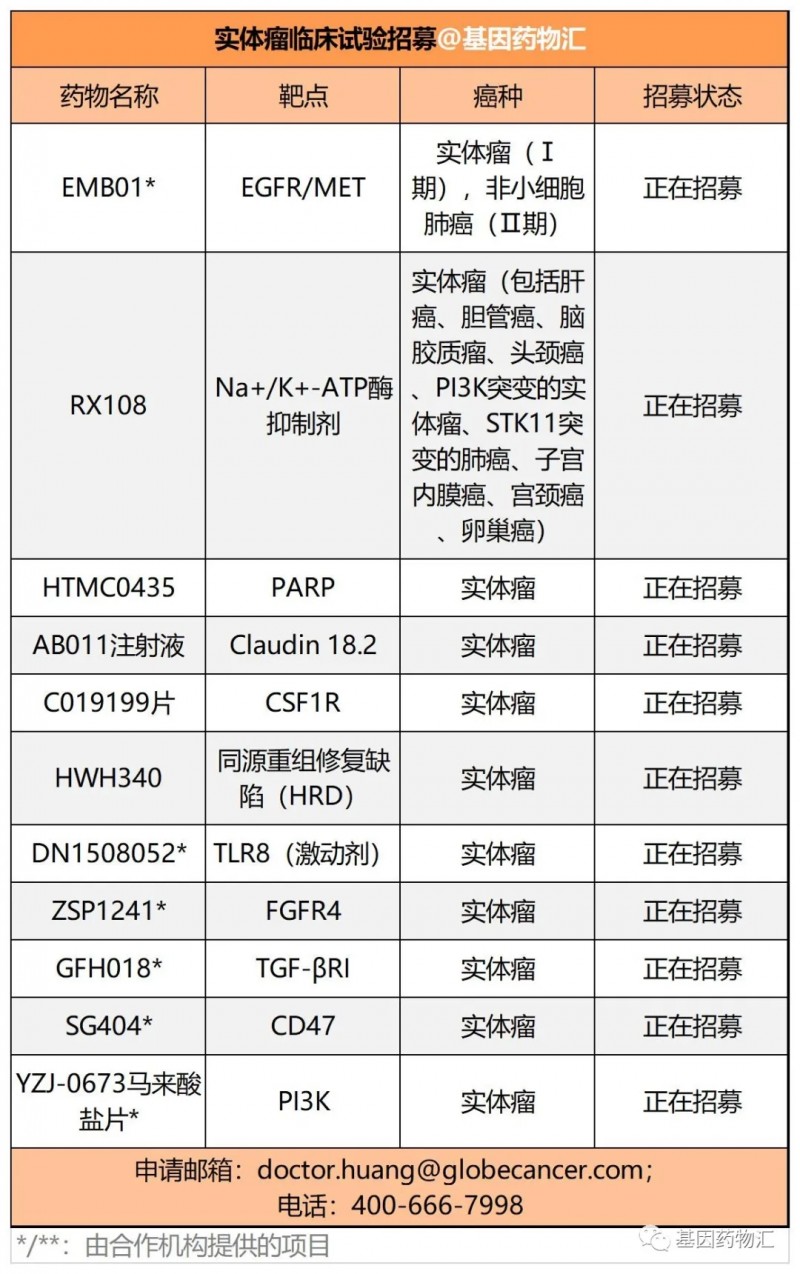
基因药物汇为大家精选了一部分不限癌种、正在招募患者的临床试验项目,为各位癌症患者提供申请临床试验的途径。
项目数量很多,我们根据药物的类型、靶点将项目粗分为8类。大家可以咨询全球肿瘤医生网医学部(400-666-7998)了解各项临床试验的具体入排标准,或进行申请。
NTRK/TRK抑制剂
通常情况下,NTRK在各类实体瘤中的检出率不足1%,但在部分特殊的癌种中检出率可以超过10%。
而各类NTRK抑制剂,疗效也不负“治愈系”之名,几乎每一款都疗效非常出众。首款上市的拉罗替尼,治疗各类实体瘤患者的整体缓解率为75%,其中完全缓解率高达22%;恩曲替尼治疗各类实体瘤患者的整体缓解率为57%,45%的患者缓解持续超过12个月。
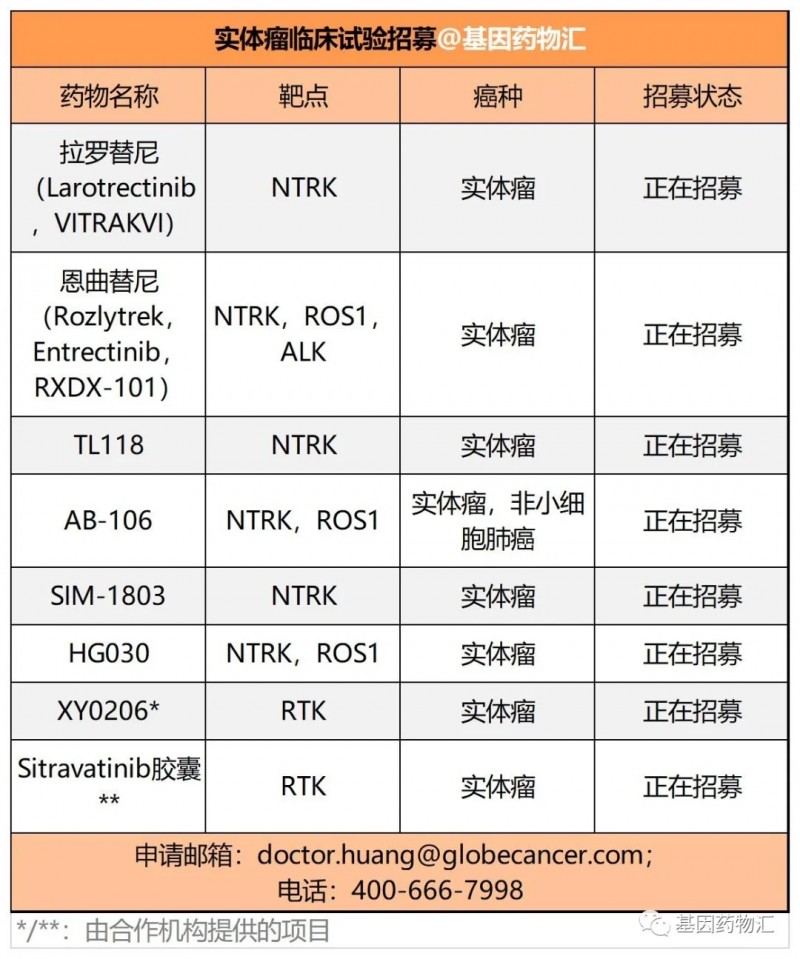
VEGF/VEGFR抑制剂
VEGF/VEGFR抑制剂又被称为抗血管生成抑制剂,主要通过抑制新血管的生成,来截断肿瘤病灶组织的血液供应,进而杀死癌细胞或抑制病灶的生长、扩散。
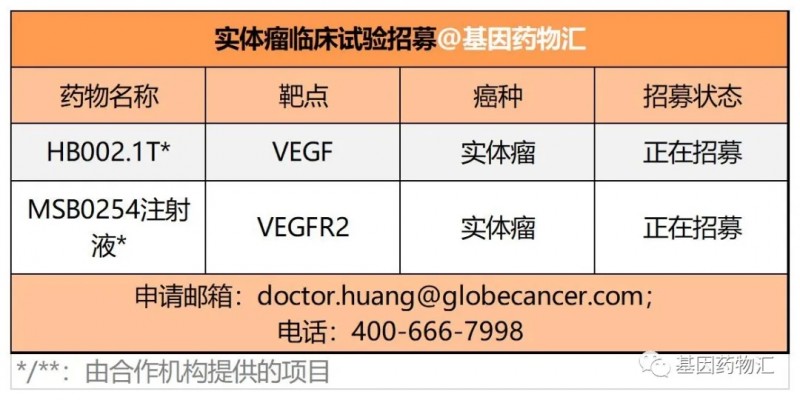
BRAF抑制剂
BRAF突变可能见于多个癌种,约50%~70%的恶性黑色素瘤、40%~70%的乳头状甲状腺癌、35%~60%的卵巢癌、5%~15%的结直肠癌、1%~3%的非小细胞肺癌患者存在BRAF突变,整体约占全部恶性肿瘤的8%。BRAF V600E是BRAF突变最常见的亚型。
这样的特点使BRAF同样成为了一个颇具潜力的广谱抗癌靶标。在一项2020年10月发布的临床试验中,研究者评估了BRAF抑制剂Encorafenib+MEK抑制剂Binimetinib治疗126例包括黑色素瘤及结直肠癌在内的多种实体瘤的疗效。结果显示,联合用药方案在结直肠癌中的缓解率为18%,在黑色素瘤中的缓解率为42%;其中,黑色素瘤初治患者的缓解率为67%。
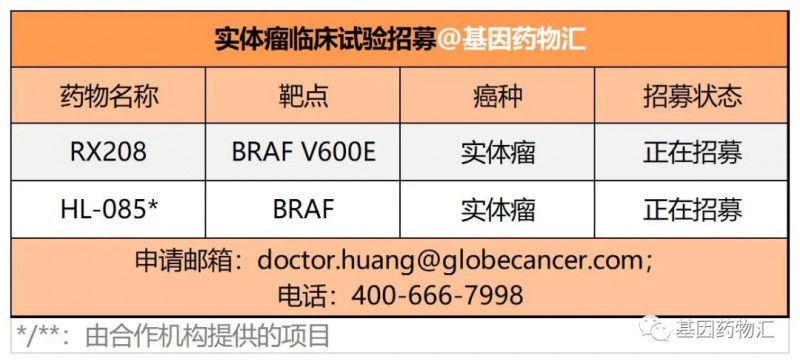
HER2抑制剂
HER2(人表皮生长因子受体2)是重要的癌症驱动基因,在多个癌种当中高度表达,其中肺癌检出率约2.5%,乳腺癌检出率约15%~25%,胃癌检出率约20%,胆管癌检出率约20%,卵巢癌检出率约27%,子宫内膜癌中检出率可以达到18%~80%。
使用HER2抑制剂治疗多种实体瘤的临床试验正在开展。如靶向HER2的双特异性抗体药物Zanidatamab,目前已经在胆管癌适应症获得了FDA的突破性治疗指定,治疗胆管癌整体缓解率为46.7%,疾病控制率66.7%。
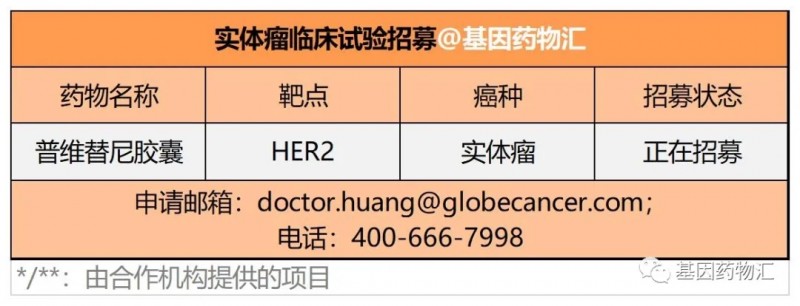
其它靶向药物
除了上述几种以外,还有很多具有泛癌种抗癌潜力的驱动基因或分子分型,如EGFR、MET等等都已经被证实在多类癌症当中存在一定的检出率。其中有检出率较高的类型,如Claudin 18.2、HRD,也有一些检出率较低、相对罕见的类型。但整体来说,正是因为这些靶点的药物的研发与进展,“让每一位癌症患者都找到合适的‘特效药’”的希望才逐渐变得可以触及。
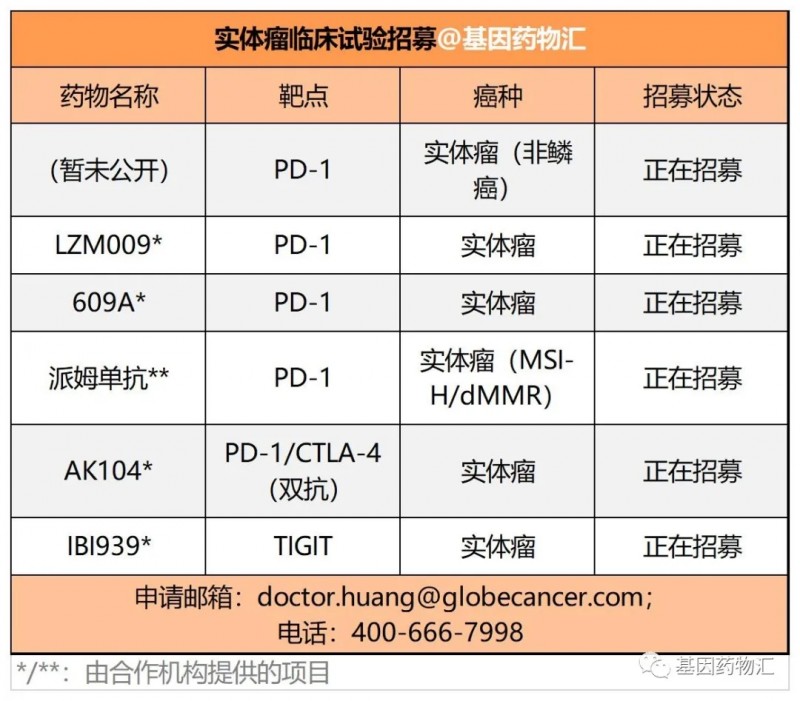
PD-1/PD-L1抑制剂等免疫治疗药物
免疫治疗是癌症精准治疗的另一个重要支柱。包括已经获批了实体瘤适应症的派姆单抗在内,各类免疫治疗药物均具有良好的泛癌种抗癌潜力。
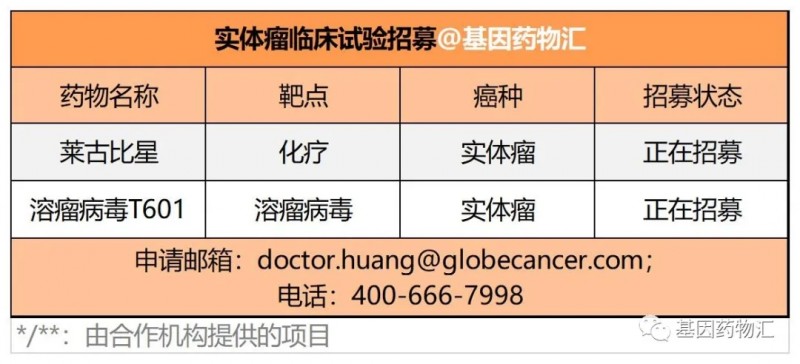
其它药物







































 首页
首页 咨询
咨询 方舟新药
方舟新药 营养商城
营养商城