2021年非小细胞肺癌CSCO指南,非小细胞肺癌最新治疗方案
CSCO 指南主要基于国内外临床研究成果和 CSCO 专家意见,确定推荐等级,是国内医生在临床实践中遵循和认可的临床治疗标准和参考,意义重大。
2021年中国临床肿瘤学会(CSCO)于近期在北京以线上线下相结合的方式,盛大召开。在本次大会上,来自全国各地的知名学者针对非小细胞肺癌诊疗进展进行要点解读,更新了众多新的治疗方案。全球肿瘤医生网医学部为病友们整理了最新的内容,供大家参考,希望给大家带来全新的希望。
非小细胞肺癌的分期
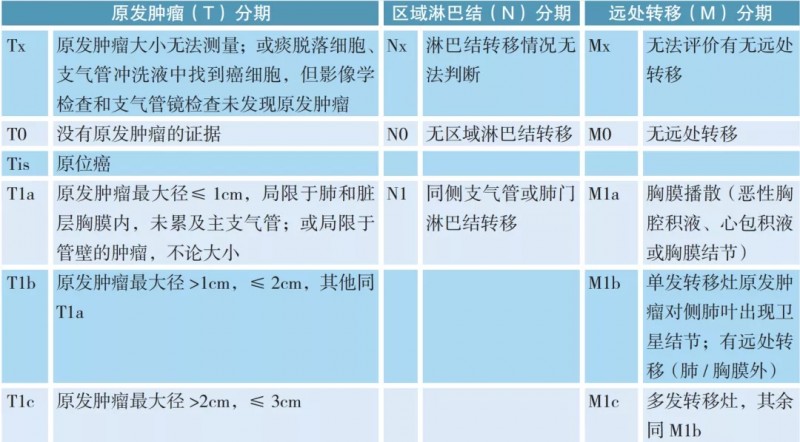
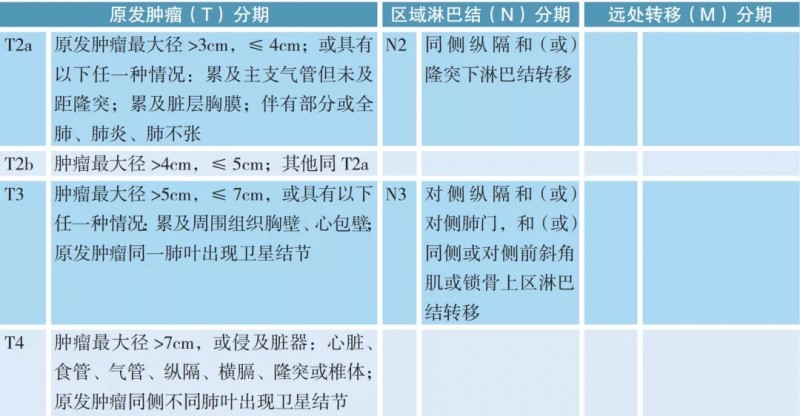
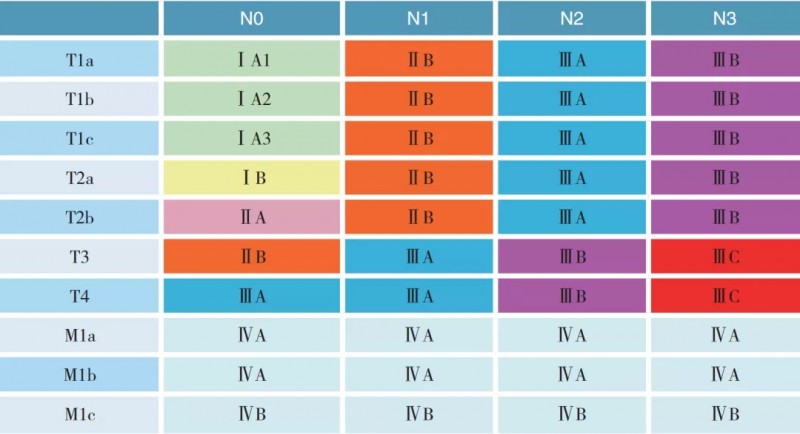
注:M1a/1b期均为Ⅳa期,M1c均为ⅣB期
不同分期非小细胞肺癌的治疗方案
2021更新内容
●早、中期原发性非小细胞肺癌的治疗(可手术)
1.早期EGFR实变肺癌的辅助治疗可选择奥希替尼辅助治疗。
2.纳武利尤单抗联合化疗作为可切除非小细胞肺癌的新辅助治疗,有望为患者带来潜在获益。
3.N2期完全切除术后不需要辅助放疗。
●不可手术的IIIA/IIBIIIC期NSCLC治疗
PACIFIC研究4年OS数据:度伐利尤单抗作为同步放化疗后巩固治疗。
●IV期驱动基因阳性非小细胞肺癌的治疗
1. EGFR突变NSCLC:阿帕替尼联合吉非替尼相比吉非替尼单药显著延长了无进展生存时间;伏美替尼获NMPA批准,用于治疗EGFR T790M突变阳性的局部晚期或转移性NSCLC;Mobocertinib被CDE纳入突破性疗法;Amivantamab被CDE纳入突破性治疗药物程序。
2.ALK阳性NSCLC:劳拉替尼获FDA批准用于一线治疗;恩沙替尼获NMPA批准二线治疗;Brigatinib获FDA扩大适应症批准;塞瑞替尼获NMPA批准用于一线治疗。
3.ROS1阳性NSCLC:FDA已授予Repotrectinib的突破性疗法资格。
4.MET exon14跳跃突变NSCLC:Capmatinib获FDA加速批准;Tepotinib获得MHLW批准;赛沃替尼获NMPA优先审批。
5.RET突变NSCLC: Selpercatinib获得FDA加速批准;Pralsetinib获得FDA以及NMPA批准二线治疗。
6.HER2突变NSCLC:吡咯替尼疗效具有前景,EnHertu获得美国FDA突破性疗法认定。
7.KRAS突变NSCLC:FDA授予了sotorasib突破性药物资格和实时肿瘤学审查资格,获NMPA、CDE授予突破性治疗药物资格。
●IV期无驱动基因的非鳞癌NSCLC治疗
1.一线单药治疗:KEYNOTE 024/042研究、IMPower 010研究、EMPower lung1研究2.一线联合治疗:CameL研究、ORIENT 11研究、RATIonALE 304研究、GEMSTONE 302研究CM227/9LA研究3.二线治疗:RATIonALE 303研究
●无驱动基因、IV期鳞癌治疗
1.一线单药治疗:KEYNOTE 024/042研究、IMPower 010研究、EMPower lung1研究
2.一线联合治疗:RATIonALE 304研究、ORIENT 11研究、CameL-sq研究、GEMSTONE 302研究CM227/9LA研究
3.二线治疗:RATIonALE 303研究、ORIENT 3研究。
01、ⅠA、ⅠB 期非小细胞肺癌的治疗

02、ⅡA、ⅡB 期非小细胞肺癌的治疗

03、ⅢA 或ⅢB(T3N2M0)期非小细胞肺癌的治疗(可手术)
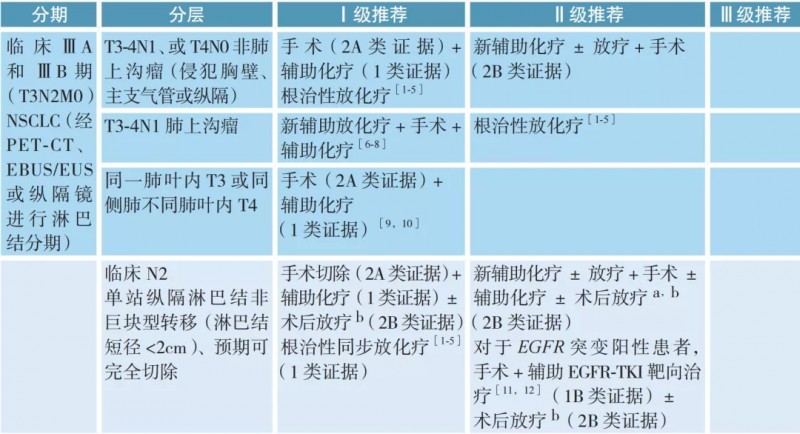

注:
a 若术前未行新辅助放疗,术后可考虑辅助放疗。
b 术后病理 N2 可以考虑术后放疗(2B 类证据) 或加入术后放疗随机分组研究。
c 该组患者的局部区域复发风险较单站 N2 淋巴结转移患者进一步升高,术后病理 N2 可以考虑术后放疗(2B 类证据)。
d 参考“不可手术ⅢA、ⅢB、ⅢC 期非小细胞肺癌的治疗”部分。
04、ⅢA、ⅢB、ⅢC 期非小细胞肺癌的治疗(不可手术)


05、Ⅳ期驱动基因阳性非小细胞肺癌的治疗方案
EGFR突变非小细胞肺癌的治疗
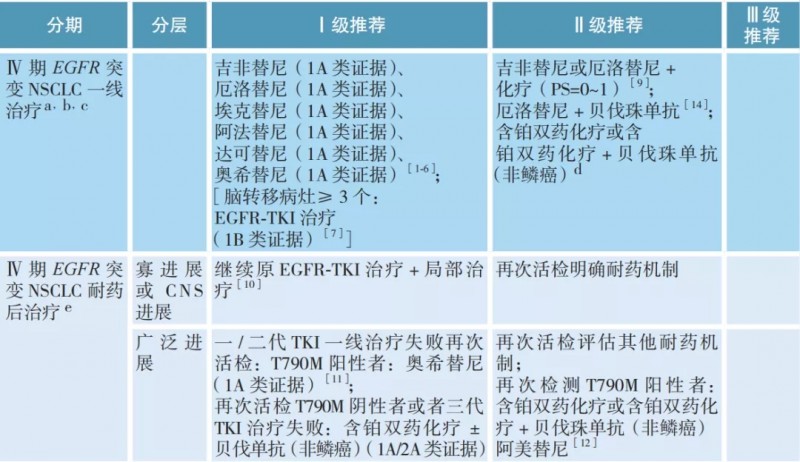

a. 本章节主要涉及多发转移患者,寡转移参考本指南其他相应章节;
b. 确诊 EGFR 突变前由于各种原因接受了化疗的患者,在确诊 EGFR 突变后,除推荐参考本指南选择EGFR-TKI 外,也可在疾病进展或不能耐受当前治疗时参考本指南一线治疗;
c. 部分患者确诊晚期 NSCLC 后因为各种原因未能明确基因类型,一线接受化疗的患者进展后活检明确诊断为 EGFR 突变,治疗参考本指南一线治疗;
d. 具体药物可参考本指南驱动基因阴性Ⅳ期 NSCLC 治疗部分;
e. 耐药后进展模式根据进展部位和是否寡进展划分为以下两种类型:寡进展或 CNS 进展:局部孤立病灶进展或者中枢神经系统病灶进展;广泛进展:全身或多部位病灶显著进展。
ALK突变非小细胞肺癌的治疗
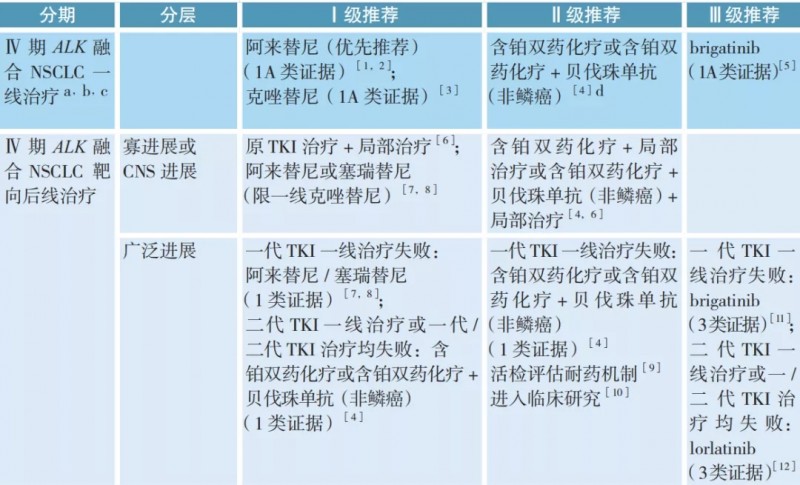

a. 本章节主要涉及多发转移患者,寡转移参考本指南其他相应章节;
b. 确诊 ALK 融合前接受了化疗,可在确诊 ALK 融合后中断化疗或化疗完成后接受 ALK 抑制剂治疗;
c. 确诊晚期 NSCLC 后未行 ALK 融合相关检测,一线治疗后活检为 ALK 融合,治疗参考本指南一线治疗;
d. 具体药物可参考本指南驱动基因阴性Ⅳ期 NSCLC 治疗部分。
ROS1 融合阳性非小细胞肺癌


a. 本章节主要涉及多发转移患者,寡转移参考本指南其他相应章节;
b. 患者确诊 ROS1 融合前接受了化疗,可在确诊 ROS1 融合后中断化疗或化疗完成后接受 ROS1 抑制剂治疗;
c. 确诊晚期 NSCLC 后未行 ROS1 融合相关检测,一线治疗后活检为 ROS1 融合,治疗参考本指南一线治疗;
d. 具体药物可参考本指南驱动基因阴性Ⅳ期 NSCLC 治疗部分。
BRAF V600E 突变 /NTRK 融合非小细胞肺癌
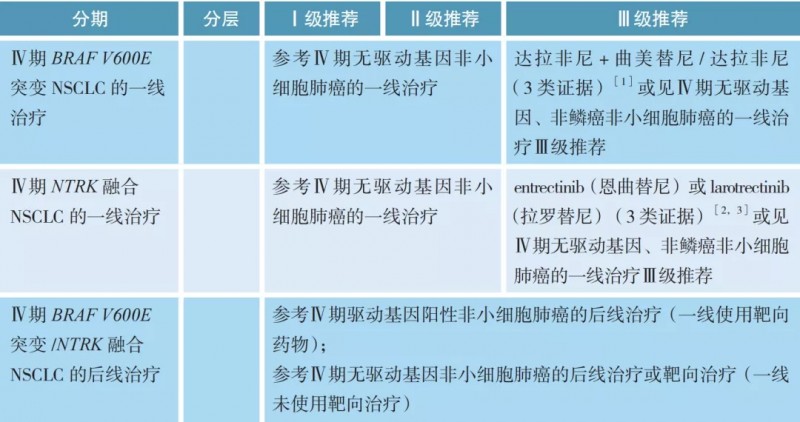
06、Ⅳ期无驱动基因、非鳞癌非小细胞肺癌


a. 抗肿瘤治疗同时应给予最佳支持治疗;
b. 包括原研贝伐珠单抗和经 NMPA 批准的贝伐珠单抗生物类似物;
c. 如果疾病得到控制且毒性可耐受,化疗直至疾病进展。
07、Ⅳ期无驱动基因、鳞癌的治疗
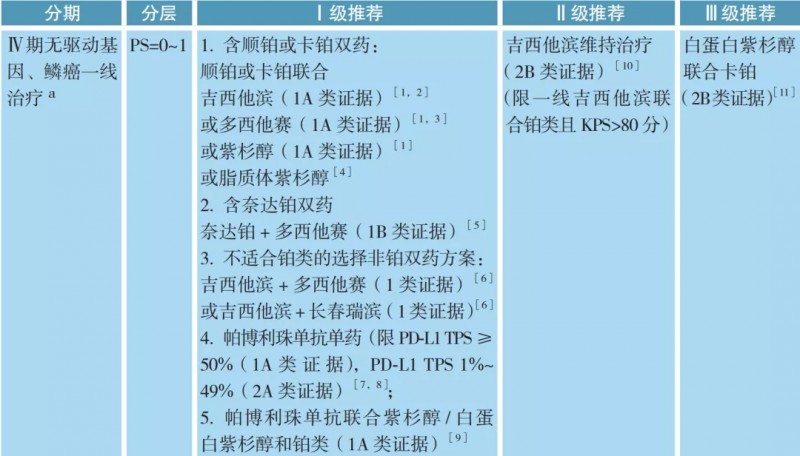
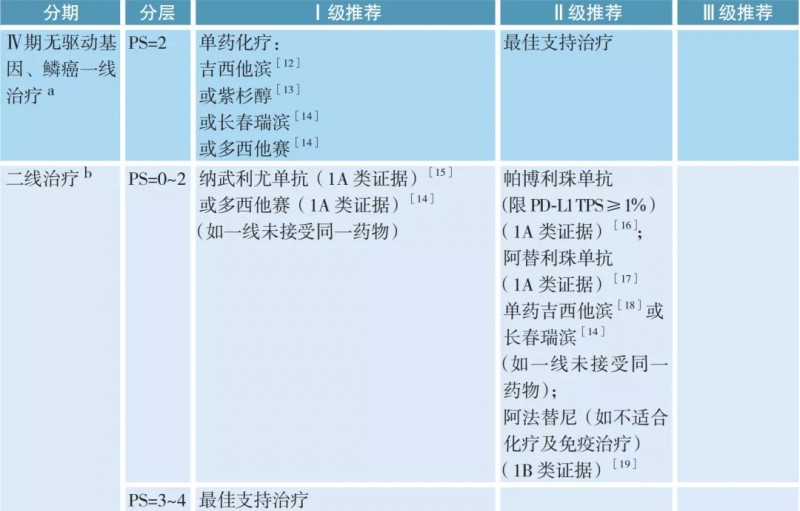

a. 抗肿瘤治疗同时应给予最佳支持治疗;
b. 如果疾病得到控制且毒性可耐受,化疗直至疾病进展。
写给病友的话
近年来,靶向和免疫药物势如破竹的研发和上市,让肺癌的治疗步入了黄金时代。截止2021年5月,非小细胞肺癌又有三块重磅新疗法获批上市,给晚期患者带来了新的选择和希望。
2021年2月3日,FDA批准tepotinib(Tepmetko)用于(MET)外显子14跳变的晚期转移性非小细胞肺癌;
2021年2月22日,FDA批准cemiplimab-rwlc(Libtayo,Regeneron Pharmaceuticals,Inc.)用于一线治疗高PD-L1表达(肿瘤比例评分[TPS]> 50%),且无EGFR,ALK或ROS1突变的晚期非小细胞肺癌(NSCLC)的患者;
2021年3月3日,FDA批准Lorlatinib一线治疗ALK阳性的转移性非小细胞肺癌患者。
不得不说,这是一个充满希望和奇迹的时代,给更多的肺癌患者带来了新的选择和希望。然而这些上市新药都远在美国,价格昂贵,中国的病友仅有个别经济条件雄厚的患者选择前往美国接受治疗,大部分病友只能望药兴叹。好消息是,目前国外上市的以及中国自主研发的几款针对肺癌EGFR,ALK,ROS1,RET,MET,NTRK靶点的抗肿瘤新药,开始招募国内患者了!这意味着,国内的患者也终于有机会免费用上这些效果更好,堪称天价的抗癌新疗法!想申请的患者可以联系全球肿瘤医生网将医学部进行初步评估,我们也将及时为大家提供招募信息。详情点击:
(注:请将基因检测报告,诊断报告电子版或拍照发送至doctor.huang@globecancer.com,邮件中留下联系方式,或直接致电医学部4006667998,医学部收到报告分析完毕后一个工作日内电话联系,为您全面分析检测报告,匹配能够入组的临床试验,以及有无新药可以使用)







































 首页
首页 咨询
咨询 方舟新药
方舟新药 营养商城
营养商城