中国首款CAR-T疗法阿基仑赛(益基利仑赛)注射液(Yescarta、Axicabtagene Ciloleucel、Axi-Cel,FKC876)获批上市,更多CAR-T临床试验招募汇总
就在昨天,中国国家药品监督管理局(NMPA)官方网站更新了一条全新的批准消息——由中美合营公司复星凯特引进、美国KITE生物技术公司研发的CAR-T细胞产品益基利仑赛注射液(阿基仑赛;Yescarta,Axicabtagene Ciloleucel,Axi-Cel;FKC876)正式获得了上市批准,中国终于迎来了首款CAR-T治疗方案!
此次益基利仑赛注射液获批的适应症为接受过二线或以上标准治疗后复发或难治性大B细胞淋巴瘤成年患者,包括弥漫性大B细胞淋巴瘤非特指型、原发性纵隔B细胞癌淋巴瘤、高级别B细胞淋巴瘤和滤泡淋巴瘤转化的弥漫性大B细胞淋巴瘤。
此前,益基利仑赛注射液已经获得了FDA批准,其适应症包括大B细胞淋巴瘤及滤泡性淋巴瘤。
超高缓解率、长期生存颠覆性的CAR-T治疗方案
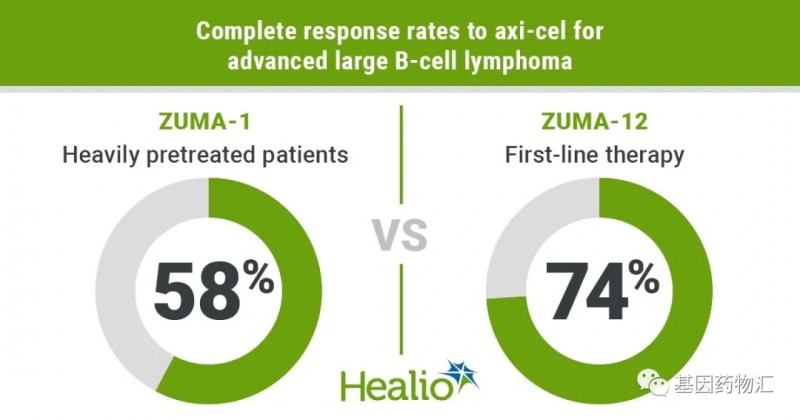
ZUMA-1试验分析了使用益基利仑赛注射液治疗经治的晚期大B细胞淋巴瘤患者的疗效。
长期生存
2020年底公布的超过4年的随访数据(51.1个月)显示,接受益基利仑赛注射液治疗的患者,中位总生存期25.8个月,4年生存率高达44%!
长期生存而不复发是癌症患者“治愈”癌症最大的希望。一般来说,临床上认为超过5年不复发的患者,复发的风险就非常非常小了。
一线疗效更出色
在另一项ZUMA-12试验中,研究者同样分析了益基利仑赛注射液一线治疗的效果。结果显示,作为一线方案时益基利仑赛注射液的疗效更加出色,治疗高危大 B细胞淋巴瘤的整体缓解率为85%,其中完全缓解率高达74%!
说完了疗效,我们也得谈谈这款新药的安全性。诚实地说,任何用于治疗癌症的药物或者方案都或多或少地会带来一些副作用。副作用并非不能承受,大部分患者也愿意忍受一些比较轻的副作用、换来更好的抗癌结果,更何况大部分副作用都是可以通过对症治疗来控制的。但一些严重的副作用是否会影响到后续的治疗、甚至导致比癌症本身更严重的伤害,是患者们最关心的问题。
安全性
作为一种与免疫相关的方案,益基利仑赛注射液治疗的副作用也比较特殊。其中最常见、也最需要重视的不良事件(黑框警告)为细胞因子释放综合征和神经毒性。
细胞因子释放综合征又被称为“细胞因子风暴”,是一系列症状的统称,因免疫细胞激活、大量释放细胞因子进入体内而导致。发生细胞因子风暴时,患者全身炎症增加、遍布各个器官,最严重时可能导致器官衰竭甚至死亡。
ZUMA-1试验中94%的患者发生了细胞因子释放综合征,其中3级或以上的比例为13%。症状发生于患者接受治疗后的第1~12天(中位数为2天),持续2~58天(中位数为7天)。
为此,研究者指出,患者应在接受治疗后每天接受相关症状和体征的监测,持续至少7天,并保证至少4周的回访。一旦发现相关症状应立刻就医,并根据病情选择支持疗法、类固醇等药物治疗。
此外,87%的患者出现了神经系统毒性,其中31%的患者为3级或以上,中位持续时间为17天。表现形式包括脑病(57%)、头痛(44%)、震颤(31%)、头晕(21%)、失语(18%)等。
抗癌"黑科技"为淋巴瘤生存困境"破局"
为了验证益基利仑赛注射液与既往标准方案之间的疗效差异,尤其是为了明确益基利仑赛注射液究竟能够为患者带来多少益处,研究者对比了SCHOLAR-1和ZUMA-1两项试验的结果。
SCHOLAR-1是一项国际性的大型回顾性分析研究,评估了曾经接受过治疗的难治性弥漫性大B细胞淋巴瘤患者,在复发后接受下一线治疗的效果。其结果显示,标准治疗方案的整体缓解率为26%,其中完全缓解率7%;患者的中位总生存期为6.3个月,2年生存率仅有20%。
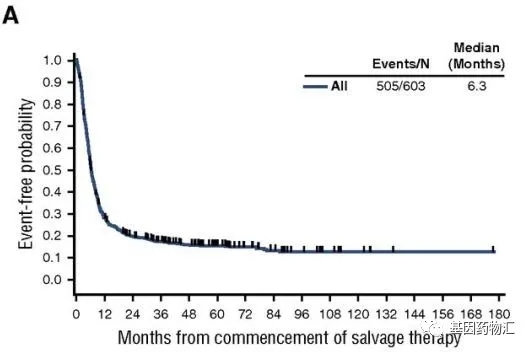
相比之下,ZUMA-1试验的结果则显示,难治性弥漫性大B细胞淋巴瘤患者接受益基利仑赛注射液治疗的整体缓解率为72%,完全缓解率54%;患者2年生存率50%!
尤其是,两项研究中患者的基线特征存在一定的差异。ZUMA-1试验中69%的患者曾经接受过3种以上既往治疗,而SCHOLAR-1中这一比例仅有23%。
益基利仑赛注射液方案显著地超越了既往标准治疗方案的疗效,为患者生存期带来了颠覆性的突破!
多靶点、多癌种CAR-T方案迎战各类癌症
除了益基利仑赛注射液,目前临床上已经取得了一定成果的CAR-T方案还有很多,广泛覆盖各类实体瘤及血液系统肿瘤,充分利用各个治疗性靶标。
胃癌CAR-Claudin18.2 T细胞疗法
Claudin18.2是一种尤其常见于胃癌的新兴治疗性标志物,阳性检出率可以接近50%~60%。目前临床上有针对这一靶点的靶向治疗药物,也有同靶点的CAR-T制剂,正在进行临床研究,且已经取得了初步的成果。
其中来自中国的CT041,在已经接受过各类标准方案治疗无效的转移性腺癌(包括胃癌及胰腺癌)中,取得了33.3%的临床缓解率。
目前这款产品的下一阶段临床试验正在招募国内患者,有需求的患者可以联系全球肿瘤医生网医学部了解详情或进行申请。
肝癌CAR-GPC3 T细胞疗法
GPC3驱动的肝癌,大约占所有肝癌的70%(在鳞状非小细胞肺癌中也占到了63%)。对于一种治疗性靶标来说,这样高的比例几乎意味着,针对这一靶标的药物或疗法一旦成功上市,必定会彻底颠覆原有的标准治疗格局。
一款由我国科济生物研发的CAR-GPC3 T细胞疗法治疗肝癌该患者,6个月生存率为50.3%,1年生存率为42.0%,3年生存率仍然有10.5%。
目前这款产品的下一阶段临床试验正在招募国内患者,有需求的患者可以联系全球肿瘤医生网医学部了解详情或进行申请。
淋巴瘤CAR-CD20 T细胞疗法
CD20的全称是B淋巴细胞抗原CD20,是一种在B细胞表面表达的抗原,同样也是各类B细胞淋巴瘤重要的治疗性靶标。
针对这一靶标的CAR-T疗法中,MB-106治疗慢性淋巴细胞白血病的整体缓解率高达92%,其中完全缓解率达到58%;治疗滤泡性淋巴瘤整体缓解率89%,其中完全缓解率为67%。
针对同一靶标的国研CAR-T项目也在紧锣密鼓地进行着临床试验,如MRG001、LUCAR-20S等,均在招募各类非霍奇金淋巴瘤患者。有需求的患者,或希望参与任何临床试验项目的患者,可以联系全球肿瘤医生网医学部(400-666-7998)进行申请。
不同癌症、不同靶标,精准施治、个性化治疗
除了上述几种以外,基于不同类型癌症的特点,研究者还有针对性地研究了其它各类新CAR-T制剂,例如用于治疗T细胞淋巴瘤的CAR-CD4 T细胞疗法,用于治疗卵巢癌、间皮瘤、胰腺癌、肺癌等的CAR-MSLN T细胞疗法,用于治疗肺癌、结肠癌、胃癌、乳腺癌、胰腺癌等的CAR-CEA T细胞疗法,用于治疗神经胶质瘤、头颈部肿瘤的CAR-EGFR T细胞疗法等等。
目前的CAR-T细胞临床试验已经广泛覆盖超过16类癌症,有需求的患者都可以联系医学部详细咨询。
关于CAR-T方案进一步推广的思考
作为一种新兴的治疗方案,CAR-T疗法从问世到上市,在疗效广受认可的同时,也面对了许多矛盾与争议,其中最大的争议来自价格。
在美国,Yescarta(益基利仑赛注射液)治疗一疗程的价格大约是37.3万美元。与远超常规方案的疗效相对应的,是远超常规的高价。
这显然是一个国内患者难以承受的价格。而此次益基利仑赛注射液中国获批之后,国内价格尚未公布,但已经有了两种声音:一种来自业内人士,表示国内CAR-T上市初期与国外的定价不会有太大的差异;另一种声音来自部分专家,认为国内的定价必须符合国内市场,照搬国外定价只会将绝大多数患者拒之门外,让这种新方案无法发挥应有的价值。
事实上,国外的专家也就CAR-T的价格问题产生过许多争议。其中最大的争议点在于,新疗法的价格是否会导致比贫富差距更大的不平衡。
“所有的癌症专科医生都希望有一种方案,能够治好患者的疾病且永远都不复发。”来自希望之城的细胞免疫治疗中心T细胞疗法研究实验室的主任Stephen J. Forman博士表示。他认为,目前为止CAR-T疗法已经展现出了“根治性”的潜力,能够并为患者带来持久的、稳定的无癌生存。
既然有如此强大的潜力,那么CAR-T疗法的推广就是有价值的。但如何突破价格的壁垒、让更多患者有机会用上这种疗效出众的新兴治疗手段,甚至在这种疗法进一步普及之后,是否能够将其提升至一线,是下一阶段亟待解决的问题。
我们相信,随着抗癌科技的发展,免疫疗法、细胞免疫疗法一定能够逐步普及,价格降低、甚至纳入医保范围,让更多患者有用上疗效更好的治疗方案的机会。
当然,现阶段癌症患者还可以选择参与临床试验,借着这个新药井喷的“浪潮”,抢先体验这些新一代的治疗方案。







































 首页
首页 咨询
咨询 方舟新药
方舟新药 营养商城
营养商城