不同腹水的诊断方式对比,腹水的危害有哪些,癌性腹水怎么治疗、如何治疗,恶性腹水的治疗方法,治疗腹水的药物有哪些
癌性腹水,又叫恶性腹水,这是一个许多癌症患者在晚期、终末期都会经历的症状。我国现存癌症患者数量近1800万,其中合并腹腔转移或已经发生了恶性胸水、腹水的患者,占比接近20%。
虽然只是一种因癌症而导致的症状,但是和大部分的癌症很相似,腹水的早期发现难度比较大。再加上腹水的治疗难度不小,症状的发展和癌症的进展息息相关,许多患者,都在治疗的某个阶段面对严重的腹水症状束手无策了。
恶性腹水该怎么治疗?千万别等到患者都痛苦难忍了才着急治!
如何发现腹水?几种诊断方式各有利弊
等患者自己提出腹部胀痛难忍、呼吸困难,或者等医生发现患者的腹部已经状如蛙腹,才开始考虑怎么治疗腹水的事情,显然是有点晚了。通常来说,临床上与腹水相关的检查项目包括这么几种:
1、问诊/体格检查
患者自述不适:1500 mL以上
移动性浊音阳性:1000 mL以上
液波震颤阳性:3000~4000 mL以上
如果患者能够在对自身的症状的表述当中提出与腹水相关的不适症状,意味着患者体内的腹水量已经到了1500 mL以上;如果通过医生的检查,发现患者存在移动性浊音阳性(这是一种腹部叩诊),意味着患者体内的腹水量已经到了1000 mL以上;另一项体格检查,液波震颤阳性则代表患者的腹水量已经高达3000~4000 mL以上。
以腹水的标准200 mL以上来论,这三种检查手段显然不能敏锐而早期地发现腹水。而临床上另一种诊断腹水的常用检测方式,就是各类影像学检查。
2、影像学检查
彩超/CT:300 mL以上,可以用于鉴别不同类型的腹水
不论是彩超还是CT,都能在腹水只有300 mL以上的情况下诊断出腹水,且可以用于鉴别不同类型、不同病因导致的腹水。存在腹水高风险的癌症患者,应当在必要的情况下完善这些检查。
3、实验室检查
腹腔穿刺液的检查可以用于鉴别腹水的性质以及成因;血液、尿液检查也可以用于评估患者的肝功能、肾功能,协助疾病的诊断,以及患者病情的评估。
那么,哪些癌症更容易诱发腹水呢?
哪些患者应当警惕腹水?这种癌症发生腹水的风险接近100%
腹水的成因很多,对于因癌症而引发的腹水,主要包括这么几类的情况。
第一,癌细胞侵犯至腹膜,因血管内皮生长因子(VEGF)表达升高等原因,导致腹膜上的毛细血管通透性增加,液体渗入腹腔形成腹水。
第二,癌细胞侵犯至肝脏,导致患者肝脏功能紊乱,进而产生腹水;若患者血液中游离的癌细胞增多,导致肝脏静脉压力上升,也可能导致腹水;严重时,患者肝脏内癌症病灶破裂,可能导致血性腹水。
第三,若癌细胞转移至淋巴,堵塞淋巴管,也会导致腹水。
基于这样的特点,我们不难看出,原发部位位于腹腔内的、存在或容易发生腹膜转移的、存在或容易发生肝转移的、转移期血液内游离癌细胞较多的、以及侵犯了相关淋巴结等的癌症,患者出现恶性腹水的风险更高。
例如,卵巢癌(30%~60%)、腹膜癌(接近100%)、胃癌(10%)、肝癌(35%)以及胰腺癌和肠道肿瘤等,都属于癌性腹水发生风险高的癌症类型。这部分患者,以及其它的晚期和转移性癌症的患者,都应该关注自身的症状,必要时进行相关的检查。
发生癌性腹水之后,该如何治疗
临床上对于腹水的治疗,主要分为两个部分:一方面是对症治疗,针对腹水的症状进行治疗,缓解患者的痛苦;一方面是对因治疗,通过控制导致腹水的疾病,减少腹水的产生。
癌性腹水是患者的疾病发展至晚期的标志之一,也是影响晚期患者生活质量的主要因素之一。其治疗的主要目的是在不引起血管内容量不足的情况下,控制积液量、缓解患者呼吸困难及疼痛,进而延长患者生存期、提高生活质量。但如果处理不当,甚至可能造成感染乃至循环衰竭等严重并发症,危及患者生命。
1、引流
引流是癌性腹水最主要的局部外科治疗手段之一,也是最直接、最快捷解决腹水带来的痛苦的方法,主要分为穿刺抽液引流和留置引流管引流两种方式。
当大量液体影响患者的呼吸,或者患者腹胀症状非常严重、疼痛难以忍受的时候,可以采取引流的方式,快速缓解患者的痛苦。
引流也分为穿刺以及置管,一般来说,需要反复引流,又没法接受腹腔静脉分流术等手术的患者,可以考虑置管引流。
但单纯采用抽液治疗仅改善症状,并不能控制患者疾病,通常会在1~3天内复发,治标不治本。且反复抽液或长期引流会导致患者蛋白质大量流失,同时增加腔内感染或气胸等其它并发症的风险,因此必须配合其它治疗手段,对患者疾病进行控制或治疗。
如果患者疼得受不了,或者已经“上不来气儿”,当然可以抽液(引流)。但是这个方法不能经常用,一次也不能抽太多,否则还可能导致一系列更严重的并发症,比如蛋白质大量流失,也比如腔内感染。
但从这种治疗的结果上来说,一旦引流过一次,患者就很难再忍受大量腹水蓄积压迫的痛苦了,不得不反复频繁引流。因此这就像是一种有“成瘾性”的治疗手段,患者对于这种手段产生了生理和心理上的依赖。
至于实际治疗中该不该用,得由主治医生、患者和患者家属商量着来。
2、利尿剂
利尿剂直接作用于肾脏,通过抑制肾小管对于水、钠的重吸收,促进电解质与水的排泄,使尿量增多。钠的排泄量增加,血管内外达到负钠平衡,能够减少患者的腹水量。
但利尿剂并非一定能缓解患者的症状,根据文献报道,利尿剂治疗恶性腹水的缓解率仅约44%左右。
使用利尿剂常见的不良反应包括低钠血症、低钾血症、高尿酸血症等,因此在治疗过程中必须重点关注患者的电解质和尿素水平,避免发生电解质紊乱。部分药物可能造成肝毒性,不适用于部分晚期肝癌患者。
3、胸腹腔内药物治疗
胸腹腔内药物治疗包括化疗、硬化剂、生物制剂治疗等。在治疗方式方面,如热灌注化疗(当然也包括热疗)等手段也能够提升局部药物治疗的疗效。
化疗是晚期癌症最重要的治疗手段之一,同样也是癌性胸腹水患者不可或缺的治疗方式。与全身用药的方案相比,局部注射的化疗方案能够更有针对性地提高患者局部的药物浓度,在增强疗效的同时减轻毒性反应。通过杀伤癌细胞、控制癌症的发展,可以减少胸腹水的生成,因此与利尿剂治疗和局部引流等方式相比,胸腹腔内化疗更具备“治本”的效果。
局部化疗的药物通常应根据患者的原发病灶类型及药物敏感性综合考虑决定。目前临床上常用的化疗药物包括顺铂、卡铂、奥沙利铂、紫杉醇、表柔比星等,其缓解率通常在40%~60%左右,患者的治疗需求仍高度未满足。
近几年,用于治疗腹水的新药也受到了许多重视。新的化疗药物、针对一些腹水中癌细胞上常见的靶标的单克隆抗体药物,以及细胞类的药物,都有或多或少的进展。
用于治疗腹水的靶向或免疫手段有哪些
其实对于腹水特别严重的患者,使用靶向药物进行治疗是需要反复斟酌的。许多靶向治疗药物依靠肝肾代谢,可能导致肝损伤或肾损伤,因此腹水本来就可能是部分癌症患者接受靶向治疗后的副作用。
但通过专家们不断的研究,仍然有一些对于腹水治疗颇有益处的靶标被发现,并且在靶向和免疫治疗当中得到了利用。
我们列举两类比较有代表性的新兴腹水治疗方案。
1、EpCAM+CD3,靶向+免疫"双抗"
既然要用精准治疗的手段来治疗腹水,那么最重要一点自然是,找到合适的靶标。
人上皮细胞粘附分子(EpCAM)是一种Ⅰ型跨膜糖蛋白,会表达于正常体细胞上,但在正常情况下被一些特殊的机制屏蔽了功能,不会发挥作用。在一部分类型的癌细胞(如卵巢癌、胃癌、结肠癌、胰腺癌、前列腺癌、肺癌和子宫内膜癌细胞)的表面,多至覆盖整个细胞,是常见的表达最强的肿瘤相关抗原之一。
大家可以参考Claudin 18.2这个胃癌的“新星”靶点来理解EpCAM在癌细胞中的异常表达和其作为靶向治疗药物靶标的机理。
引起恶性腹水的上皮癌细胞中,EpCAM的表达普遍上调;但人体正常的腹腔内层为间皮起源,EpCAM的表达很低。这样的表达差异使EpCAM成为了一个用于治疗恶性腹水的良好靶标,一些腹腔注射的靶向药物治疗恶性腹水的理论基础正是基于此。
除此以外,CD3是一个大家都比较熟悉的免疫检查点,位于T细胞表面,能够激活T细胞的免疫功能。
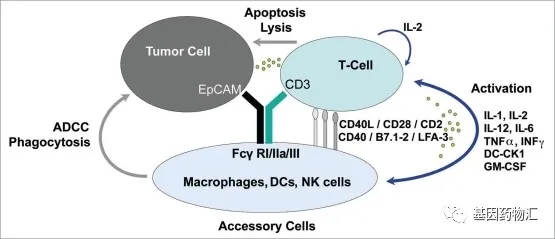
以EpCAM和CD3为靶标的双靶点药物(“双抗”),历史上最著名的一款,正是世界上首款获批的“双抗”卡妥索单抗(Catumaxomab)。
"双抗"时代的开创者:卡妥索单抗
卡妥索单抗(Catumaxomab)首次于21世纪初问世于德国,是首个获得正式批准的“双抗”药物。以现在的眼光来看,“双抗”绝对是免疫治疗发展的最重要的方向之一,卡妥索单抗的研究者在二十余年前、免疫治疗刚刚开始起步的年代就踏上了这个方向,并且取得了成熟的研究成果,显然是具有跨时代意义的。
以现在的眼光来看,卡妥索单抗在既往临床试验中展现出的疗效并不差,对于发生了癌性腹水(又称恶性腹水)、尤其是因胃癌而导致的腹水的患者,治疗效果甚至称得上是比较出色的。
一项发布于2011年ASCO大会上的Ⅰ/Ⅱ期临床试验中,研究者分析了卡妥索单抗腹腔注射联合穿刺,以及仅使用穿刺抽取腹水的疗效。
结果显示,联合了卡妥索单抗治疗的患者,6个月生存率为28.9%,显著超过了仅使用穿刺的患者的6.7%,患者生存期显著延长。
在RLC>13%的患者中,卡妥索单抗治疗的获益更加显著。联合卡妥索单抗治疗的患者6个月生存率37.0%,显著超过了仅使用穿刺的患者的5.2%。
我们查阅了当时的文献发现,卡妥索单抗的临床试验项目很多,主要以各类腹腔内肿瘤或腹腔转移肿瘤、腹水的治疗为主,包括了胃癌、卵巢癌、上皮性肿瘤引起的恶性腹水等等。
但在卡妥索单抗刚刚问世的时候主流思想还认为,通过激活人体自身免疫能力来抗癌、延长患者生存期,是一件不可能做到的事情。这款具有跨时代意义的新药,在上市之后的多年间备受冷落,几经转手,最终于2017年因经营问题遗憾退市,让人不得不感叹一句“生不逢时”。
不过如今,免疫治疗与“双抗”的价值得到了更充分的重视,原本被视为“不可能做到”的事情,也成为了可能(比如PD-1抑制剂的成功)。卡妥索单抗开启了新的临床试验,为返回市场做出努力,同靶点的其它药物也纷纷问世,临床试验开始招募患者。
而在癌症治疗蓬勃发展的今日,许多与卡妥索单抗同靶点的药物也加入到了腹水这个适应症的“战场”之中。今非昔比,对于腹水这个因癌症导致的症状的治疗,如今的我们投入了更多的关注。
我国自主研发的同靶点药物M701,近期公开了Ⅰ期试验中期数据。在已经完成数据收集的23例患者当中,所有治疗相关的不良事件发生率为82.6%,其中3级或以上严重不良事件发生率为21.7%。
最常见的所有等级不良事件包括低蛋白血症(34.8%)、贫血(26.1%)、低钾血症(17.4%)、低钠血症(17.4%);3级或以上严重不良事件中最常见的包括贫血(8.7%)、低钾血症(4.3%)、高血糖(4.3%)。
缓解率方面,在16例可评估的患者当中,腹水的临床缓解率为62.5%,控制率为100%;包括了3例完全缓解、7例部分缓解和6例疾病稳定。患者的中位总生存期为152天,其中卵巢癌患者的中位总生存期为148天,胃癌患者为209天。
目前这款药物的后续试验正在招募患者,腹水患者可以联系基因药物汇-临床新药招募中心了解招募详情,或将病历资料及联系方式发送至招募中心邮箱(doctorjona0404@gmail.com)进行申请。
2、TILs
TILs是肿瘤浸润性淋巴细胞的缩写,指一类能够向肿瘤组织迁移的淋巴细胞。与普通的淋巴细胞相比,这些细胞对癌细胞的识别能力更强,距离“杀伤癌细胞”的目标更近一步。
单一机构的研究显示,从肿瘤病灶分离出的淋巴细胞中有超过60%能够识别癌细胞,而从血液中分离出的淋巴细胞,能够有效识别癌细胞的比例不到0.5%。
但癌细胞及肿瘤病灶内存在一些特殊的机制及环境,抑制了这部分淋巴细胞的杀伤功能。在大多数的病灶内,即使已经有一部分淋巴细胞成功地“深入敌营”,也不能组织起对癌细胞真正有效的攻击。
采用从胸腹水中分离出的淋巴细胞进行扩增与培养,并使用这些细胞进行治疗,得到的疗效显著超过从血液中提取的淋巴细胞。
从胸腹水中分离的淋巴细胞并进行扩增的成功率较高,因此通过TILs治疗的成功案例也比较多。这些试验多为单机构小型试验,取得了比较好的结果。
一项2017年公开的研究中,分析了13例胸腹水患者,在接受穿刺术引流后,分别接受TILs治疗或顺铂治疗的疗效。结果显示,TILs治疗的整体缓解率为33.33%,疾病控制率为83.33%;相比之下,顺铂治疗的患者的整体缓解率为28.57%和71.43%。
目前,多项TILs疗法临床试验正在招募患者,大家可以咨询招募中心了解详情。
除了治疗,患者还要关注哪些调养
除了各种治疗手段,癌症患者还应该在医生的指导下选择一些能够辅助改善健康水平的食物,或者部分情况下还需要使用一些药物。
前文中我们说过,腹水的产生必定伴随着患者体内大量的有益的蛋白质的流失。这种时候,患者必须要增加每日饮食中高质量蛋白质的摄入。对于一些胸腹水严重、身体状况极差的患者,也应当在医生指导下考虑补充白蛋白等。
除此以外,患者还应该严格控制钠盐的摄入量,其次是必须限制水的摄入量。低盐饮食的目的在于尽可能多地将体内多余的水经肾脏排出体外,限制入量则是能够尽可能地减少腹水的产生——一方面减少产生,一方面增加排出,这样才能尽快清除腹水。
讲到这方面的时候,小汇认识的一位医生拉着小汇的手,痛心疾首道:千万不要因为患者渴就放任他喝水,尤其是还偷偷喝,喝完了也不告诉我们。千万不要!
如果大家想结合自己的病情、了解更多关于营养补充的知识,也可以联系招募中心详细咨询。
积极配合治疗,才能减轻痛苦、延长生存期
总得来说,尽管有各种各样的全身及局部治疗方案,癌性胸腹水的治疗仍然是临床上一个亟待深入研究的重点方向。
当然,不论采用何种方案,患者积极配合治疗才是发挥出最好的治疗效果的关键。希望每位患者都能找到更适合自己的治疗方式,减轻痛苦、延长生存期!







































 首页
首页 咨询
咨询 方舟新药
方舟新药 营养商城
营养商城