CAR-T疗法突破5大难点,抗癌效果翻倍,CART细胞治疗实体瘤有戏了,更多的CAR-T临床试验招募正在进行中
细胞免疫疗法
免疫疗法已然成为人类对抗癌症新的希望,而CAR-T疗法则是近年来最有前景的肿瘤免疫疗法之一。这项技术在治疗各种恶性肿瘤方面取得了巨大进展,已成功应用于多种血液恶性肿瘤的治疗。
特别是今年我国正式开启细胞免疫治疗元年,分别于6月份迎来首款CAR-T疗法——阿基仑赛注射液;9月3日,迎来第二款获批的CAR-T产品——瑞基奥仑赛注射液,这也是中国首款1类生物制品的CAR-T产品。
根据Clinical Trials.gov提供的数据,截至2021年4月,共有1358项活跃状态的细胞治疗试验;与2019年~2020年24%的增长相比,2020年至2021年增长了43%。这一增长的大部分是由于CAR-T细胞临床试验,其自2019年更新以来增加了83%,以及更多试验测试了其他细胞疗法、TCR-T细胞疗法和TIL细胞疗法。而NK/NKT细胞的试验数量下降,尚未完全恢复。
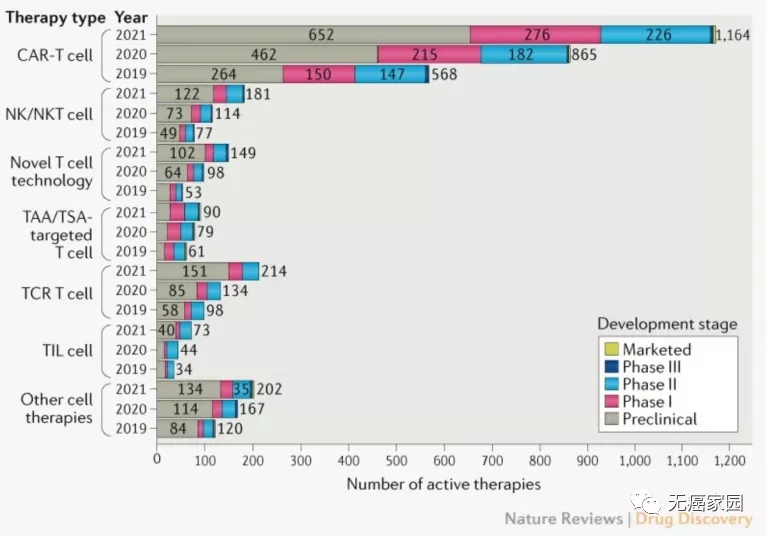
然而值得一提的是,以上大多数试验依然是集中在血液肿瘤(非实体瘤)领域,在广阔的实体瘤领域依然困难重重,而实体瘤才是抗癌的“主战场”。如2021年最新的全球癌症数据指出,约90%的癌症发病率都是由实体瘤引起,但关于实体瘤的细胞治疗临床试验却很少(实体瘤占40%,且大部分处于早期阶段)。由此可见,实体瘤仍然是细胞免疫治疗的难点。
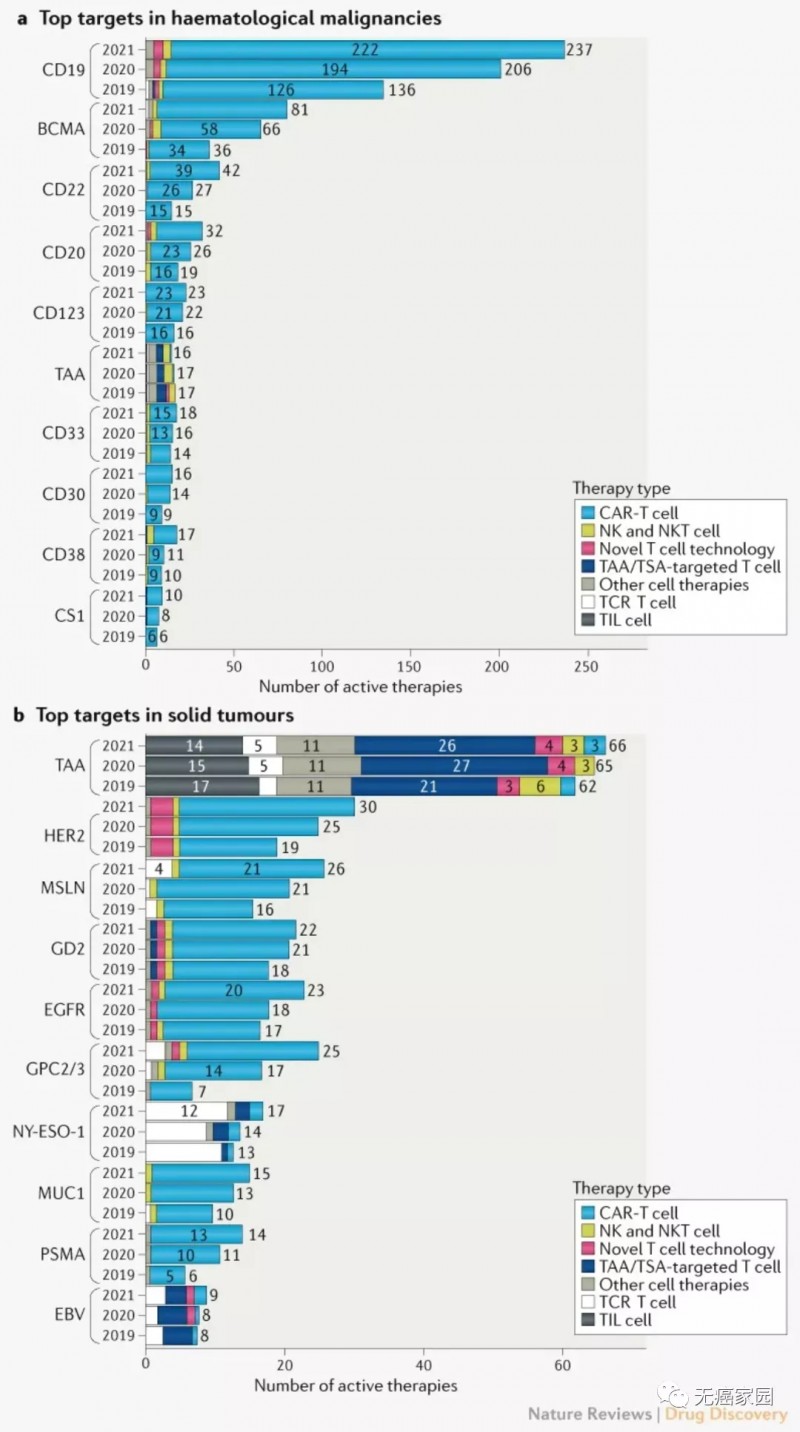
a为血液肿瘤的细胞治疗靶点;b为实体瘤的细胞治疗靶点
面临五大"困境",CAR-T攻克实体瘤任重道远
CAR-T治疗在实体瘤上的临床疗效差强人意。究其原因,主要在于实体瘤的细胞疗法存在不少难点,主要面临以下几大“困境”:
缺乏独特的肿瘤相关抗原作为CAR-T靶点
血液肿瘤的靶点大多单一且具有特异性不同,以2021年最新的全球癌症数据为例,主要集中在CD19、CD20、CD22、BCMA等靶点。
而实体瘤的肿瘤特异性抗原(TSA)很少,目前发现的肿瘤高表达的抗原多为肿瘤相关抗原(TAA),在正常组织中均有表达,这就表明会有脱靶的风险,脱靶风险高的话不仅安全性成问题,也会导致癌症的复发,病情反复难愈。
不同类型实体瘤的异质性大
实体瘤中用于CAR-T细胞疗法的抗原为肿瘤特异性抗原(TSA),如EGFRvIII、前列腺癌抗原PSA、黑色素瘤相关突变抗原1(MUM1)等,这些抗原虽然在肿瘤细胞中高表达,但是在同种肿瘤类型的不同患者身上却具有高度异质性,从而限制CAR-T的疗效。
T细胞无法有效归巢到肿瘤部位
一些实体瘤会抑制某些趋化因子的分泌。趋化因子与其受体的相互作用会促进T细胞向肿瘤微环境的迁移。同时,CAR-T细胞表面也缺乏与实体瘤分泌的趋化因子相匹配的相关受体,造成CAR-T对肿瘤部位的归巢能力差。
T细胞衰竭作为一种免疫细胞,T细胞帮助对抗感染和疾病,如癌症。但是据多项临床试验显示,CAR-T细胞疗法的效果会随着时间的推移而减弱。T细胞会出现衰竭,当这种情况发生时,免疫系统的抗癌反应会受到限制。T细胞的衰竭很可能在哪些CAR-T细胞失败案例中起主要作用。在肿瘤内,来源于患者并且用于CAR-T生产的细胞、以及回输给患者的CAR-T细胞中,均能在不同程度上检测到T细胞衰竭状态。
肿瘤内复杂的微环境对免疫有抑制作用
CAR-T细胞在实体瘤中的疗效受到限制,部分原因是免疫抑制性肿瘤微环境。实体瘤中复杂的肿瘤微环境,有利于具有物理屏障、多种免疫抑制机制及多种生化因素的肿瘤进展,导致CAR-T细胞疗法在癌症患者临床试验中的疗效有限。
在对抗实体瘤的道路上CAR-T面临多重困境,下面针对上述机制总结了目前CAR-T在实体瘤中的一些新突破。
基于特定肿瘤微环境选择合适靶点的方法
为了攻克实体瘤这一艰巨的目标,国内外的学者针对CAR-T进行了多种改造,不断地发现新靶点,以用于治疗多种实体肿瘤。
随着针对实体瘤的CAR-T治疗的临床试验数量不断增加,现对这些试验进行总结,以探索基于特定肿瘤微环境选择合适靶点的方法。如下图为针对不同的癌症的抗原分类。
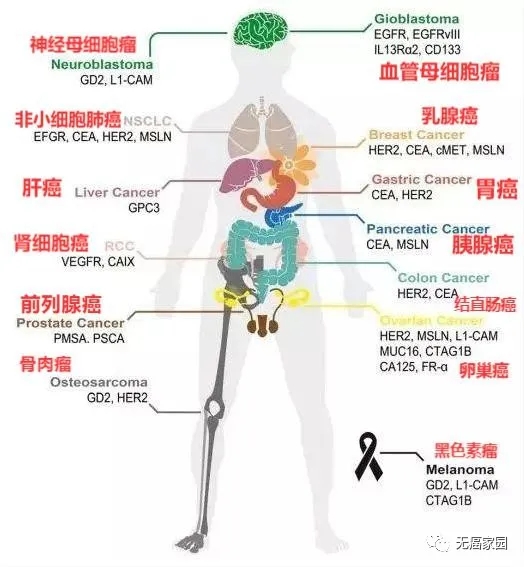
不同癌症的CAR-T靶点分类
目前,无癌家园也有多款实体瘤的CAR-T临床试验正在进行招募,有意向者可咨询医学部400-626-9916具体评估病情!
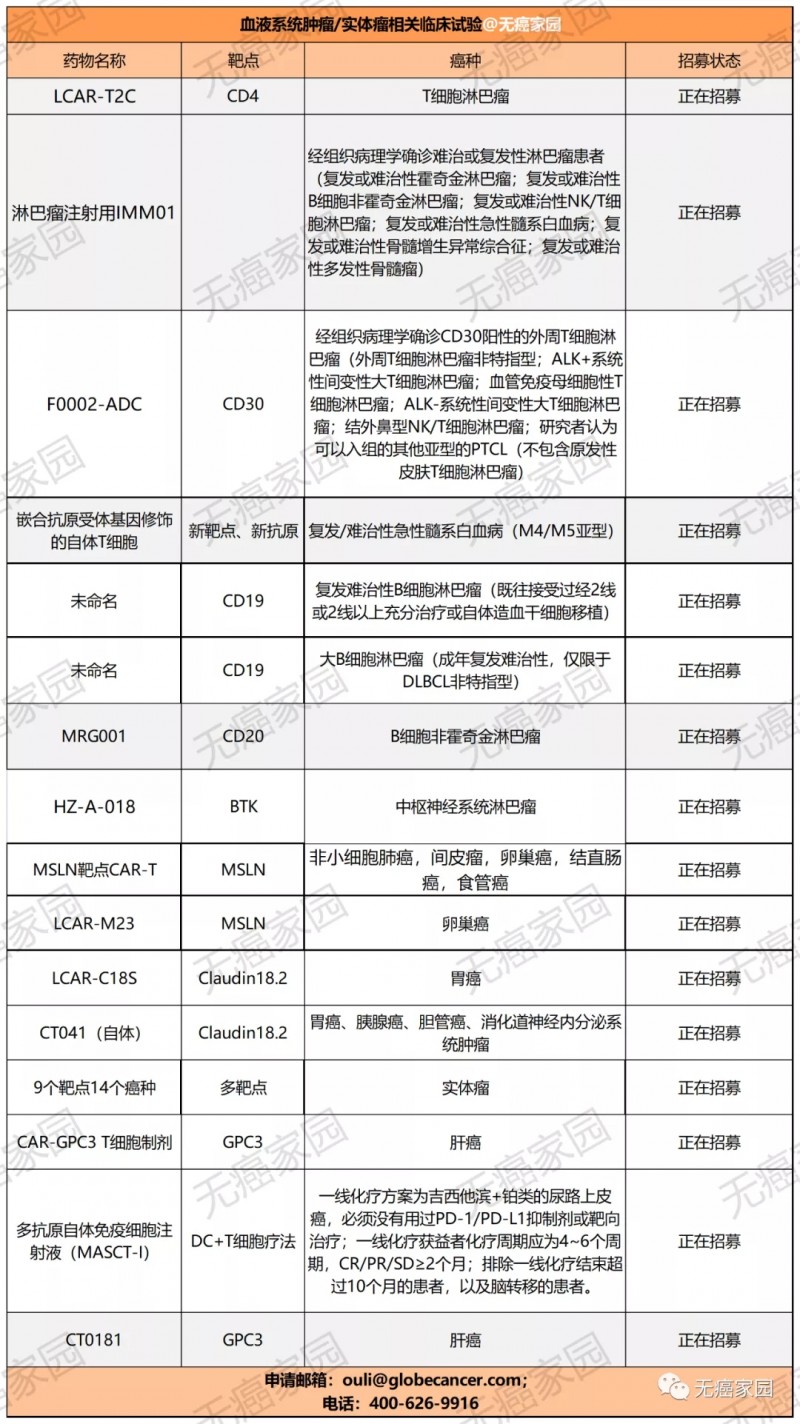
接下来,无癌家园的小编就给大家一一回顾下CAR-T疗法在各癌种中颇为出圈的临床研究,希望为各位癌友们提供新的治疗选择。
CAR-T疗法治疗胃癌及胰腺癌
9月16~21日召开的欧洲肿瘤内科学会(ESMO)年会上,由科济药业开发的靶向Claudin18.2(CLDN18.2)自体CAR-T候选产品CT041展现了其在消化系统肿瘤中的突出疗效,可谓是大放异彩!
Claudin18.2(CLDN18.2)是一种胃特异性膜蛋白,被认为是胃癌和其他癌症类型的潜在治疗靶点。基于此,中国研究人员开发了国际上首个针对 Claudin18.2的CAR-T细胞。
截止到2021年4月8日,纳入的37例CLDN18.2表达阳性的晚期消化道肿瘤患者,其中包括28例胃癌/胃食管结合部癌、5例胰腺癌和4例其他类型的实体瘤,约84%的患者既往接受过至少2线治疗,中位转移器官数量为3个。
研究数据颇为亮眼
1)总疗效:所有患者的客观缓解率达48.6%,疾病控制率达73%;所有胃癌患者总客观缓解率为57.1%。
2)既往接受至少2线治疗失败的胃癌患者:客观缓解率为61.1%,疾病控制率为83.3%。
3)28例胃癌/胃食管结合部癌各亚组:在既往PD-(L)1抑制剂治疗失败、存在腹膜转移、印戒细胞癌等预后差且已无有效治疗手段的患者中,客观缓解率均可维持在50%或以上。
4)安全性:CT041总体耐受性良好,未发生治疗相关死亡或免疫细胞治疗相关神经系统毒性综合征(ICANS)。
除了CT041目前正在开展临床试验外,另外一款针对既往接受过胃全切除术/胃大部切除术后的复发或转移性晚期胃腺癌(包括胃食管结合部腺癌)的靶向Claudin18.2 的CAR-T细胞制剂,名为LCAR-C18S也在临床招募中。
CAR-T疗法治疗肝癌
今年ASCO年会上我国医学研究者们首次公布了靶向GPC3的CAR-T药物(Ori-CAR-001)治疗复发/难治性肝细胞癌的最新临床研究数据。该研究的初步数据显示,Ori-CAR-001在GPC3阳性复发/难治性患者中表现出良好安全性和有效性。
截至2021年3月10日,共纳入11名接受细胞输注的复发受试者。所有受试者均患有晚期肝细胞癌,并且经过化疗、TACE(肝动脉化疗栓塞术)和靶向治疗均无效。9例可评估受试者中,4例达到部分缓解 (PR),3例达到疾病稳定 (SD),2例出现疾病进展 (PD),客观缓解率为44%,疾病控制率达到78%。
在7月29日的国际知名杂志《Journal of Hematology & Oncology》刊登了我国医学研究者们的一项成功改造CAR-T技术的临床研究,研究中提及的CAR-T产品选择的靶点是glypican-3(GPC3)和mesothelin(MSLN)中,报道的治疗结果格外令人惊艳!
其中1例晚期肝癌患者接受了瘤内注射CAR-T治疗,治疗后肝脏病灶代谢基本消失。
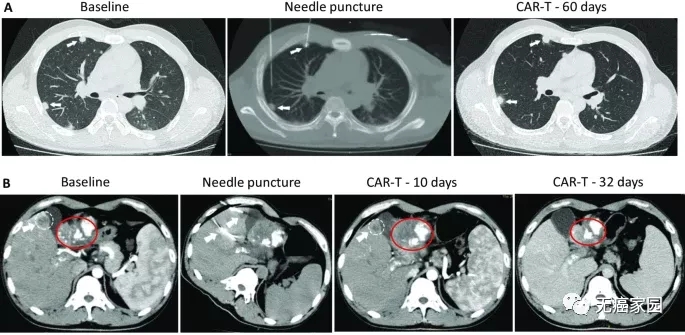
注射60天后,虽然2个肺部结节的尺寸无显著改变;但在第10天时肝脏肿瘤病变显著收缩,注射第32天后则完全消失
更绝的是1例晚期胰腺癌患者,接受的是静脉回输的CAR-T治疗,治疗后全身的病灶,基本都实现了代谢活性完全消失。
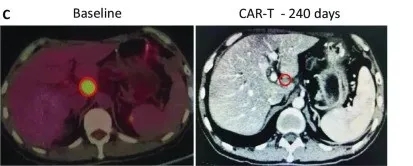
在治疗240天后达到完全缓解,未见其他肿大的淋巴结,患者病灶完全消失
除了上述小编提到的热门靶点外,还有很多治疗靶点,特整理如图所示。
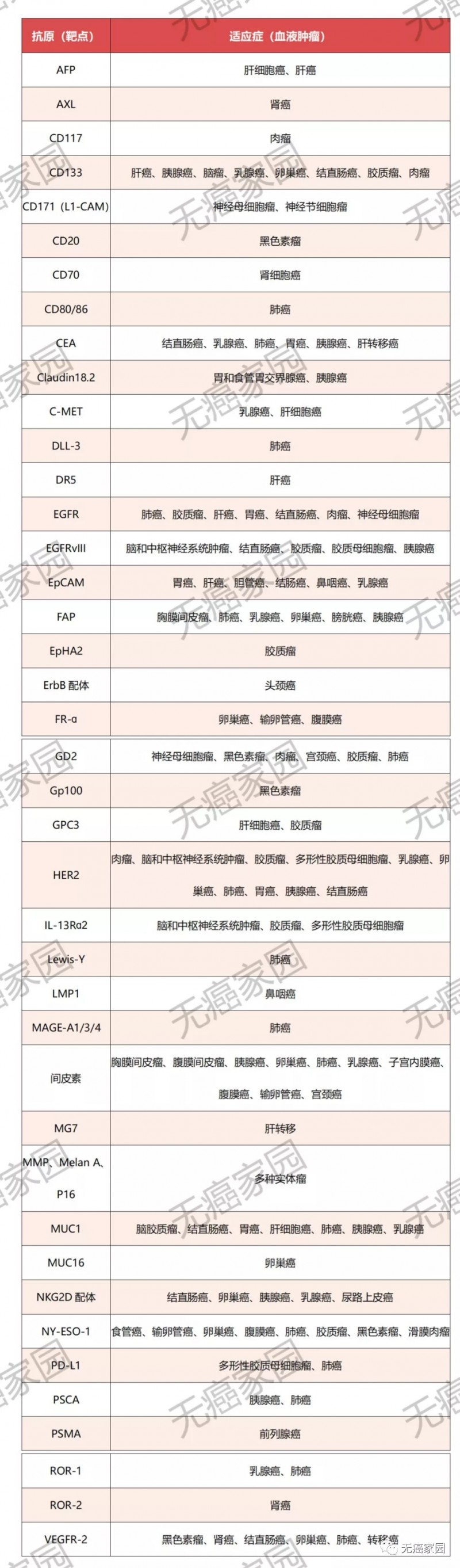
改善T细胞的浸润和转运
治疗血液肿瘤时CAR-T通常采用静脉回输,在实体瘤中,为改善CAR-T的浸润和转运难题,可采用瘤内给药的方式。瘤内给药方式在胸膜恶性间皮瘤、头颈癌和恶性胶质瘤的研究中都得到了较好的效果。
抗癌效果翻4倍,CAR-T疗法可消除多种实体瘤并预防复发
在2018年3月5日,CAR-T领域迎来一项重磅研究进展。国外的研究团队成功地开发出新一代CAR-T,通过白介素7(IL-7)和趋化因子CCL19基因转入CAR-T细胞制备出能够有效杀伤肿瘤的“超级CAR-T细胞”,能够让患有肿瘤的小鼠几乎100%生存!

这种细胞在体内存活时间更长并且能够有效地帮助树突细胞以及T细胞浸润到肿瘤组织内部一起杀伤肿瘤。
研究人员将这种超级CAR-T细胞称为“7×19CAR-T”,就是在常规CAR-T基础上进行改造,使常规CAR-T可以表达IL-7和CCL19两种趋化因子。
在多种实体瘤小鼠模型中,研究结果证实,全新CAR-T治疗实体瘤的效果是目前常规CAR-T的至少4倍,对于那些常规CAR-T几乎无效的实体瘤,新一代CAR-T也能实现肿瘤的完全消除。更重要的是,全新一代CAR-T还解决了常规CAR-T治疗后易复发的难题。即使在新一代CAR-T消除实体瘤100天之后,再次接种癌细胞,这些癌细胞也无法生长出肿瘤。
改造特殊CAR-T技术,让晚期肝癌、胰腺癌病灶通通消失
上述的临床前实验的设想有幸在人体中得到实现!针对CAR-T细胞进入肿瘤组织困难、CAR-T细胞进入肿瘤组织后容易被其他免疫抑制性的分子或细胞所阻挡无法发挥作用等问题,我国的医学研究者想到的办法是让CAR-T细胞同时分泌细胞因子和趋化因子。这些因子好比给CAR-T细胞配置了一个自带的能量马达,能够增强CAR-T细胞进入肿瘤内部的能力。
就在7月29日,国际知名杂志《Journal of Hematology & Oncology》刊登了我国医学研究者们的一项成功改造CAR-T技术的临床研究,研究中提及的CAR-T产品选择的靶点是glypican-3(GPC3,主要是肝癌)和mesothelin(MSLN,又称为间皮素,可以应用于多种上皮癌症,比如恶性间皮瘤、胰腺癌、胃癌、卵巢癌等),为了使CAR-T细胞具有更强的进入肿瘤内部的能力,研究人员特地加装了白介素7(IL-7)和趋化因子CCL19。
此次研究纳入的是6例具有GPC3或MSLN表达的晚期肝细胞癌(HCC)、胰腺癌(PC)和卵巢癌(OC)患者。治疗结果格外令人惊艳!
其中1例晚期肝癌患者接受了瘤内注射CAR-T治疗,治疗后肝脏病灶代谢基本消失。
更绝的是1例晚期胰腺癌患者,接受的是静脉回输的CAR-T治疗,治疗后全身的病灶,基本都实现了代谢活性完全消失。
国研引领CAR-T新技术,覆盖多个实体瘤领域,收效颇丰
即使CAR-T疗法治疗实体瘤的道路很艰难,但是我国的医学研究者并不气馁。国内研究机构致力于通过开发创新型的CAR-T疗法根治实体瘤,甚至为了解决实体瘤治疗的种种困难和挑战,自主开发出了治疗实体瘤的CoupledCAR™平台技术,并已在临床研究中取得了良好的疗效。
2020年5月,第23届美国基因与细胞治疗学会(ASGCT)年会上,我国细胞研究机构发布了关于CoupledCAR® CAR-T技术在实体瘤治疗中显示出的良好疗效及安全性。两名甲状腺癌和两名结直肠癌患者在CART细胞回输后均达到了部分缓解(PR)。
2020年11月10日,第62届美国血液学会(ASH)年会上,我国细胞研究机构描述了两个经过大量预处理的结直肠癌和甲状腺癌患者组。7 名结直肠癌患者组接受抗 GCC(鸟苷酸环化酶 2C) CoupledCAR® CAR-T细胞治疗,而3名甲状腺癌患者组接受抗TSHR(促甲状腺激素受体) CoupledCAR® CAR-T治疗细胞。在两组中,CoupledCAR® CAR-T 细胞在体内均表现出快速且显著的扩增以及浸润到肿瘤组织部位,证明肿瘤杀伤力的增强以及肿瘤组织的缩小。
结果显示,结直肠癌组实现了71.4% (5/7) 的总缓解率和14.3% (1/7) 的完全缓解率。甲状腺癌组达到66.7% (2/3) 的总缓解率和 33.3% (1/3)的完全缓解率。
目前,我国针对实体瘤的CoupledCAR™平台在CAR-T技术领域具有百余项全球专利及专利申请。简单来讲,CoupledCAR™解决了实体瘤CART细胞难以进入到实体肿瘤内部难以在体内扩增、以及难以对肿瘤细胞造成杀伤的难题。
解除免疫抑制
一些研究通过修饰CAR-T细胞,使其过度表达促进炎症的细胞因子(如IL-12、 IL-15和IL-18),这样的CAR-T细胞被称为“装甲”CAR-T细胞,可以调节局部微环境。研究证实,在卵巢癌中,IL-12可以提高T细胞的增殖和存活能力,抵抗凋亡和PD-1诱导的功能抑制。
无进展生存5个月,生存达17个月!新型CAR-T疗法成效显著!
2月18日,国际一流学术期刊《癌症免疫治疗杂志》刊登了关于中国医学研究者采取CAR-T自分泌PD-1抗体用于实体肿瘤治疗的研究成果。临床数据显示,一名晚期难治性卵巢癌患者采用这种治疗手段后,无进展生存5个月,生存达17个月。

此文也是国际上第一篇使用CAR-T自分泌PD-1抗体用于实体肿瘤治疗的临床数据文章。研究者介绍道,目前已经有多种CAR-T细胞疗法可以在血液肿瘤的初始治疗中达到100%的初期缓解率,对于复发弥漫性大B细胞淋巴瘤(DLBCL)患者中,第5年时46%的患者可达到完全缓解。
因此,对于CAR-T细胞治疗技术而言,能否有效地攻克实体瘤是肿瘤治疗的核心关键!目前最核心的难点就在于找到合适的靶点和解除肿瘤微环境对于CAR-T细胞的抑制,那么到这里不得不提到的免疫疗法就是PD-1/PD-L1抑制剂。
PD-1/PD-L1抑制剂对PD-1的阻断作用可以显著增强CAR-T细胞的抗肿瘤功效和反向免疫抑制。在该研究中采用的是阿帕替尼(Apatinib),这是一种有前景的抗血管生成药物和小分子血管内皮生长因子受体-2(VEGFR-2)酪氨酸激酶抑制剂。经过多线治疗后已用于晚期胃癌,非小细胞肺癌,乳腺癌和卵巢癌。此外,抗血管生成剂与免疫疗法的结合还改善了实体瘤的疗效。
在这项研究中,化疗失败史的卵巢癌患者接受了与阿帕替尼组合的两次αPD-1-mesoCAR-T细胞输注。MRI观察到肝转移结节的协同抑制作用。该患者获得部分缓解,生存了17个月,并有轻微的副作用。结果表明,CAR-T细胞与阿帕替尼的组合将成为治疗晚期/难治性卵巢癌的新治疗方法。
多靶点联用
目前针对两个靶点的双特异性CAR-T已在血液肿瘤领域得到应用,可以提高CAR-T对抗原的识别能力,增加疗效和安全性,降低肿瘤逃逸的风险。靶向两种或者多种不同肿瘤相关抗原的CAR-T疗法也是治疗实体瘤的重要方向。
9月23日,Nature Cancer上发表了一篇针对神经母细胞瘤(NB)模型的双靶点CAR-T研究进展。该研究就是靶向GD2和B7-H3两种神经母细胞瘤的相关抗原。
CAR-T疗法的获批将为中国患者带来更多临床获益
阿基仑赛注射液、瑞基奥仑赛注射液的纷纷获批上市,首先对符合其适应症的患者又增加了一种新的治疗选择,也就多了一份治愈的希望。
其次,这两次的获批意味着CAR-T疗法已经被国内环境所接纳,未来更多CAR-T产品或适应症的研发及审批都将得到提速。
经过近30年的发展,CAR-T细胞疗法已然兴起,该领域不会孤立的发展。目前已经有一些试验表示,很可能最好的肿瘤响应需要特异性的CAR-T疗法结合小分子治疗、免疫调节、化疗和基于抗体的治疗等多种治疗的协同作用,这些试验不提供特定的CAR,而是针对一些可能的抗原靶点设计CAR,这些抗原靶点取决于病人疾病的免疫表型。
在个性化医疗的时代,无论是单一疗法还是联合疗法,CAR-T无疑是医药领域火热的研究对象,希望今后能够取得更多突破,在血液肿瘤和实体瘤的治疗上展现其独特的实力!
参考文献
1.https://pubmed.ncbi.nlm.nih.gov/33972771/
2.https://pubmed.ncbi.nlm.nih.gov/32731404/
3.https://www.nature.com/articles/s43018-021-00244-2?proof=t%2525C2%2525A0

































 首页
首页 咨询
咨询 方舟新药
方舟新药 营养商城
营养商城