新泛突变EGFR靶向药物TAS6417(CLN-081)获FDA突破性疗法指定
TAS6417获FDA突破性疗法指定
2022年1月5日,FDA授予CLN-081(TAS6417)突破性疗法指定,用于治疗EGFR外显子20插入突变(ex20ins)的局部晚期或转移性非小细胞肺癌患者,且患者前期曾经接受过铂类化疗。
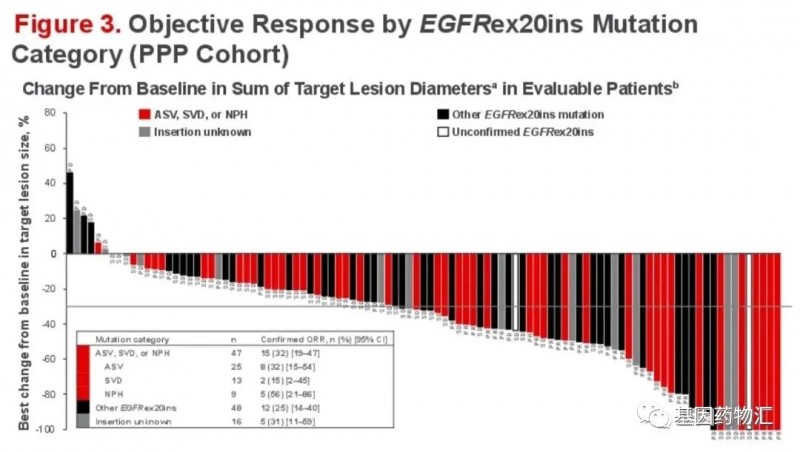
根据目前已经公开的临床试验数据,在42例接受CLN-081治疗的患者(有可用于评估的实体病灶)当中,整体缓解率为50%,疾病控制率64%。截至2021年ASCO大会上数据发布时,仍有52%的患者还在接受治疗。
报告了数据的44例患者,中位治疗线数为2次,范围在1~9次;其中8例患者接受过第一代EGFR抑制剂阿法替尼或吉非替尼的治疗,9例患者使用过奥希替尼,4例患者接受过泛HER抑制剂波齐替尼(Poziotinib)和/或第一代EGFR ex20ins抑制剂Mobocertinib(TAK-788)治疗,25例患者接受过免疫治疗。
值得注意的是,在前线接受过EGFR ex20ins抑制剂治疗的4例患者中,2例患者达到了部分缓解,2例患者疾病稳定,整体来说,疾病控制率达到了100%!
CLN-081是一种新型的疗法,尽管目前临床上已经有了
多款已经上市或正在进行临床试验的ex20ins靶向治疗药物,但这款药物仍有其独特之处。
CLN-081是一款泛突变的选择性EGFR酪氨酸激酶抑制剂,这意味着这款靶向药物对于各类EGFR突变亚型都具有一定的治疗潜力,其中就包括了被称为EGFR难治突变亚型的ex20ins。
目前,临床上已经有两款靶向治疗药物获批了ex20ins的适应症,均用于治疗接受过前线化疗之后的患者。
Amivantamab-vmjw(Rybrevant,JNJ-6372)
适应症:EGFR外显子20插入突变(ex20ins)的非小细胞肺癌
日期:2021年5月22日
相关阅读:获批了!靶向“双抗”JNJ-6372获FDA批准上市,难治非小细胞肺癌迎来首款新药!
相关临床试验及数据:
【CHRYSAILS试验】Amivantamab(JNJ-6372)治疗已经接受过铂类化疗且疾病进展的EGFR ex20ins突变非小细胞肺癌患者,整体缓解率为40%,中位治疗时间11.1个月,中位无进展生存期8.3个月,中位总生存期22.8个月。
Mobocertinib(Exkivity,TAK-788)
适应症:EGFR外显子20插入突变(ex20ins)的非小细胞肺癌
日期:2021年9月15日
相关阅读:又一款上市了!第二款EGFR难治突变靶向药获FDA批准,疾病控制率78%!
相关临床试验及数据:
【NCT02716116】Mobocertinib治疗已经接受过铂类化疗且疾病进展的EGFR ex20ins突变非小细胞肺癌患者,整体缓解率为28%,中位缓解持续时间17.5个月,中位无进展生存期为7.3个月,中位总生存期24.0个月。
如果患者们需要申请EGFR ex20ins抑制剂的临床试验,可以联系基因药物汇-临床新药招募中心了解详情。
此次CLN-081获得了突破性疗法称号的适应症也相同,但在其已经公开的临床试验数据当中,还包括了一部分已经在前线接受过了其它EGFR ex20ins抑制剂治疗的患者。这部分患者在接受CLN-081治疗的时候仍然能获得相当不错的疗效。
除此以外,其它的临床前试验也证实,CLN-081对于EGFR突变的其它亚型,包括常见突变外显子19缺失(ex19del)和L858R,以及T790M(第一/第二代EGFR抑制剂耐药突变)都具有很强的抑制能力,对于罕见突变G719X、L861Q和S768I,以及常见的(顽固的)ex20ins也具有一定的治疗潜力。
总而言之,根据研究者的评估,CLN-081的适应症范围比现有的许多药物药更广,很有希望为现有的EGFR突变非小细胞肺癌治疗打开一个全新的局面。
目前,研究者正在推进这款药物的其它临床试验,以进一步地评估其疗效。







































 首页
首页 咨询
咨询 方舟新药
方舟新药 营养商城
营养商城