癌症肿瘤CART治疗,盘点2022年11大CAR-T细胞免疫疗法实体瘤的"明星靶点"
CART治疗效果
对于癌症的治疗和攻克,我国的医学家们从未停止过研究创新的脚步,从最初的化疗药,再到现如今的靶向、免疫治疗,我们距离治愈癌症的目标也越来越近。而近期内最火的癌症疗法,当属于免疫疗法中的嵌合抗原受体T细胞(CAR-T)。
与以往开发抗癌药物,包括最新的靶向药物,成功的目标都是“延长患者的寿命”、“提高患者生活质量”,描述抗癌药物有效的指标是“1年生存率”、“5年存活率”等,并没有不切实际地提出把“治愈癌症”作为目标。
然而CAR-T当时是以治愈癌症为目标,最早接受CAR-T治疗的是30例白血病患者,他们并不是普通的白血病患者,而是尝试了多种治疗(化疗、靶向治疗等)后,其中甚至有15例进行了骨髓移植,但是不幸都失败了。通常情况下,他们的生存期不超过半年,按照中国的说法,死马当活马医。
结果就是这批吃螃蟹的人震惊了世界!27例患者的癌细胞在治疗后完全消失,20例患者在半年后复发,体内仍然没有发现癌细胞。最典型的当属Emily。
迄今为止,Emily已被成功治愈9年,她也成为这一史诗级疗法的代言人而载入史册。

作为一种“活的”药物,CAR-T疗法与传统药物有着很大的区别。它是一种治疗肿瘤的新型精准靶向疗法。通过基因工程技术将T细胞激活,并装上定位导航装置CAR(肿瘤嵌合抗原受体),将T细胞这个普通“战士”改造成“超级战士”,即CAR-T细胞,专门识别体内肿瘤细胞,并高效杀灭肿瘤细胞,从而达到治疗恶性肿瘤的目的。与传统的化疗和造血干细胞移植相比,它对肿瘤细胞的杀伤更为精准,在提高疗效的同时大幅减轻了毒副作用。
目前,随着2021年阿基仑赛注射液、瑞基奥仑赛注射液先后在中国获批上市,2022年西达基奥仑赛被美国FDA获批上市,CAR-T疗法已进入井喷期。这项技术在治疗各种恶性肿瘤方面取得了巨大进展,已成功应用于多种血液恶性肿瘤的治疗。
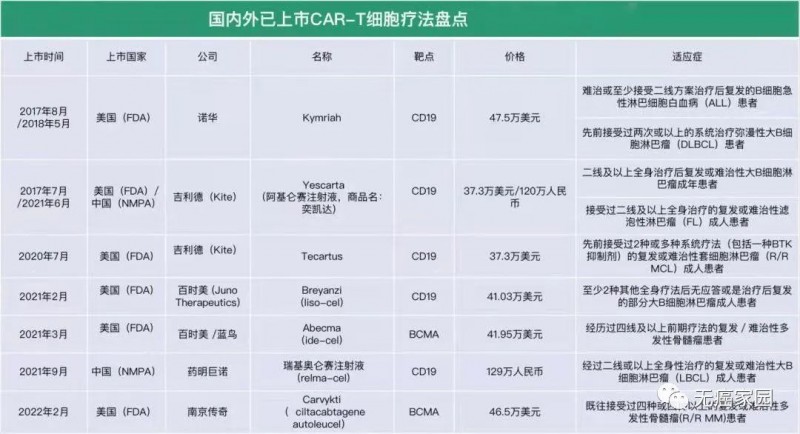
目前国内外已上市的CAR-T细胞疗法
CAR-T细胞免疫疗法实体瘤的"明星靶点"
然而,面对占比90%以上的实体瘤治疗领域,CAR-T疗法同样存在巨大的临床需求。值得一提的是,在实体肿瘤方面如消化系统肿瘤领域CAR-T取得了一定的疗效,包括食管癌、胃癌、肝癌、结直肠癌、胰腺癌、胆管癌等。
而CAR-T疗法用于实体瘤的关键点就是实体瘤靶点的选择,目前目前临床在研的CAR-T项目涉及的靶点分布情况,以2021年最新的全球癌症数据为例,主要集中在GPC3、Claudin18.2、MSLN、HER2、EGFR等热门靶点上。
今天,无癌家园小编就给各位癌友们盘点下2022年11大实体瘤“明星靶点”,想必这也是癌症患者们都格外关注的重磅内容!
TOP1、Claudin18.2
Claudin18.2(CLDN18.2)是Claudin蛋白质家族的一员,位于细胞膜表面,正常情况下仅低水平表达于胃粘膜分化上皮细胞,但在病理状态下,Claudin18.2在多种肿瘤中有的表达显著上调,包括80%的胃肠道腺瘤、60%的胰腺肿瘤。此外,CLDN 18.2活化还可见于食管癌、卵巢癌和肺腺癌中,因此是具有潜力治疗癌症的热门靶点。
据无癌家园小编查阅ClinicalTrials及CDE(国家药监局)发现,目前批准临床的Claudin18.2产品就多达几十款,多数药物均是拟用于治疗晚期胃癌、胰腺癌及实体瘤患者。
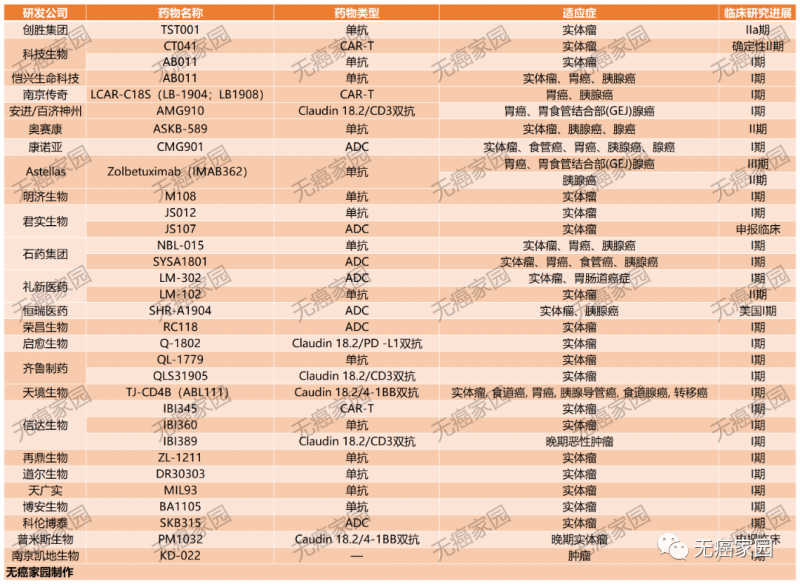
因该靶点在正常组织中的高度特异性表达,再加上在多种癌症中的激活表达,使得Claudin18.2蛋白成为了研究人员开发胃癌、胰腺癌等实体瘤免疫疗法的理想靶点。同时,由于胃癌是国内的一大瘤种,Claudin 18.2靶点有望实现胃癌新靶点药物的瓶颈突破。
胃癌、胰腺癌
作为国际上首个针对Claudin18.2的CAR-T细胞,CT041早在2019年ASCO年会上就崭露头角,当时总客观缓解率为33.3%就已经惊艳世界,如今更加显著的疗效无疑是锦上添花!此次的临床数据展现出对消化系统肿瘤的良好治疗前景!
国产CAR-T疗法CT041首次亮相ESMO
2021年欧洲肿瘤内科学会(ESMO)年会上,由科济药业开发的靶向Claudin18.2(CLDN18.2)自体CAR-T候选产品CT041展现了其在消化系统肿瘤中的突出疗效,可谓是大放异彩!
研究数据格外亮眼!
1. 所有患者的客观缓解率达48.6%,疾病控制率达73%;所有胃癌患者总客观缓解率为57.1%。
2. 既往接受至少2线治疗失败的胃癌患者:客观缓解率为61.1%,疾病控制率为83.3%。
3. 而且总体耐受性良好!
截止到2022年3月3日,CT041成为全球首个且唯一进入到确证性Ⅱ期临床试验的用于治疗实体瘤的CAR-T细胞候选产品。这是CAR-T攻克实体瘤领域是里程碑般的存在,可喜可贺!
除此之外,还有多款靶向CLDN18.2的CAR-T细胞疗法。例如,由传奇生物研发的LB-1904,用于治疗胃癌或者胰腺癌,目前已经进入临床I期试验。此外,传奇生物还启动了一项靶向Claudin18.2 的CAR-T细胞制剂LCAR-C18S,用于治疗晚期胃腺癌患者,目前也正在进行临床试验招募中。
目前急招B细胞淋巴瘤、T细胞淋巴瘤、T细胞白血病(T-ALL)、急性白血病、非霍奇金淋巴瘤、肝癌、胃癌、前列腺癌、甲状腺癌等癌种!
想要评估病情是否能够接受CAR-T疗法可将病理报告、治疗经历及出院小结等提交至无癌家园医学部进行初步评估!
TOP2、GPC3
磷脂酰肌醇蛋白聚糖3(glypican 3,GPC3)在调控细胞生长和分化方面起重要作用,与肝癌的发生、发展密切相关。GPC3在肝细胞癌、卵巢透明细胞癌、卵黄囊癌等生殖系统肿瘤中表达,其在肝细胞癌中的表达率达74.8%,而在正常肝组织内几乎无表达,称为肝癌CAR-T治疗新的理想靶点。
肝癌
由上海交通大学医学院附属仁济医院肿瘤介入科科主任翟博教授团队等完成的突破性研究成果,发表在2020年5月5日的国际权威期刊《Clinical Cancer Research(临床肿瘤研究)》上。
截止到2019年7月24日,共有13例患者接受了中位值为19.9×108的CAR-GPC3 T细胞。所有患者均为GPC3阳性,均接受过手术治疗、局部治疗或全身性的系统治疗,都携带乙型肝炎病毒(HBV)。
其中有2例患者获得部分缓解(PR),所有患者6个月、1年和3年的生存率分别为50.3%、42.0%和10.5%,中位生存时间(OS)为278天(39.7周)。
2021年ASCO年会上我国医学研究者们首次公布了靶向GPC3的CAR-T药物(Ori-CAR-001)治疗复发/难治性肝细胞癌的最新临床研究数据。
截至2021年3月10日,共纳入11名接受细胞输注的复发受试者。所有受试者均患有晚期肝细胞癌,并且经过化疗、TACE(肝动脉化疗栓塞术)和靶向治疗均无效。9例可评估受试者中,4例达到部分缓解 (PR),3例达到疾病稳定 (SD),2例出现疾病进展 (PD),客观缓解率为44%,疾病控制率达到78%。
TOP3、间皮素(Mesothelin)
间皮素(MSLN)在肿瘤中的表达非常广泛,约有95%恶性间皮瘤,80%~85%胰腺癌,68.8%卵巢癌和53%肺癌表达间皮素。MSLN高表达调控了多种细胞信号通路,并与肿瘤增殖、侵袭和不良预后有密切联系。MSLN也是三阴性乳腺癌特征性标志物,而三阴性乳腺癌对单抗药物几乎无敏感性,MSLN CAR-T细胞有望成为三阴性乳腺癌仅有的免疫治疗药物。
卵巢癌
国际知名杂志《Journal of Hematology & Oncology》刊登了我国医学研究者们的一项成功改造CAR-T技术的临床研究,研究中提及的CAR-T产品选择的靶点有mesothelin(MSLN,又称为间皮素,可以应用于多种上皮癌症,比如恶性间皮瘤、胰腺癌、胃癌、卵巢癌等)。
其中1例晚期胰腺癌患者,接受的是静脉回输的CAR-T治疗,治疗后全身的病灶,基本都实现了代谢活性完全消失。
典型病例
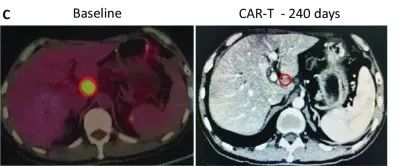
受试者GD-G/M-005 是一例具有 MSLN 表达的晚期胰腺癌患者。该受试者进展为局部淋巴结转移(24×33 mm)(图c)。抗 MSLN-7 × 19 CAR-T 细胞首先通过肝动脉输注,当晚伴有高烧,没有细胞因子释放综合征 (CRS) 或神经毒性。随后,他每1~2个月接受一次抗 MSLN-7×19 CAR-T 细胞的静脉输注。
直到增至CAR-T细胞输注的5倍,CT分期显示他在治疗240天后达到完全缓解,测定的淋巴结为8.3×9.6mm,并未见其他肿大的淋巴结(图C),患者此时病灶完全消失,保持正常状态。
TOP4、EGFR
表皮生长因子受体(EGFR)是一种酪氨酸激酶受体,约在50%的成人原发性胶质母细胞瘤中存在,此外,也可作为非小细胞肺癌、肝癌、胃癌、结直肠癌等癌种的靶点。
非小细胞肺癌
301医院在国内率先开展CAR-T疗法,成果显著。韩为东教授曾报道过利用EGFR为靶点的CAR-T治疗EGFR表达强阳性(EGFR表达超过50%)的晚期难治性的非小细胞肺癌患者。
研究结果显示,其中11例患者疗效可评价:2例患者肿瘤明显缩小,5例疾病稳定。
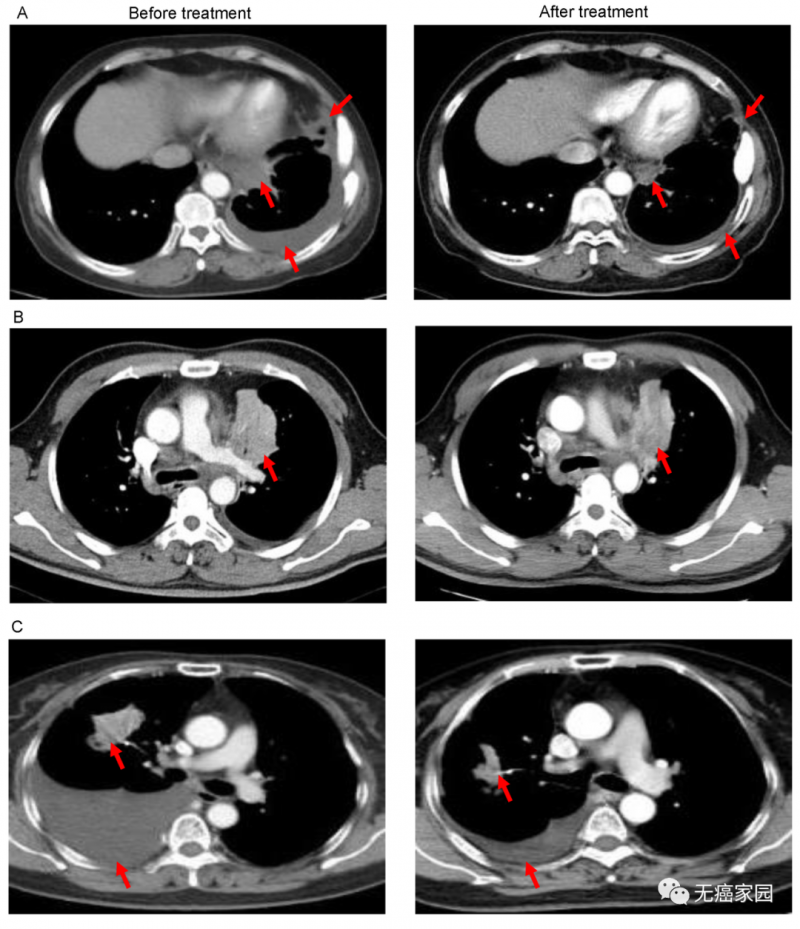
图A中患者1在输注CAR-T细胞后,通过CT扫描显示其胸腔积液减少,转移性肺门淋巴结和胸膜结节轻度缩小(箭头)。
图B中CT图像显示患者8的原发性肿瘤缩小(箭头);
图C中CT检查发现CAR-T治疗后患者9的胸腔积液吸收和肺部病变明显消退。
TOP5、前列腺特异性膜抗原(PSMA)
PSMA是一种II型跨膜蛋白,通常在肾小管和十二指肠中表达,并特异性地表达于前列腺癌上皮细胞。在前列腺癌组织中,PSMA的表达明显上调。
研究显示,PSMA在超过90%的前列腺癌细胞表面都出现了过表达(比正常前列腺细胞高100~1000倍),并且在晚期和去势抵抗性前列腺癌患者癌细胞中表达水平更高。因此,PSMA称为前列腺癌诊断及治疗的重要靶点。
前列腺癌
2022年2月17日,在2022年美国临床肿瘤学会泌尿生殖系统癌症专题研讨会(ASCO GU)上,Poseida Therapeutics公司公布了其自体CAR-T细胞疗法P-PSMA-101,在治疗转移性去势抵抗性前列腺癌(mCRPC)患者的1期临床试验的中期结果。
截止到2021年12月31日,共纳入17例转移性去势抵抗性前列腺癌(mCRPC)患者,其中可评估患者14例。值得一提的是,这些患者平均接受七线治疗,自诊断以来的平均中位时间为6.4年。
试验的关键结果包括:
●71%(10/14)的患者肿瘤标志物前列腺特异性抗原(PSA)水平明显下降;
●36%(5/14)的患者PSA水平下降>50%;
●1例患者显示肿瘤完全消除,并保持10个月以上的持久缓解;
●一些患者的活体组织检查证实,干细胞记忆T细胞(Tscm)这种产品的性质可使CAR-T细胞定向转运到骨骼中,这对前列腺癌等易骨转移的疾病非常重要。
●P-PSMA-101表现出良好的安全性和耐受性。
TOP6、HER2
人表皮生长因子受体-2(HER2)是一种大分子的I型跨膜蛋白,又称ErbB2,是ErbB受体家族的一员。HER2最早出现在乳腺癌的研究中,乳腺癌红基因突变容易导致HER2阳性,并且HER2高表达欲肿瘤低预后、低无病生存期有关,HER2也高表达在部分膀胱癌、卵巢癌、子宫内膜癌、胰腺癌和非小细胞肺癌中。
HER2在大约10%的胃癌中过表达,针对Her2的单克隆抗体Herceptin也已经被批准用于Her2过表达的胃癌中。近期临床前研究显示,CAR-T-HER2细胞对HER2+的胃癌细胞具有特异性的杀伤效果。
TOP7、癌胚抗原(CEA)
癌胚抗原(CEA)最初发现于结肠癌和胎儿肠组织中,后被证实广泛存在于内胚叶起源的消化系统肿瘤,比如胃癌、肝癌、胰腺癌(超75%)、结直肠癌(60%)。一项临床前研究显示,靶向CEA的CAR-T细胞可以诱导胃癌细胞发生凋亡。
例如,第三军医大学钱程教授团队曾报道了CEA CAR-T细胞在10例晚期结直肠癌患者中的临床效果,其中7例患者疾病稳定,2例出现明显肿瘤缩小,所有患者均观察到血清CEA不同程度下降。
TOP8、神经节苷脂2(GD2)
GD2是一种表面糖脂抗原,在神经母细胞瘤、星形细胞瘤、视网膜母细胞瘤、肉瘤、黑色素瘤等多种肿瘤细胞中高表达,而在正常组织中表达受限,主要在神经元细胞体和间充质干细胞上低水平表达,因此成为CAR-T的理想靶点。
Louis等学者第一次构建了GD2靶向的CAR-T细胞治疗神经母细胞瘤,I期临床试验结果显示,19例患者中有3例患者完全缓解,除轻微疼痛外无明显不适。2016年,在贝勒医学院公布的一项GD2 CAR-T细胞临床试验的结果中,11例神经母细胞瘤患者中有5例获得疾病稳定,经后续补充治疗2例获得完全缓解。
目前,GD2 CAR-T细胞在实体瘤中的疗效最为显著,并有希望成功进入III期临床试验,成为第一个进入III期临床试验的实体瘤CAR-T细胞靶点。
TOP9、上皮细胞黏附分子(EpCAM)
EpCAM是一个过表达在多种肿瘤的跨膜糖蛋白,被认为是一种潜在的肿瘤干细胞标志物,有超过90%的胃癌过表达EpCAM,但是EpCAM也表达于胰腺等组织,所以针对EpCAM的单克隆抗体在临床中可引发胰腺炎,故针对EpCAM的CAR-T必须注意这样的风险。
TOP10、EGFRvⅢ
表皮生长因子受体变体Ⅲ(EGFRvⅢ)是一种胶质母细胞瘤相关特异性抗原,是胶质母细胞瘤治疗的理想靶点。EGFRvⅢ由部分细胞外结构域的框内缺失导致,在正常组织中不表达,具有肿瘤特异性和免疫原性表位。在人EGFRvⅢ阳性胶质母细胞瘤的移植模型中,EGFRvⅢCAR-T对野生型 EGFR 缺乏反应性,并可显著延迟肿瘤进展。
TOP11、黏蛋白1(MUC1)
MUC1是一种跨膜黏蛋白,广泛过表达在胃癌、肝癌、胰腺癌,目前已经广泛开展了抗MUC1的CAR-T治疗临床试验。
Posey等学者是最早构建肿瘤MUC1靶向的CAR-T细胞的团队之一,在2016年他们就通过动物实验验证了MUC1 CAR-T对胰腺癌、乳腺癌、非小细胞肺癌、白血病细胞等多种癌细胞又识别杀伤作用。
国内杨林教授团队曾报道过1例MUC1 CAR-T细胞治疗精索细胞癌的临床试验,患者出现肿瘤缩小和瘤灶内坏死,试验中无不良反应发生。
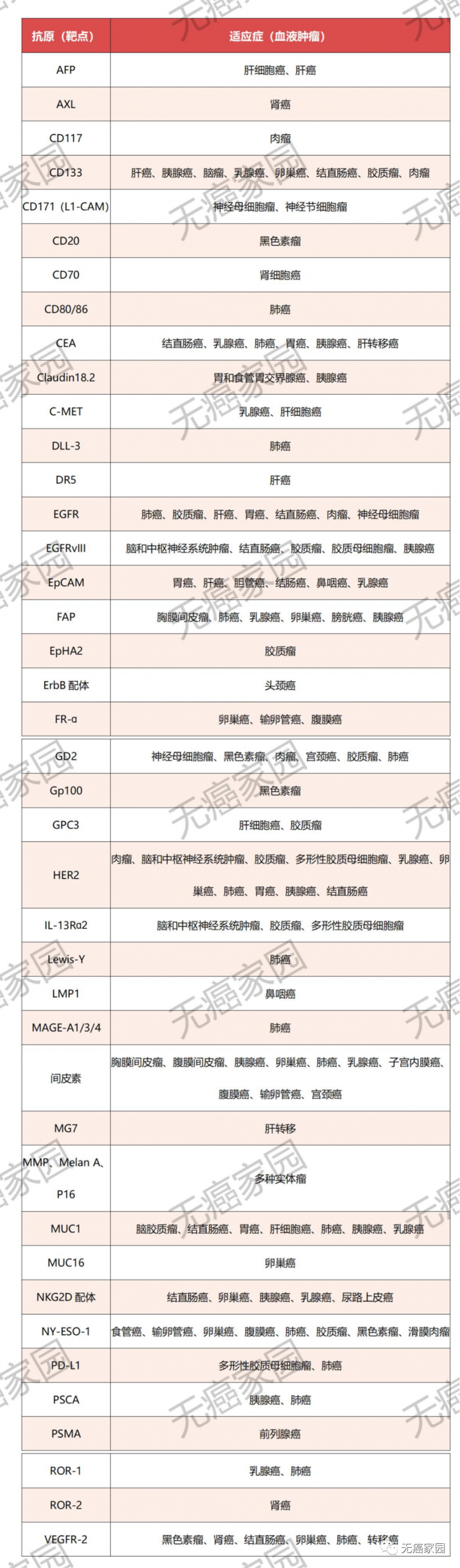
除了上述小编提到的热门靶点外,还有很多治疗靶点,特整理如图所示。
天价≠神药!CAR-T疗法虽好,但要理性看待
CAR-T疗法作为新型细胞疗法,近年来在全球癌症细胞免疫治疗领域,可谓是独占鳌头。
但是面对CAR-T疗法,大家还需要保持清醒,理性看待!的确有一部分晚期癌症患者采用CAR-T疗法逆转命运。但它并非万能神药,在实体瘤的治疗上依然充满挑战。
而且与其他的抗癌药一样,CAR-T疗法也有其副作用,例如细胞因子风暴、神经毒性、B细胞终身缺失等,但目前已经有很好的控制方法,能够较好地应对。
因此,基于不菲的价格和副作用,通常CAR-T疗法被用于标准治疗失败(手术、放疗、化疗、靶向治疗、PD-1治疗等)的复发难治性患者身上。
2021年我国迎来了细胞免疫治疗的元年,作为先锋的CAR-T疗法,是未来发展方向之一。CAR-T疗法主要在于改造T细胞来使其识别肿瘤细胞的特殊靶点,理论上,可以有无数种针对不同靶点的CAR-T疗法,这意味着蕴含着无限可能。
希望不久的将来,能够在国内外医学科研工作者的努力下,降低细胞疗法毒副作用,降低价格,突破实体瘤的瓶颈,让越来越多的晚期癌症患者获益!
参考文献
1.https://stemcellres.biomedcentral.com/articles/10.1186/s13287-020-02128-1
2.https://www.sciencedirect.com/science/article/pii/S0024320520310523







































 首页
首页 咨询
咨询 方舟新药
方舟新药 营养商城
营养商城