胰腺癌靶向治疗,这6类新的胰腺癌靶向治疗方案疾病控制率高达100%
胰腺癌又被称作“癌王”,它将癌症所有的“恶毒”之处展现得淋漓尽致:起病隐匿、鉴别困难、进展迅速、容易转移、治疗困难……如果不接受任何治疗,晚期胰腺癌患者的中位生存期仅有4个月左右!
这样的特点,导致了大量的胰腺癌患者直到发展至Ⅳ期,才开始接受系统的治疗。但是晚期以及转移性胰腺癌的治疗又非常困难,患者可以选择的方案并不多,接受治疗的过程中也极易发生耐药、进展以及转移。
直到近几年,大量新靶点的药物以及疗法投入临床,才终于改变了这样的困境。这一次,基因药物汇为大家总结了胰腺癌靶向治疗最关键的6个靶点。其中,3个靶点已经有获批上市用于胰腺癌治疗的药物,3个靶点的药物正处于临床研究当中,非常值得关注。
胰腺癌BRCA突变靶向治疗
从致病的角度来说,BRCA1和BRCA2是家族性胰腺癌最常见的原因。BRCA2突变的携带者在一生的某个时刻罹患胰腺癌的概率高达5%~10%,BRCA1突变则会导致胰腺癌的风险增加2~4倍。
而且这类突变能够导致的癌症不仅仅只有胰腺癌,还包括了乳腺癌(10倍)、卵巢癌(50倍)、前列腺癌(4.5倍)等等。因此如果家族当中有相关的癌症病史,家属一定要注意做好筛查,定期体检。
以治疗BRCA1/2突变最经典的药物之一,奥拉帕利(Olaparib)为例。这款药物在2019年12月获得了美国食品药品管理局(FDA)的批准,用于一线化疗后获益、疾病未进展的胰腺癌。
为该项批准提供依据的是Ⅲ期POLO试验的结果。这项试验为来自4个大洲、119个医学中心的3315例患者进行了BRCA突变的筛查,其中7.5%的患者被发现存在这类突变。这些患者接受了一线铂类化疗,治疗时间超过16周,并在获益之后,接受奥拉帕利或安慰剂的维持治疗。
结果显示,接受奥拉帕利治疗的患者,无进展生存期几乎达到了安慰剂的两倍(7.4个月 vs 3.8个月)。奥拉帕利治疗,能够明显降低转移性胰腺癌患者发生疾病进展或者死亡的风险。
胰腺癌KRAS突变靶向治疗
KRAS是胰腺癌最主要的几个驱动基因突变之一,根据既往的研究,其检出率在10%左右。
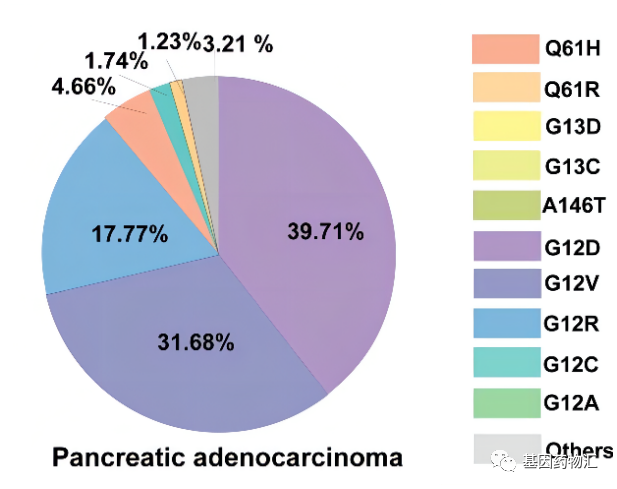
尽管KRAS突变的重要性一直备受关注,但相关药物以及治疗方案的研发进展一直不太理想。自从被确认为原癌突变以后的超过三十年内,KRAS抑制剂的研发都止步不前。并不是没有新药问世,只是各类新药的疗效都不尽理想,很难真正投入临床。
直到2013年,一篇刊登于Nature(《自然》)杂志上的文章,公开了被认为是将KRAS从“不可治”扭转为“可治”的颠覆性研究成果。来自加州大学旧金山分校的研究团队首次发现了KRAS突变蛋白质上能够被小分子药物结合的位点,实现了使用药物使KRAS蛋白质失活的突破。
至2019年,Sotorasib(AMG510)同样在Nature震撼登场,才向所有人证明——KRAS突变的“不可成药”终于成为了历史,KRAS抑制剂的研究终于走上了正轨。
在本年度的ASCO消化道肿瘤分会上,两款经典KRAS抑制剂分别公布了治疗包括胰腺癌在内的多类消化道癌症的最新数据。疗效刷新历史!
1、阿达格拉西布
根据本年度美国临床肿瘤学会(ASCO)胃肠道肿瘤研讨会上公布的Ⅱ期KRYSTAL-1试验最新数据,Adgrasib(阿达格拉西布,MRTX849)在包括胰腺癌在内的多类消化道肿瘤的治疗当中,都具有非常出色的潜力。
此次Ⅱ期试验涵盖了包括胆道癌、阑尾癌、小肠癌、胃食道结合部癌、食道癌以及胰腺导管腺癌在内的多类消化道肿瘤。目前公开了27例可评估患者的治疗结果,患者均为KRAS G12C突变的患者,先前接受过至少2种系统性抗癌治疗。
结果显示,27例可评估的患者,整体缓解率为41%,疾病控制率高达100%,即全部受试患者均达到了临床疾病稳定。
在10例胰腺癌患者当中,整体缓解率为50%,中位缓解持续时间7.0个月,中位无进展生存期为6.6个月;其它患者的整体缓解率为35%,中位缓解持续时间为7.9个月,中位无进展生存期为7.9个月。
这说明什么?显然,KRAS G12C突变的胰腺癌患者,对于Adgrasib治疗的响应率更高,响应时间也非常不错;其它消化道肿瘤的患者,响应率也不错,响应时间更长。目前这款药物的多项临床试验均在进行当中,其中部分试验正在招募受试患者。希望尝试这款药物或其它同类药物的患者,可以咨询基因药物汇了解详情。
2、索托拉西布
同样是在本年度ASCO-GI上公布的数据,另一款经典的KRAS G12C抑制剂Sotorasib(索托拉西布,Lumakras,AMG-510)的疗效也非常出色。
根据Ⅰ/Ⅱ期CodeBreaK100试验的数据,使用Sotorasib治疗曾经接受过大量预处理(多线治疗,其中79%的患者接受过至少2种或更多治疗)的KRAS G12C突变的局部晚期或转移性胰腺癌患者,取得了不错的疗效。
患者38例,接受Sotorasib治疗的整体缓解率为21.1%,疾病控制率为84.2%,也就是说有84.2%的患者达到了临床疾病稳定。治疗的中位缓解持续时间为5.7个月,中位无进展生存期为4.0个月,中位总生存期为6.9个月。
Sotorasib对于一部分存在多发转移的患者,同样有非常好的疗效。举例来说,一位64岁的女性患者,基线时存在肝脏、淋巴结、肺以及腹膜多个部位的转移,之前曾经接受过FOLFIRINOX方案的治疗。在接受Sotorasib治疗之前,她的肝脏上有一个直径2.2厘米的病灶;治疗18周后,病灶缩小到了0.8厘米。
胰腺癌NTRK突变靶向治疗
NTRK本身是一种检出率比较低的突变,在胰腺癌当中有检出,但是比例仅占5%以下。但由于几款疗效非常出众的NTRK抑制剂的存在,这部分患者已经有机会得到非常好的治疗了。如果大家检测到了NTRK基因相关的突变,或有意向了解关于这些项目的信息,可以咨询基因药物汇。
1、拉罗替尼
拉罗替尼(Larotrectinib)是一款NTRK抑制剂,目前已经获批了实体瘤的适应症。在拉罗替尼取得了75%的超高缓解率的实体瘤临床试验当中,就有一部分胰腺癌的患者接受了治疗。
在这些获益的患者当中,相当一部分是已经接受过多种治疗、多次耐药、生存期非常不乐观的患者。凭借拉罗替尼的治疗,许多患者延长了很久的生命,生活质量也有保障!
拉罗替尼治疗胰腺癌案例
这位患者的癌症类型比较罕见,属于胰腺腺泡细胞癌,是一种罕见的胰腺外分泌恶性肿瘤。
患者确诊时已是81岁高龄,伴有胰周淋巴结肿大,不过患者状态不错,接受了手术切除,但在术后一个周期的吉西他滨辅助治疗之后,因为耐受性比较差而停止了治疗。
6个月后,患者疾病再次进展,这一次仍然选择了吉西他滨治疗,但降低了剂量。患者的胰周淋巴结大小持续增加,6个周期的治疗后,方案更换为吉西他滨+白蛋白紫杉醇(Nab-紫杉醇)。
联合方案使用仅4个周期之后,患者疾病持续进展,并且发生了新的肝转移。此时的基因检测结果显示患者存在SEL1L-NTRK1融合突变,因此患者开始使用拉罗替尼。
和前一案例当中的患者一样,这位患者使用的方案为标准的100 mg剂量每日两次方案。至案例发布时,患者已经接受了13个月的治疗,影像学缓解效果良好,没有出现严重的不良反应。
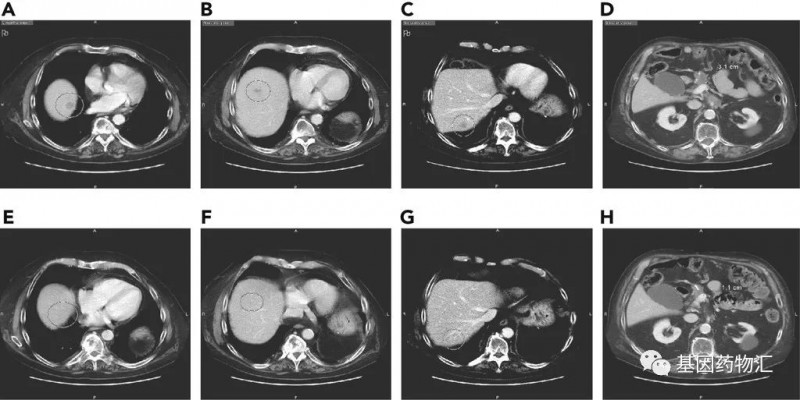
胰腺癌Claudin 18.2靶点靶向治疗
Claudin 18.2属于紧密连接蛋白家族中的一种亚型,在多种肿瘤组织中高度表达,比如胃癌(60%~80%)、胰腺癌(50%)、食管癌(30%~50%)和肺癌(40%~60%)等,但是在正常组织中几乎没有表达,因而具有出色的治疗潜力。
根据一些报告,大约28%的胰腺癌患者,表达Claudin 18.2的癌细胞能够超过75%。
其中,Claudin 18.2抑制剂Zolbetuximab已经到达了Ⅱ期临床试验阶段,多款同靶点其它药物也有一定的成果。如果胰腺癌患者希望尝试这一靶点的治疗方案,或者了解相同靶点的其它药物,可以联系基因药物汇。
胰腺癌HER2突变靶向治疗
HER2,全称人表皮生长因子受体2,是最重要的癌症驱动基因之一,在多类癌症当中高度表达。目前,乳腺癌、胃癌、食管癌、胆管癌、肺癌等等许多类型的癌症患者,都会重视HER2表达水平的检测。在胰腺癌当中,HER2的表达率大约为26%,高表达率约2%。
随着免疫疗法研究的深入,嵌合抗原受体(CAR)-T细胞疗法已经逐渐成为了一种昂贵但行之有效的治疗手段。在多个类型的血液系统肿瘤的治疗当中,CAR-T疗法已经获得了批准,投入了临床应用。
在胰腺癌这个适应症上,已经有一些小型研究探索了CAR-HER2-T疗法的疗效。在一项纳入了胰腺癌及胆管癌患者的11例患者小型研究显示,5例患者疾病稳定,1例患者达到临床缓解;患者的中位无进展生存期为4.8个月。
如果大家想了解更多CAR-T疗法项目,或尝试这类方案,可以咨询基因药物汇。
胰腺癌EGFR突变靶向治疗
EGFR抑制剂在胰腺癌治疗当中的价值,要从与EGFR相关的信号传导通路说起。Akt-2是EGFR信号通路当中的一个组成部分,在高达60%的胰腺癌活检标本当中存在过表达。因此,通过EGFR抑制剂来调节这条信号通路,有可能会对大量的胰腺癌患者有价值。
针对这一类型患者的治疗药物当中,厄洛替尼已经获得批准上市。从疗效上来分析,接受厄洛替尼+吉西他滨治疗的患者,1年生存率为24%,单独使用吉西他滨的对照组患者为17%。
小汇有话说
随着医学技术的发展,曾经被视为“无药可救”的“癌王”胰腺癌,治疗手段也越来越多了。从上面我们提到的靶向药物,到新兴的质子疗法、电场疗法等等,各种各样的新药物、新方案都加入了对抗“癌王”的队伍当中。
我们非常期待这些药物的未来发展,同时也希望,这样蓬勃的发展,能够转变为患者们生存期与生存质量实实在在的提升。







































 首页
首页 咨询
咨询 方舟新药
方舟新药 营养商城
营养商城