官宣!全球首款TIL疗法Lifileucel(LN-144、Amtagvi)获批上市!
如果说大家熟知的号称120万一针的鼎鼎大名的嵌合抗原受体T细胞(CAR-T)疗法在多种血液肿瘤(白血病、淋巴瘤、多发性骨髓瘤等)中表现出不俗的疗效,那么在占比90%以上的实体瘤方面,肿瘤浸润淋巴细胞(TIL)疗法则蕴含巨大的杀癌潜力,被喻为肿瘤细胞的“天然克星”!
就在春节假期的尾声之际,我们迎来一大振奋人心的消息!2024年2月16日,Iovance Biotherapeutics公司宣布Lifileucel(LN-144)获得美国食品和药物管理局(FDA) 加速批准上市(PDUFA日期为2月24日),用于治疗PD-1抗体治疗后进展的晚期黑色素瘤,商品名为Amtagvi。根据新闻稿可知,这也是全球首款获批上市的TIL疗法,更是首款获批的治疗实体瘤的T细胞疗法,具有里程碑的意义!

▲ 图片来源:FDA官网
疾病控制率高达80%!全球首款TILs疗法Lifileucel获批上市!
Lovance作为目前TILs细胞治疗领域领头羊,早些时候已向FDA启动递交创新型疗法LN-144(Lifileucel)滚动上市申请,用于治疗PD-1/PD-L1治疗后进展的晚期黑色素瘤。
TIL疗法招募实体瘤患者
扫描下方二维码 提交病历 快速申请入组!

本次获批主要是基于全球性的多中心2期研究C-144-01的临床试验数据,试验对象是在之前的抗PD-1/L1治疗和靶向治疗(如适用)期间或之后发生进展的晚期黑色素瘤患者。
数据截止到2022年7月15日,中位随访时间为36.5个月。在153例患者中,独立评审委员会(IRC)根据RECIST v1.1标准评估的客观缓解率(ORR)为31.4%,其中,9例获得完全缓解(CR),39例部分缓解(PR),71例疾病稳定(SD),27例疾病进展(PD)。在中位随访27.6个月的研究中,中位DOR未达到,41.7%的缓解持续时间≥18个月。中位总生存期(OS)和无进展生存期分别为13.9个月和4.1个月。
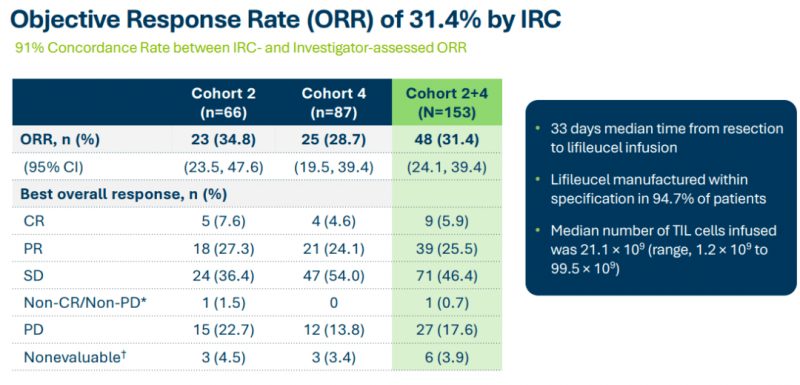
图源官网
在队列2(n=66)患者中,ORR为34.8%,5例患者达到CR,18例达到PR,24例达到SD,15例PD;中位随访时间为36.6个月时,中位DOR尚未达到。
在队列4(n=87)患者中,ORR达到28.7%,4例患者达到CR,21例达到PR,47例达到SD,12例PD;中位随访时间为23.5个月时,该队列的中位DOR为10.4个月。
Lifileucel的疾病控制率达到了惊人的79.3%(111/140)。从注射lifileucel到最佳疗效的中位时间为1.5个月,随着时间的推移疗效加深。7例PR患者转化为CR,其中1例患者在最初数据分析后约10个月内转化为CR。
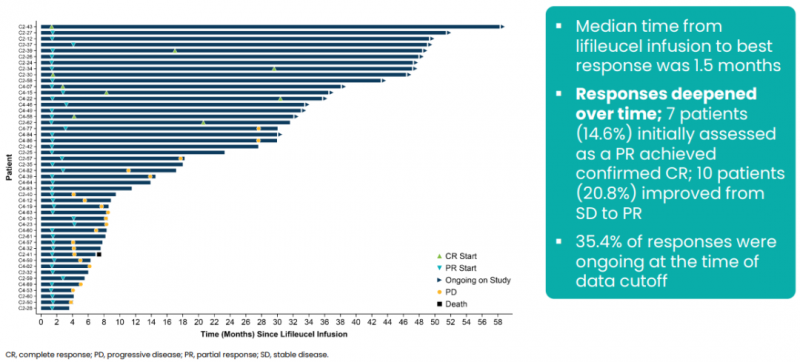
图源官网
在去年12月举办的ESMO免疫肿瘤学大会上,Iovance公布了C-144-01试验的4年随访数据。分析显示,由ICR所评估最长的缓解持续时间为55.8个月,且缓解仍在持续中。
值得一提的是,对lifileucel产生应答患者的肿瘤负荷较小,显示晚期黑色素瘤患者若能及早接受该疗法治疗,有可能增加治疗益处。
TIL疗法招募实体瘤患者
扫描下方二维码 提交病历 快速申请入组!

FDA 生物制品评估与研究中心 (CBER) 主任 Peter Marks 博士在一份新闻稿中表示:“不可切除或转移性黑色素瘤是一种侵袭性癌症,可能致命。Amtagvi的批准代表了科学和临床研究努力的巅峰,为治疗选择有限的患者提供了一种新型 T 细胞免疫疗法。”
目前,3期TILVANCE-301试验 (NCT05727904) 正在ITT人群中研究 lifileucel 加 pembrolizumab (Keytruda) 与 pembrolizumab 单药疗法。
目前无癌家园有TILs免疫细胞临床试验正在招募中,主要治疗恶性实体肿瘤等癌种。
有意向的患者若想参加可整理出完整的病理报告、治疗经历、出院小结等致电医学部,详细评估病情。






































 首页
首页 咨询
咨询 方舟新药
方舟新药 营养商城
营养商城