首款靶向HER2阳性的广谱抗体偶联(ADC)药物Enhertu(DS8201、德曲妥珠单抗)获FDA加速批准
化疗抗癌,常常是“杀敌一千,自损八百”。抗体药物,能够精准找到肿瘤靶点,但有时候战斗力不足。
要是能给抗体药物上安上化疗药物“弹头”,是不是就能更精准地打击癌细胞了?
基于此,一种被称为“生物导弹”的ADC(抗体药物偶联物)横空出世。从疗效数据来看,ADC药物给后线患者带了更多的治疗选择和延长生存期的希望,有多款药物的客观缓解率或中位无进展生存期相比化疗提高了一倍。
近年来ADC药物发展迅猛,作为最早获批应用ADC药物的实体瘤,ADC药物在乳腺癌治疗上迅猛发展并占据乳腺癌治疗的半壁江山。
要说起一款重磅抗体药物偶联物(ADC)的话,Enhertu(DS8201)当之无愧,其综合临床研究成果可谓是“实力抢镜”,就在近日又带来了令人惊讶的重磅消息!2024年4月5日,美国食品药品监督管理局(FDA)加速批准了由第一三共与阿斯利康联合研发的抗体偶联药物(ADC)Enhertu(德曲妥珠单抗,DS-8201)用于治疗具有“不限癌种”适应证的HER2阳性实体瘤患者,成为继PD-1抑制剂(针对MSI-H患者)及部分靶向药(针对RET、NTRK等基因阳性)后,首款具有不限癌种适应症的ADC药物。简单来说,只要是具备了HER2阳性的实体瘤患者均可使用,对于罹患了HER2阳性罕见癌症的患者来说尤为重要,这已实现了跨癌种治疗的可能。

截图源自Astrazeneca官网
HER2阳性全癌种都能用!ADC新药Enhertu横扫多种实体瘤!
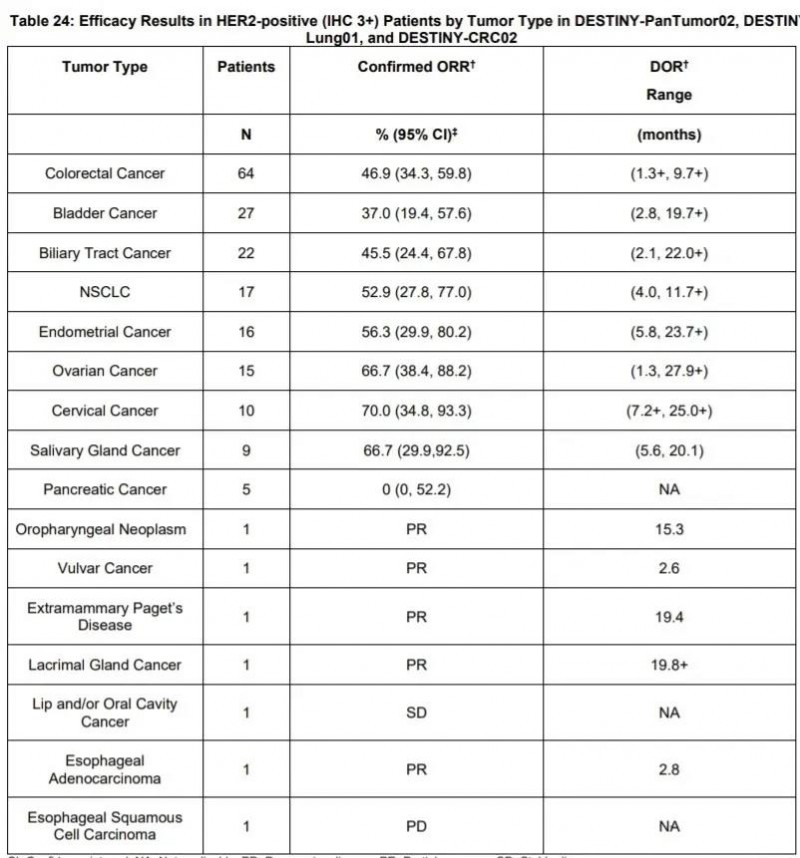
对192例既往接受过不可切除或转移性 HER2 阳性 (IHC 3+) 实体瘤成年患者的疗效进行了评估,这些患者参加了三项多中心试验之一:DESTINY-PanTumor02 (NCT04482309)、DESTINY-Lung01 (NCT03505710) 和 DESTINY- CRC02 (NCT04744831)。
三项试验的主要疗效结果指标是确认客观缓解率,另一个疗效指标是缓解持续时间。所有结果均由独立中央审评(ICR)基于RECIST v1.1标准进行评估。
1.在DESTINY-PanTumor02中,患者的客观缓解率为51.4%,中位缓解持续时间为19.4个月。
2.在DESTINY-Lung01中,客观缓解率为52.9%,中位缓解持续时间为6.9个月。
3.在DESTINY-CRC02中,客观缓解率为46.9%,中位缓解持续时间为5.5个月。
此次上市申请是基于正在进行的DESTINY-PanTumor02 II期试验的数据,其中Enhertu被证实了具有临床意义和持久的反应,可为既往治疗的表达 HER2 的转移性实体瘤患者带来临床意义的生存获益,包括胆管癌、膀胱癌、宫颈癌、子宫内膜癌、卵巢癌和其他肿瘤。
根据2023年欧洲肿瘤内科学会(ESMO)披露的数据,267例患者覆盖子宫内膜癌、宫颈癌、卵巢癌、膀胱癌、胆管癌等多个瘤种,客观缓解率为37.1%,中位缓解持续时间为11.3个月。
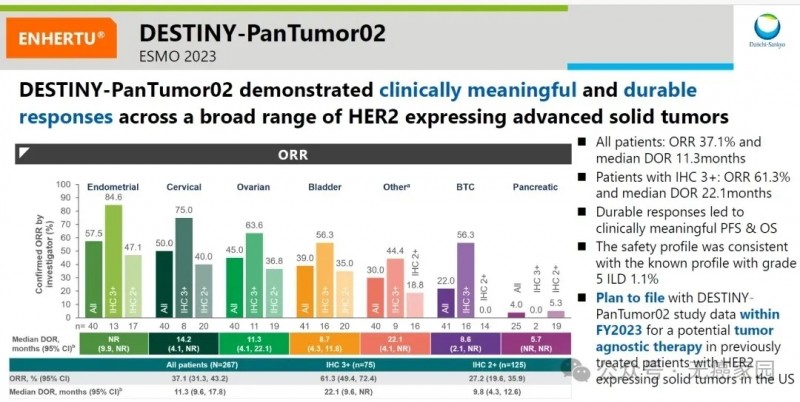
根据此次说明书公开的最新数据,DESTINY-PanTumor02的客观缓解率为51.4%,中位持续缓解时间为19.4个月。

对各不同瘤种的客观缓解率和缓解持续时间范围如图所示。
总之,基于此次获批,将有大批患者受益于Enhertu这款神奇的药物,肿瘤患者也将迎来革命性的疗效突破,有望迈入“治愈”的大门。再加上此前已经获批的HER2低表达乳腺癌、非小细胞肺癌、胃癌等适应症,Enhertu连续表现出佳绩,未来更加值得期待。
目前无癌家园正在展开的关于HER2阳性靶点的临床研究还有很多,例如GQ1001、C406、KN026、M108等药物等。
想要评估病情是否能够接受上述新药新疗法临床试验可将病理报告、治疗经历及出院小结等提交至医学部进行初步评估!
"靶向+化疗"强强联手,缔造抗癌新药Enhertu
Enhertu(DS8201,一种HER2抗体+伊立替康类化疗药物的偶联药物)属于ADC型药物类型(抗体偶联药物)。它有两部分组成:第一部分是针对HER2靶点的抗体,可以精准的识别并且结合HER2高表达甚至低表达的肿瘤细胞;第二部分是剧毒的化疗药伊立替康。这种设计会使抗体带着化疗药去找肿瘤细胞,然后精准地给肿瘤细胞下毒,毒死它们。
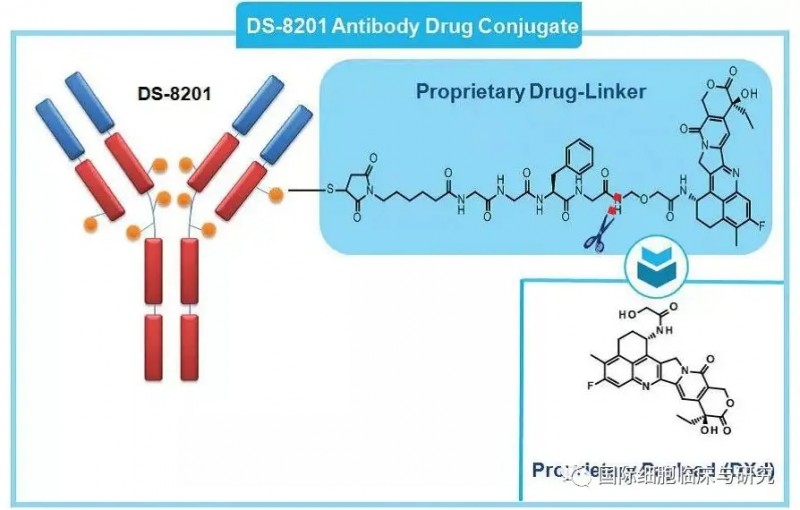
图为DS-8201的设计结构,图中橙色小圆球为化疗药(来源dsi.com)这种药物设计结合了靶向药的精准和化疗药的高效,既避免了全身使用化疗药的毒副作用,也比单独使用靶向药具有更强的杀伤能力,一举两得。
目前,Enhertu在美国FDA已经拿下五种适应症,其中最新适应症为HER2阳性(IHC 3+)的泛实体肿瘤。
SUMMARY/获批适应症
2019年12月21日,美FDA批准Enhertu上市,治疗接受过2种或以上抗HER2疗法的无法切除或转移性HER2阳性乳腺癌患者。
2021年1月15日,美FDA批准Enhertu用于既往接受过曲妥珠单抗治疗的局部晚期或转移性HER2阳性胃或胃食管交界(GEJ)腺癌患者。这是首个被批准治疗HER2阳性胃癌的ADC药物。
2022年4月27日,Enhertu再次获得FDA突破性疗法认证,用于治疗不可切除或转移性HER2低表达(IHC 1+或IHC 2+/ISH阴性)乳腺癌成年患者。
2022年8月12日,Enhertu获得FDA加速批准用于治疗携带HER2基因突变的不可切除或转移性非小细胞肺癌成人患者
如何检测HER2是精准治疗癌症的前提!
最后,小编在这里需要提醒大家的是,如何检测HER2是关键!
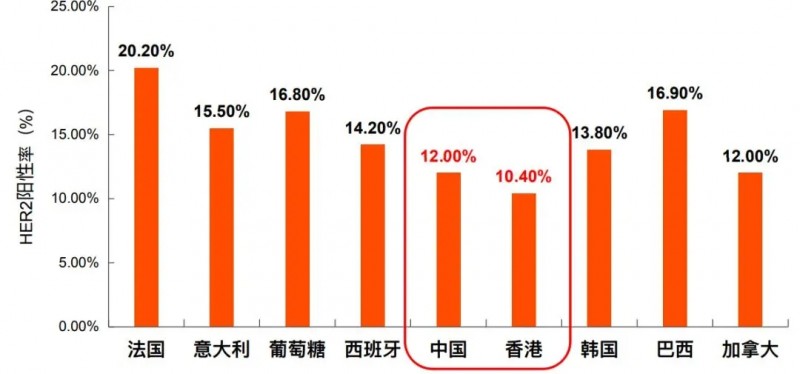
长期以来,IHC和FISH是检测HER2的金标准,临床上一项大型、非干预性、国际性流行病学研究(HER-EAGLE),共纳入4949例胃腺癌或胃食管结合部癌患者,旨在评估不同国家真实世界中的HER2阳性率 :结果显示,我国胃癌患者的HER2阳性率低于国外水平。传统的FISH/IHC遗漏将近50%的HER2/ERBB2改变!
因此,各位癌友们一定要慎重选择检测机构,如做过检测的病友可以联系医学部进行解读,评估可用的治疗方案。
参考文献
1.https://www.astrazeneca-us.com/media/press-releases/2024/enhertu-fam-trastuzumab-deruxtecan-nxki-granted-priority-review-in-the-us-for-patients-with-linkstatic-her2-positive-solid-tumors-01292024.html
2.https://www.ajmc.com/view/trastuzumab-deruxtecan-receives-fda-approval-for-her2-positive-solid-tumors







































 首页
首页 咨询
咨询 方舟新药
方舟新药 营养商城
营养商城