2024年AACR年会揭示CAR-T细胞免疫疗法治疗肾癌、胃癌、结直肠癌完全缓解长达3年
在本月举行的第115届美国癌症研究协会(AACR)年会上,公布了多项“CAR-T治疗实体瘤的突破性临床研究数据”,正式向胃癌、肾癌、结直肠癌等多款实体瘤宣战!
AACR作为全球知名的癌症研究盛会之一,与欧洲肿瘤内科学会(ESMO)、美国临床肿瘤学会(ASCO)并称为“全球三大癌症学会”,一直以来都是临床前沿研究成果的发布高地,见证着全球抗癌研究的发展与变革。
本次CAR-T治疗多款实体瘤的惊艳数据一经发布,无一例外的引起了广泛的关注,为抗癌圈带来了不小的震撼,这也意味着实体瘤患者未来将有更多的选择与希望!全球肿瘤医生网医学部小编盘点了本次会议上,值得关注的CAR-T治疗实体瘤三大进展,以供参考,希望为大家带来战胜癌症的信心!
CTX130治疗透明细胞肾细胞癌,获长期完全缓解(CR)
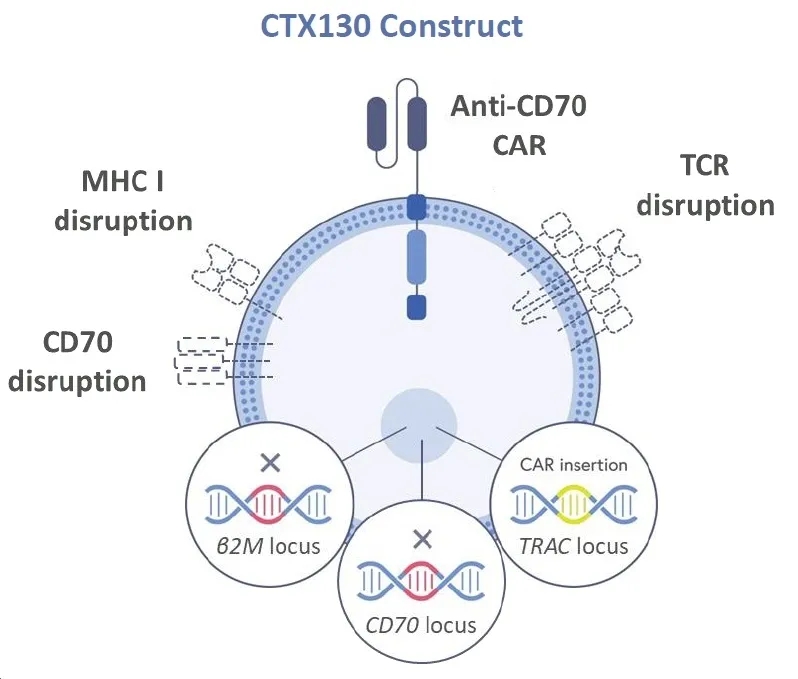
▲图源“BMJ”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
2024 AACR:CR首达3年之久
在2024 AACR年会上,报告了CTX130™(一种CD70靶向的同种异体CAR-T细胞疗法),治疗透明细胞肾细胞癌(ccRCC)的1期临床研究结果。本次共入组16名IV期透明细胞肾细胞癌患者,中位年龄为63岁(范围,53-77岁),既往接受过中位数3种治疗(范围,1-6)。这些患者在入组后,先接受标准淋巴细胞清除治疗(环磷酰胺+氟达拉滨),之后输注CTX130。截至2023年10月9日,结果显示如下:
1、完全缓解(CR):1例患者(6.3%)实现完全缓解(CR),现已在3年(36个月)的随访中,持续出现CR。
2、病情稳定(SD):75%(12例患者)达到病情稳定(SD),其中1例患者病情稳定超过18个月。
3、疾病控制率(DCR):DCR高达81.3%。
综上,本次最新研究结果,强化了CTX130卓越的安全性及抗肿瘤活性。目前,持久CR(完全缓解)已超过3年,这是同种异体CAR-T细胞疗法在难治性实体瘤中首次出现,同时也是CR持续时间最长的一次!
2022 SITC:患者CR持续18个月!
其实,早在2022年第37届癌症免疫治疗学会年会(SITC)上,就曾报道过CTX130,治疗透明细胞肾细胞癌(RCC)的病例分析。
这位64岁男性,于2017年确诊透明细胞肾细胞癌,既往接受过阿替珠单抗、卡博替尼治疗后病情复发,肺部和胸膜出现转移病灶。考虑到他的病情符合入组标准,随后参加了CTX130治疗肾细胞癌的1期临床试验(NCT04438083)。结果如下:
该患者经CTX130治疗后,获得部分缓解(PR),更为惊喜的是,他在治疗第3个月竟然实现完全缓解(CR),而且在第18个月复查时,依然保存CR状态!据悉,这是异基因CAR-T细胞,首次实现这种持久的完全缓解(CR)!
图1 该患者在回输CTX130前、治疗第42天、第18个月时的影像学对比
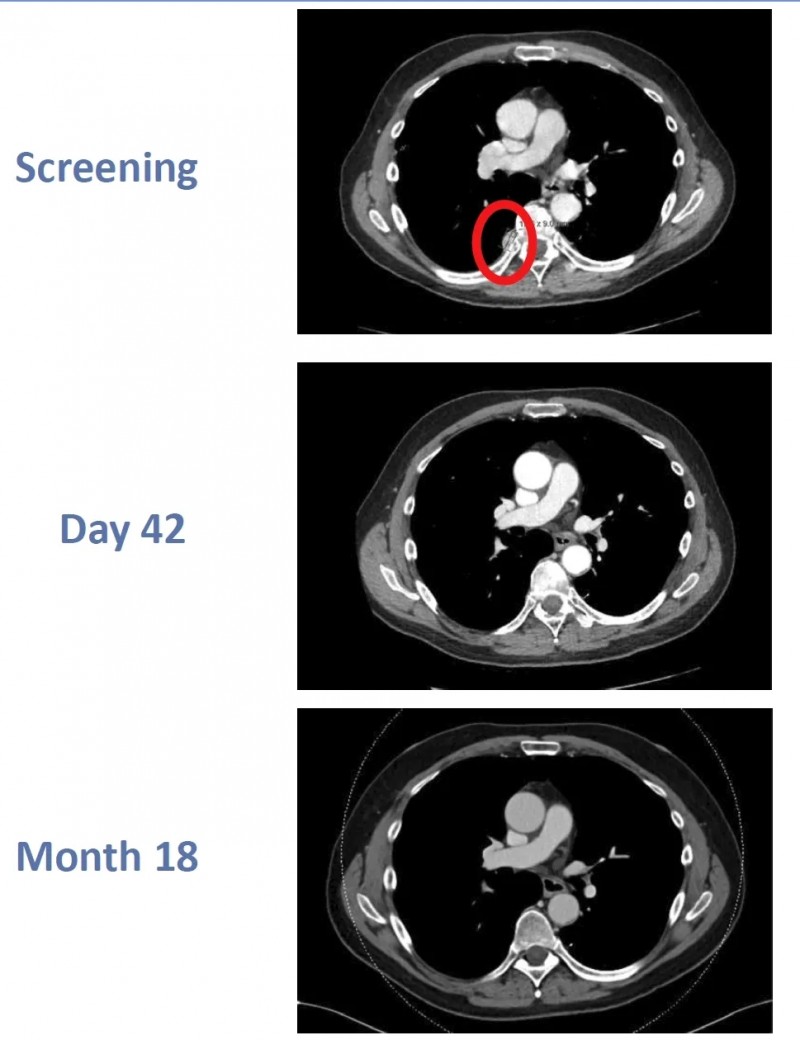
▲图源“BMJ”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
中国患者如何寻求CAR-T治疗帮助?
目前目前正有多款CAR-T临床试验正在招募中,主要针对结直肠癌、胃癌、胰腺癌、肝癌、间皮瘤、卵巢癌、T细胞淋巴瘤、非霍奇金淋巴瘤、T细胞白血病(T-ALL)、B细胞淋巴瘤等癌种!想参加的患者,可按如下进行申请:
1、按要求将完整的病理检查报告、病史资料等资料,提交至医学部;
2、医学部进行初步评估后,将为患者匹配合适的临床试验;
3、向相应的试验中心,提交患者的病历资料;
4、评估通过后,协助患者参加临床试验。
EpCAM CAR-T治疗胃癌等上皮性肿瘤,安全可行
2024 AACR:胃癌疾病控制率(DCR)高达90.0%!
上皮细胞粘附分子(EpCAM)是一种跨膜糖蛋白,在上皮和上皮源性肿瘤(如胃癌、结直肠癌、胰腺癌、肺癌等)中高表达,与这些肿瘤的复发和转移密切相关。因此,EpCAM被美国食品和药物管理局(FDA)批准作为肿瘤的诊断标记物。
本次AACR大会上公布的数据显示,EpCAM CAR-T在胃癌治疗中展现出良好的疗效,本次1期临床试验结果显示,胃癌组的客观缓解率(ORR)达到20.0%,疾病控制率(DCR)更是高达90.0%!
上皮性肿瘤1期临床研究:3例患者无进展生存超700天
此前,我国也进行过EpCAM CAR-T的相关研究,在一项关于“EpCAM CAR-T治疗上皮性肿瘤的1期临床试验(NCT02915445)”中,入组12例III期或IV期晚期EpCAM阳性的上皮性肿瘤(包括胃癌、结肠癌、直肠癌等)患者,中位年龄为54.9岁(27.2~69.6岁)。其中10例患者在治疗前已发生转移,7例患者接受根治性切除加化疗,5例患者仅接受化疗。所有入组患者在入组后,先接受环磷酰胺+氟达拉滨预处理化疗,之后采用递增剂量给予EpCAM-CAR-T细胞治疗。
结果显示,5例患者在治疗后保持病情稳定(SD)状态;2例患者获得部分缓解(PR);3例患者无进展生存期(PFS)超过23个月(约700天)!而且所有患者均未出现治疗相关的细胞因子释放综合征(CRS)。
其中,2例患者(10号和3号患者)观察到肿瘤消退的证据(详见图3)。尤其是10号患者,通过腹膜接受了一次高剂量T细胞输注,治疗7个月后腹膜肿瘤得到缓解(详见图3),表明CAR-T细胞在10号患者中,具有长期持续性。而3号患者也在治疗3个月后,实现了部分缓解(详见图2+3)。
图2 入组患者的疾病进展、实质性治疗及现状
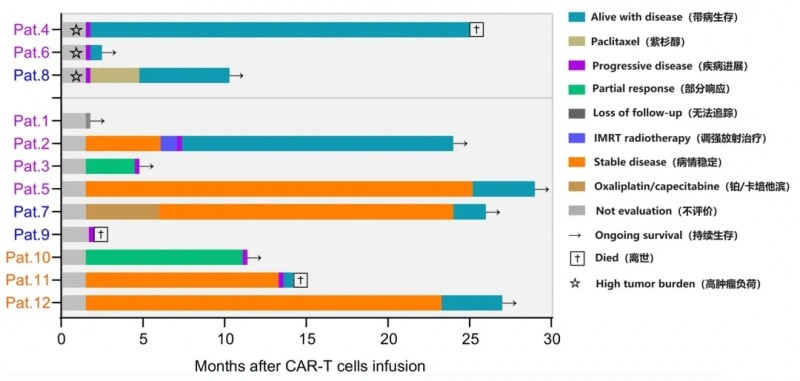
▲图源“Sci Adv”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
图3 计算机断层扫描显示,10号和3号患者EpCAM-CAR-T治疗后的肿瘤反应
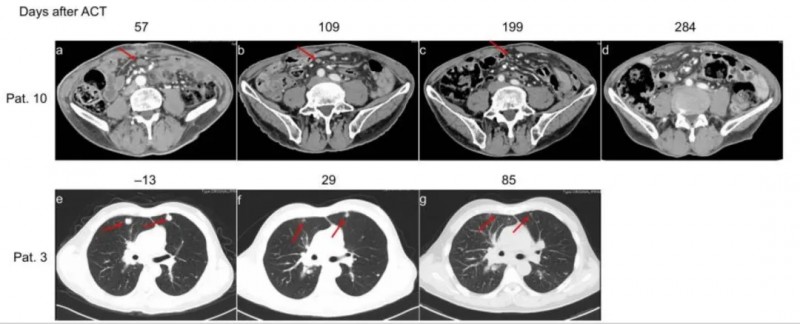
▲图源“Sci Adv”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
注:红色箭头代表肿瘤部位。
2024 AACR:GCC19 CAR-T细胞治疗结直肠癌,客观缓解率(ORR)达50%
GCC19 CAR-T是一款靶向GCC的自体CAR-T产品,用于治疗晚期结直肠癌。GCC即“鸟苷酸环化酶-C”,在70%~80%的结直肠癌患者的转移灶中表达,且主要局限于肠道。
据本次AACR报道,2022年8月,美国启动了一项针对标准化疗难治性转移性结直肠癌患者的1期临床研究(NCT05319314),截至2023年11月1日,已有4例患者入组接受了初始剂量水平的GCC19 CAR-T细胞治疗。结果显示:
1、根据独立审查:客观缓解率(ORR)达50%(2/4)。2例患者达到部分缓解(PR),另1例患者达到病情稳定(SD),在PET/CT上显示部分代谢缓解(PMR)。
2、根据研究中心研究者的审查:ORR达25%,其中1例确认PR,3例SD被评估为最佳缓解。剂量水平1(即低剂量组,1x106细胞/kg)的中位无进展生存期(PFS)为3.8个月。
小编寄语
CAR-T疗法在血液肿瘤治疗领域的战绩颇丰,国内外先后有多款产品获批上市,为白血病、淋巴瘤、骨髓瘤等多款复发或难治性血液肿瘤患者带来了“生”的希望!然而,CAR-T细胞在治疗实体瘤领域,存在靶点局限、细胞难以浸润到肿瘤区域等限制,也在一定程度上制约了CAR-T疗法的发展。因而,如何高效、安全地利用CAR-T细胞治疗实体瘤,一直是各国学者急需攻克的抗癌关键课题。
值得欣慰的是,近年来已有多项CAR-T治疗实体瘤的临床试验正在如火如荼地开展,其中也不乏幸运患者获得完全缓解。尤其是随着2024年AACR数据的公布,更是为免疫细胞疗法的发展打了一剂“强心针”,CAR-T攻克晚期实体瘤未来可期!全球肿瘤医学部小编也将持续关注,并及时更新CAR-T治疗实体瘤的更多重要进展,让更多的实体瘤患者从中获益!小编坚信只要不放弃希望,曙光终将来临!如果您对目前的治疗方案存疑,或想寻求CAR-T疗法、TIL、TCR-T、CAR-NK等国内外其他新兴抗癌技术的帮助,可联系医学部,详细评估病情或申请国内外专家会诊。
参考资料
[1]Pal S K, Tran B, Haanen J B,et al.Abstract CT002: CTX130 allogeneic CRISPR-Cas9-engineered chimeric antigen receptor (CAR) T cells in patients with advanced clear cell renal cell carcinoma: Long-term follow-up and translational data from the phase 1 COBALT-RCC study[J]. Cancer Research, 2024, 84(7_Supplement): CT002-CT002.
https://aacrjournals.org/cancerres/article/84/7_Supplement/CT002/742428/Abstract-CT002-CTX130-allogeneic-CRISPR-Cas9?searchresult=1
[2]Pal S,et al.558 CTX130 allogeneic CRISPR-Cas9–engineered chimeric antigen receptor (CAR) T cells in patients with advanced clear cell renal cell carcinoma: results from the phase 1 COBALT-RCC study[J]. 2022.
https://jitc.bmj.com/content/10/Suppl_2/A584
[3]Luo T I,et al.Abstract CT069: Targeting EpCAM via CAR T-cells is an effective treatment for gastric cancer patients and subsequent toll-like receptor signaling activation in CD36+ monocyte underlies the resulting cytokine release syndrome[J]. Cancer Research, 2024, 84(7_Supplement): CT069-CT069.
https://aacrjournals.org/cancerres/article/84/7_Supplement/CT069/742501/Abstract-CT069-Targeting-EpCAM-via-CAR-T-cells-is?searchresult=1
[4]Li D,et al.EpCAM-targeting CAR-T cell immunotherapy is safe and efficacious for epithelial tumors. Sci Adv. 2023 Dec;9(48):eadg9721.
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC10691766/
[5]Keenan B P,et al.Abstract CT129: A phase 1 dose escalation study of a novel coupled CAR T cell therapy, GCC19CART, for patients with linkstatic colorectal cancer[J]. Cancer Research, 2024, 84(7_Supplement): CT129-CT129.
https://aacrjournals.org/cancerres/article/84/7_Supplement/CT129/742392/Abstract-CT129-A-phase-1-dose-escalation-study-of?searchresult=1







































 首页
首页 咨询
咨询 方舟新药
方舟新药 营养商城
营养商城