中国"初代"TCR-T细胞疗法,携二期惊艳数据,二战ASCO!客观缓解率远超预定疗效
2024年6月1日,我国初代针对“晚期软组织肉瘤”的TCR-T产品-TAEST16001,II期临床试验数据,惊艳亮相2024年度美国临床肿瘤学会年会(ASCO)。据悉,这款TCR-T产品的临床试验由北京大学肿瘤医院和广州中山大学肿瘤防治中心作为牵头单位共同开展,目前I期临床试验已完成,国内多家临床机构正在参与II期临床试验。
ASCO年会作为全球肿瘤治疗领域的盛会,其规模、学术水平和权威性首屈一指,汇集了世界一流的肿瘤学专家及全球近期肿瘤学科研成果,今年共收到了超过7000份的研究摘要投稿。值得骄傲的是,我国多款抗癌新药及抗癌新技术(如TCR-T、CAR-T、TIL疗法)杀出重围,在国际舞台脱颖而出,充分显示了我国在前沿抗癌领域的研究进展和成就,获得国际顶级学术会议的认可。
中国"初代"TCR-T细胞产品,惊艳亮相2024 ASCO大会
TAEST16001 TCR-T,重拳出击软组织肉瘤
TAEST16001是由我国香雪生命科学自主研发的一款TCR-T细胞免疫治疗产品,使用慢病毒作为载体,对患者自身的T细胞进行基因修饰,赋予它们一个“工程”高亲和力NY-ESO-1特异性的t细胞受体(TCR),然后将这些修饰过的T细胞,回输到患者体内,以达到抗癌效果。
TAEST16001是中国首个获得国家药品监督管理局药品审评中心IND批件,并开展临床研究的TCR-T细胞产品!适用于表达NY-ESO-1抗原且HLA-A*02:01阳性的晚期软组织肉瘤。其中,“NY-ESO-1抗原”即“纽约食管鳞状细胞癌1抗原”,通常在睾丸内的生殖细胞中表达,但在其他各类癌种(如滑膜肉瘤、粘液样/圆细胞脂肪肉瘤)中,也可能存在高表达。
▲截图源自“NMPA官网”
TAEST16001的I期临床试验早在2022年,就已亮相ASCO大会,并获得国际同行认可。本次II期临床试验的阶段性总结数据,再次以学术海报形式,亮相2024年度的ASCO年会。
▼中国团队在ASCO会议现场
▲图源“香雪生命科学技术官网”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
近半数患者获部分缓解,客观缓解率远超预定目标

▲截图源自“ASCO Publications”
截至2024年4月,TAEST16001的II期临床试验(NCT05549921)共入组8例患者,中位年龄为37.5岁(28~49岁)。这些患者在入组后,首先接受淋巴细胞清除化疗(氟达拉滨+环磷酰胺),之后回输TAEST16001 TCR-T细胞,最后接受白细胞介素-2(IL-2)治疗。
经过至少两次肿瘤评估后,结果显示:50%(4例)的患者获得部分缓解(PR),37.5%(3例)患者达到病情稳定(SD)。TAEST16001的安全性良好,疗效数据令人鼓舞,截至统计日期止,客观缓解率(ORR)达到50%,远超出预先设定的目标疗效(ORR=25%)。中位无进展生存期(PFS)为5.9个月。初始缓解中位时间达1.1个月(1.1~2.2),缓解持续时间的中位时间长达5.0个月(1.5~8.8)。
▼一例48岁滑膜肉瘤患者,TAEST16001治疗前后影像学对比
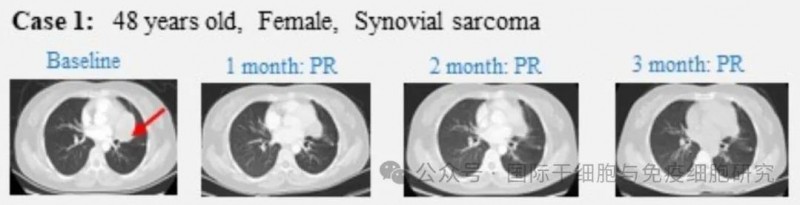
▲图源“ASCO”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
如何寻求TCR-T疗法帮助
目前有多款在研的TCR-T疗法,正在招募患者,主要针对头颈部肿瘤、乙型肝炎病毒相关肝细胞癌、肛门癌、头颈部肿瘤(喉癌、口腔癌)、妇科恶性肿瘤(宫颈癌、卵巢癌)等多款实体瘤。
想参加的患者可将近期病理报告、治疗经历、出院小结等资料汇总后,提交至医学部,进行初步评估,或了解详细的入排标准!
2024 ASCO:多重TCR-T(T-Plex)疗法,剑指多款实体瘤

▲截图源自“ASCO Publications”
除了我国的这款TAEST16001 TCR-T疗法外,在2024年ASCO年会上,还有另一款新型TCR-T疗法——“T-Plex”备受瞩目。
由于复杂的生物学特性,晚期恶性实体肿瘤一直难以攻克。一方面,实体瘤具有异质性,靶抗原表达可变,故而针对单一抗原的TCR-T细胞反应率(30%~50%)及持久性(3~4个月)有限;另一方面,实体瘤缺乏足够的内源性抗肿瘤T细胞,会阻碍免疫应答、抑制肿瘤微环境,即使在免疫检查点抑制剂存在的情况下亦是如此。
而T-Plex有望打破传统TCR-T的限制,T-Plex是一种多重细胞疗法,包含2~3种不同的TCR-T细胞。针对实体瘤中不同和常见HLA类型(T-Plex)的常见共同抗原,施用多种增强型TCR-T细胞;通过CD8a/b和显性阴性TGFb受体的共同递送作用,增强肿瘤杀伤力,并维持长期的抗癌疗效。
本次ASCO大会公布了T-Plex的筛选研究(NCT05812027)及第1阶段研究(NCT05973487)的初步数据。从2023年9月到摘要提交时,共有149例不同实体瘤(包括黑色素瘤、头颈癌、非小细胞肺癌、卵巢癌等)患者参加了筛选方案,在完成靶标筛选的患者中,92%表达至少一个靶标,65%符合至少一个TCR-T治疗的条件。
其中,参与治疗研究的首位受试者已接受了T-Plex(TSC-203A0201)治疗,该药物用于治疗靶向PRAME的转移性皮肤黑色素瘤,目前该患者未出现急性毒性反应。
初步数据表明,截至目前评估的大多数实体瘤患者,免疫库中的HLA和靶标组合可产生≥1个TCR-T匹配,许多患者符合多重TCR-T治疗的条件。目前还有3例受试者的药物生产正在进行中,让我们拭目以待其效果!
▼TCR-T选择与实体瘤患者数量之间的关系
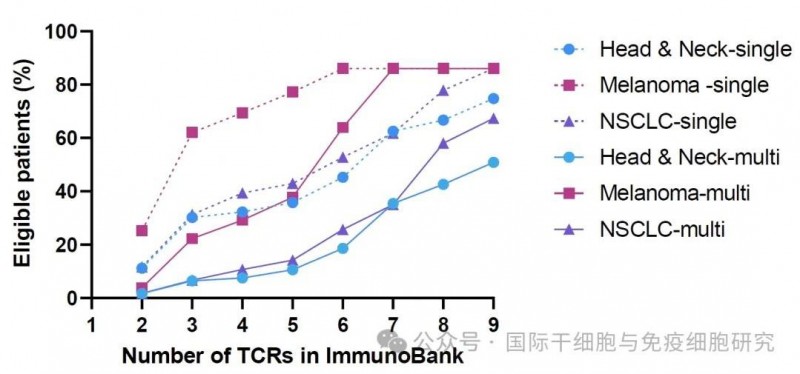
▲图源“Journal of Clinical Oncology”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
注:随着TCR-T选择数量的增加,适合单一治疗(虚线)或多重治疗(实线)的实体瘤患者数量增加。
TCR-T疗法:在实体瘤治疗领域杀出一条"血路"
实体瘤新利器:TCR-T细胞疗法
T细胞疗法主要包括CAR-T细胞疗法、TCR-T细胞疗法等,它们各有所长。
其中,CAR-T疗法是通过对患者的T细胞进行基因改造,以表达针对目标肿瘤细胞表面特定抗原的CAR,相当于在T细胞上安装一个“导航头”,主要用于血液肿瘤的治疗,但在治疗实体肿瘤方面存在一定的局限性。
然而,实体肿瘤占所有癌症患者的95%。而TCR-T疗法(T细胞受体工程化T细胞疗法),是利用基因工程技术对T细胞进行改造,相当于给T细胞安装一个“精密的感知器”,利用天然的TCR,来靶向细胞内蛋白质,以便精准识别并杀死狡猾的癌细胞,主要用于治疗实体瘤。
TCR-T疗法作为一种新型的抗肿瘤方案,自1988年尝试用于增强免疫系统以来,已历经30余载的发展,具有安全性良好、归巢能力强等优点。由于抗原肽来源于蛋白质降解,因此TCR可以接触整个蛋白质组作为潜在靶标,相当于T细胞功能的“守门人”,弥补了CAR-T疗法在治疗实体瘤方面的“短板”。
TCR-T疗法目前在治疗滑膜肉瘤、黑色素瘤、肝癌、非小细胞肺癌、头颈癌、卵巢癌等多款实体瘤领域,均展现了不俗的实力,为实体瘤及对免疫检查点抑制剂无反应的患者提供了新的希望与选择!
“到目前为止,TCR-T疗法非常安全,几乎没有细胞因子释放综合征,也没有神经毒性,就像CAR-T疗法中看到的那样,是一种令人兴奋的新疗法!”
——弗雷德哈金森癌症研究中心副教授Aude Chapuis
(奥德·查普伊斯)博士
我国TCR-T疗法百家争鸣,向多款实体瘤"亮剑"
近年来,我国TCR-T疗法的研发呈现百家争鸣的局势,不仅吸引了多家药企(如香雪生命、百吉生物、来恩生物、星汉德等)布局,而且有多款TCR-T产品的新药IND相继获批,精准打击多款实体瘤!
1、CRTE7A2-01
北京可瑞生物科技公司研发的一款TCR-T细胞注射液——“CRTE7A2-01”的临床新药IND,于2023年8月25日,获国家药品审评中心(NMPA)批准,用于HPV16阳性晚期宫颈癌、头颈部肿瘤等多款实体瘤的治疗,具有良好的抗肿瘤活性。此外,该药已通过美国食品药品监督管理局(FDA)的临床申请(NCT05122221),预计于2024年11月完成I期试验。
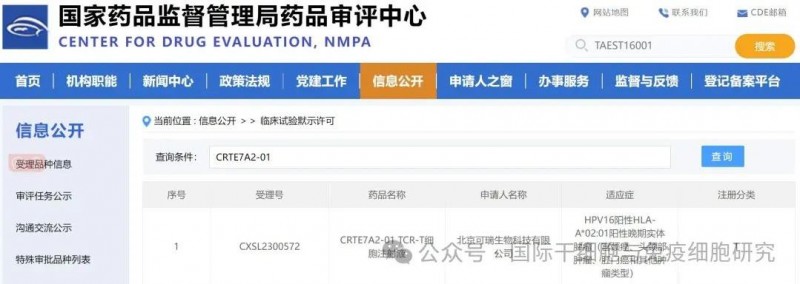
▲截图源自“NMPA官网”
2、TC-N201注射液
由广东天科雅生物医药公司研发的一款TCR-T产品——“TC-N201注射液”的临床试验申请(IND),于2022年11月28日,获国家药监局审查中心批准,用于既往治疗失败的复发或转移性(LA-A2和NY-ESO-1阳性)实体瘤的治疗。
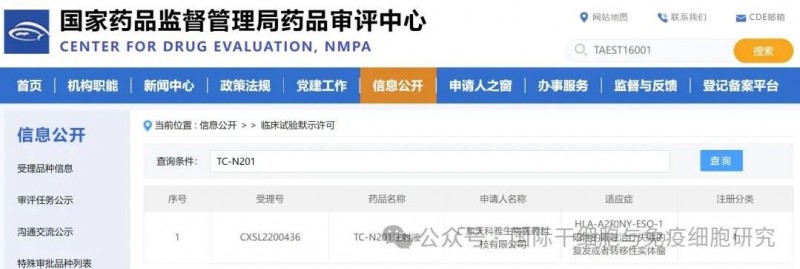
▲截图源自“NMPA官网”
3、TAEST1901
“TAEST1901注射液”是由香雪生命科学公司研发的另一款创新型TCR-T产品,其临床新药IND于2022年4月20日,获中国国家药监局药品评审中心(NMPA)批准,用于晚期肝癌或其它晚期肿瘤(HLA-A*02:01、肿瘤抗原AFP表达阳性)的治疗。

▲截图源自“NMPA官网”
小编寄语
我国新型TCR-T细胞产品-TAEST16001,本次能在7000多个项目中脱颖而出,携着二期临床数据成功突围本次ASCO盛会,也让我们看到了TCR-T疗法在实体瘤治疗领域的应用潜力。如果说CAR-T疗法是治疗血液肿瘤的利器,那么TCR-T疗法就是治疗实体瘤的新型武器,其在实体瘤治疗领域的独特优势不容小觑,我们也期望未来会有越来越多的TCR-T细胞产品问世,让更多的癌症患者获益!
好消息是,目前有几款在研的TCR-T疗法正在招募患者,想寻求TCR-T疗法或国内外其他抗癌新技术帮助的病友,可将近期病理报告、影像学资料、治疗经历等相关资料,提交至医学部,进行初步评估。
参考资料
[1]Liu J,et al.Phase IIA study of high-affinity TCR-T (TAEST16001) targeting NY-ESO-1 in soft tissue sarcoma[J].2024.
https://ascopubs.org/doi/10.1200/JCO.2024.42.16_suppl.11548
[2]Liu J,et al.Phase IIA study of high-affinity TCR-T (TAEST16001) targeting NY-ESO-1 in soft tissue sarcoma[J].2024.
https://clin.larvol.com/trial-detail/NCT05549921
[3]Thomas S S,et al.Initial data from a phase 1, first-in-human clinical trial for T-Plex, a multiplexed, enhanced T cell receptor-engineered T cell therapy (TCR-T) for solid tumors[J].2024.
https://ascopubs.org/doi/10.1200/JCO.2024.42.16_suppl.2542
[4]Zhao X,et al.The recent advancement of TCR-T cell therapies for cancer treatment[J]. Acta Biochimica et Biophysica Sinica,2024.
https://www.sciengine.com/ABBS/doi/10.3724/abbs.2024034;JSESSIonID=c47e4d4e-a00d-4b3f-ba14-3b2448009deb
[5]https://www.cgtlive.com/view/chapuis-improving-tcr-t-cell-therapies-cancer-treatment
[6]https://www.xphcn.com/about/info_16.aspx?itemid=18095
[7]https://www.cde.org.cn/main/xxgk/listpage/4b5255eb0a84820cef4ca3e8b6bbe20c







































 首页
首页 咨询
咨询 方舟新药
方舟新药 营养商城
营养商城