2024年4月5日FDA批准CAR-T细胞疗法西达基奥仑赛(Carvykti、cilta-cel)用于治疗复发或难治性多发性骨髓瘤
2024年4月5日,传奇生物的CAR-T疗法达基奥仑赛(Ciltacabtagene Autoleucel、Carvykti、cilta-cel)获得美国食品药品监督管理局(FDA)批准,用于治疗复发或难治性多发性骨髓瘤(RRMM)患者。这一突破性疗法为多发性骨髓瘤患者带来了新的希望,标志着多发性骨髓瘤治疗进入了一个新的时代。
获批依据
西达基奥仑赛的获批主要基于CARTITUDE-4研究的积极结果,这是一项国际、随机、开放标签的3期临床试验,旨在评估西达基奥仑赛与标准治疗方案(泊马度胺、硼替佐米和地塞米松[PVd]或达雷妥尤单抗、泊马度胺和地塞米松[DPd])在既往接受过一至三线治疗的复发且来那度胺耐药的多发性骨髓瘤成人患者中的疗效和安全性。
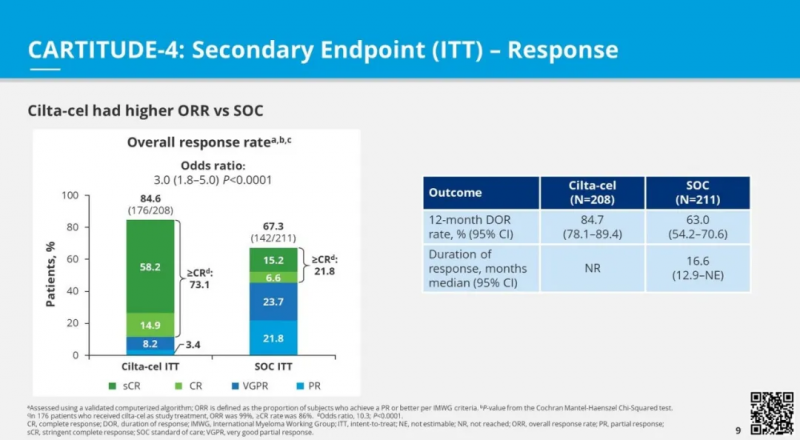
研究结果
●显著改善无进展生存期(PFS):中位随访期达15.9个月时,西达基奥仑赛治疗组PFS为76%,而标准治疗组仅为49%(HR0.26;P<.0001),达到主要临床终点;
●更高的缓解率:西达基奥仑赛治疗组在总体可测量残留疾病(MRD)、客观缓解率(ORR)、完全缓解(CR)等次要终点中均展现出显著提高;
●良好的安全性:西达基奥仑赛治疗组耐受性良好,安全性特征与已知一致。
西达基奥仑赛
西达基奥仑赛是全球首个且唯一获批用于多发性骨髓瘤患者二线治疗的BCMA靶向疗法,包括CAR-T疗法、双特异性抗体和抗体药物偶联物(ADC)。这意味着更多患者能够在早期治疗方案中受益于这一个性化免疫疗法,延缓疾病进展,改善生活质量。
西达基奥仑赛的突破性优势
西达基奥仑赛的获批具有以下突破性优势:
●疗效显著:CARTITUDE-4研究结果显示,西达基奥仑赛能够显著改善复发或难治性多发性骨髓瘤患者的PFS,延长生存期;
●安全性良好:西达基奥仑赛的安全性特征与已知一致,患者耐受性良好;
●个性化治疗:CAR-T疗法是一种个性化免疫疗法,能够精准识别并消灭肿瘤细胞,减少对正常细胞的损伤;
●二线治疗选择:西达基奥仑赛为复发或难治性多发性骨髓瘤患者提供了新的治疗选择,填补了治疗空白。
西达基奥仑赛的获批历程
西达基奥仑赛的获批历程如下:
2022年2月28日:西达基奥仑赛在美国获批上市,用于治疗既往接受过至少四线治疗的复发或难治性多发性骨髓瘤成人患者;
2023年:西达基奥仑赛相继获批在欧盟、日本上市;
2024年4月5日:西达基奥仑赛获得FDA批准,用于治疗复发或难治性多发性骨髓瘤患者,成为首个二线治疗BCMA靶向疗法。
西达基奥仑赛的未来展望
西达基奥仑赛的获批标志着多发性骨髓瘤治疗进入了一个新的时代,未来,西达基奥仑赛有望惠及更多患者,改善患者生活质量,延长生存期,传奇生物将继续致力于细胞疗法的研究与开发,为癌症患者带来更多希望。







































 首页
首页 咨询
咨询 方舟新药
方舟新药 营养商城
营养商城