我国顺利开展全球首例肺癌CAR-NK细胞疗法临床试验,晚期癌症患者有救了,ORR可达100%
据“网易新闻2024年8月11日”报道,我国已正式开启CAR-NK细胞在肺癌患者群体中的临床试验,目前已完成全球首例患者的输注。
CAR-NK细胞为癌症患者树立起了抗癌的第一道天然细胞屏障,且费用减少至CAR-T细胞的一半,为肺癌等晚期癌症患者带来了新的希望与选择!

▲截图源自“网易视频”
CAR-NK疗法:CAR和NK细胞的强强联合
NK细胞是免疫系统中的一种淋巴细胞,在人体防御肿瘤和病毒感染中发挥着至关重要的作用。具有区分健康细胞和恶性细胞的天然能力,从而降低了自身免疫反应和附带损害的风险。
而CAR-NK细胞疗法是利用基因工程技术,在NK细胞上安装一个“CAR导航头(一种人工修饰的融合蛋白)”,使其在保留NK细胞原有抗癌战斗力的同时,又能将打击目标精准锁定在癌细胞的特定抗原蛋白上,使狡猾的癌细胞无处可藏,最终达到精准抗癌的目的。与CAR-T等其他免疫细胞疗法相比,CAR-NK细胞疗法的显著优势是能高特异性靶向癌细胞,同时最大限度地减少脱靶效应。
▼CAR-NK细胞的治疗过程
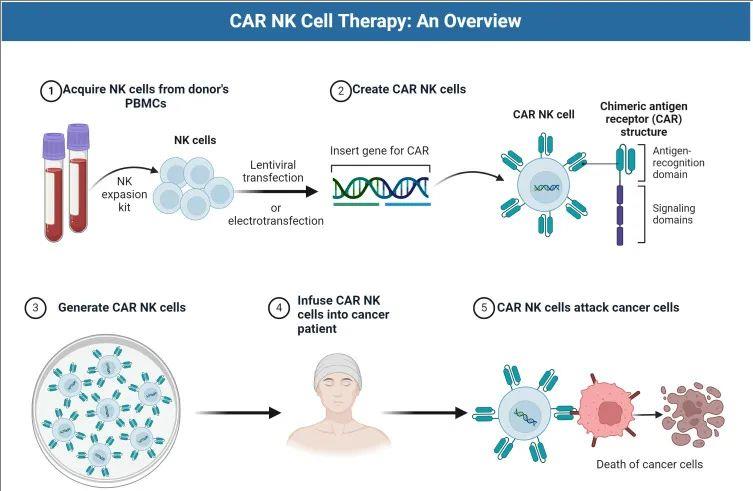
▲图源“Front Oncol”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
▼CAR-NK细胞治疗实体肿瘤的临床研究汇总
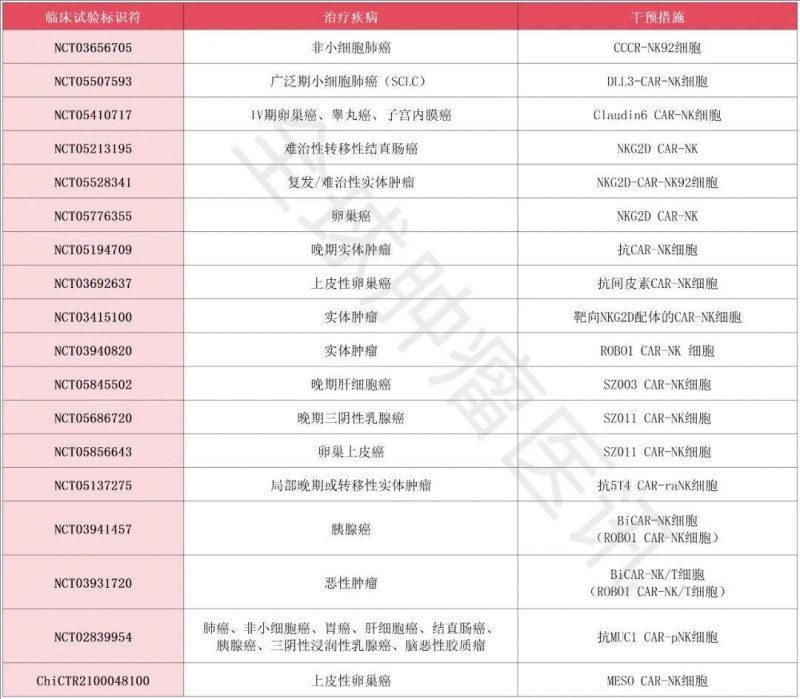
▲数据源自“nature”,全球肿瘤医生网医学部整理汇总
如何寻求CAR-NK疗法帮助?
目前有多款在研的CAR-NK疗法,正急招非小细胞肺癌、肾细胞癌、急性髓系白血病、复发或难治性多发性骨髓瘤等多款癌种,对此感兴趣的病友,可将治疗经历、近期病理报告、影像学资料等,提交至医学部,了解详细的入排标准或进行初步评估。
改良版CAR-NK:肺癌脑转移中初见疗效,肿瘤病灶缩小12mm
肺癌作为发病率很高的一类癌症,是全球面临的重大健康挑战,截至2023年,全球约有238,340例肺癌新发病例(男性117,550例,女性120,790例)。CAR-NK细胞疗法保留了NK细胞浸润实体肿瘤的天然能力,加上CAR靶向的特异性,与传统疗法相比具有降低CRS和GvHD风险、通过先天免疫机制靶向和杀死癌细胞等潜在优势,为肺癌患者提供了一种新型选择。
▼CAR-NK疗法治疗肺癌的潜在靶点
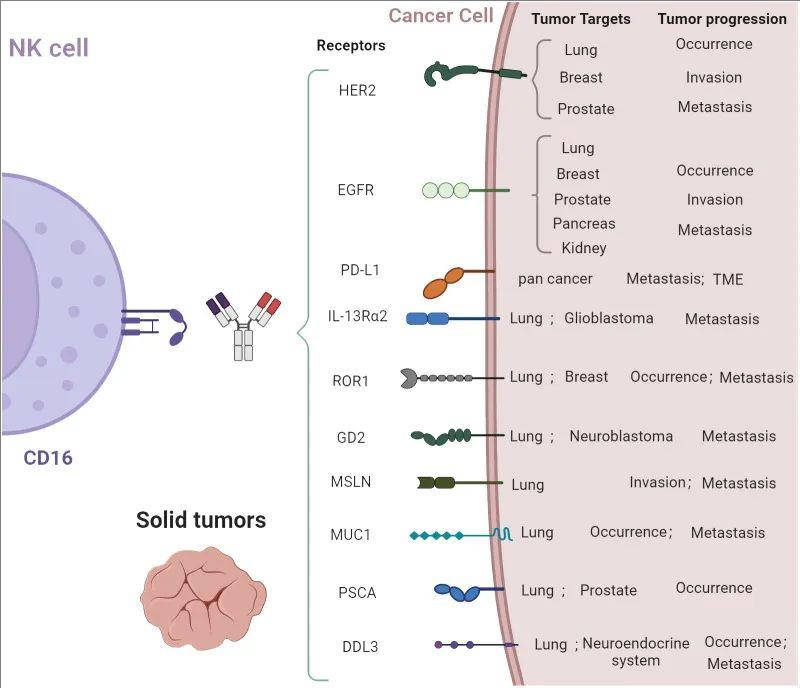
▲图源“Front Oncol”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
我国还曾进行过一项应用“改良版CCCR-NK92细胞,治疗晚期非小细胞肺癌(NSCLC)脑转移的临床研究(NCT03656705)”。
一位69岁非小细胞肺癌(NSCLC)的女性患者,基因检测提示肺组织Exon-19 19-del突变、T790突变,PD-L1表达≥1%,影像学检查提示颅内转移。既往接受过吉非替尼、奥希替尼、头部放疗、靶向治疗及局部放疗,后因担心副作用拒绝化疗,并入组接受CCCR-NK92细胞治疗。
治疗后结果显示,CCCR-NK92细胞对肿瘤有一定的疗效,肿瘤病灶出现缩小表现。CT图像显示,左肺包裹性胸腔内液由46.22mm,减少至33.59mm(图1A、C),前气管-后腔静脉间质面积淋巴结由11.3mm,减少至8.55mm(图1B、D)。
图1 CCCR-NK92细胞治疗前后CT图像对比
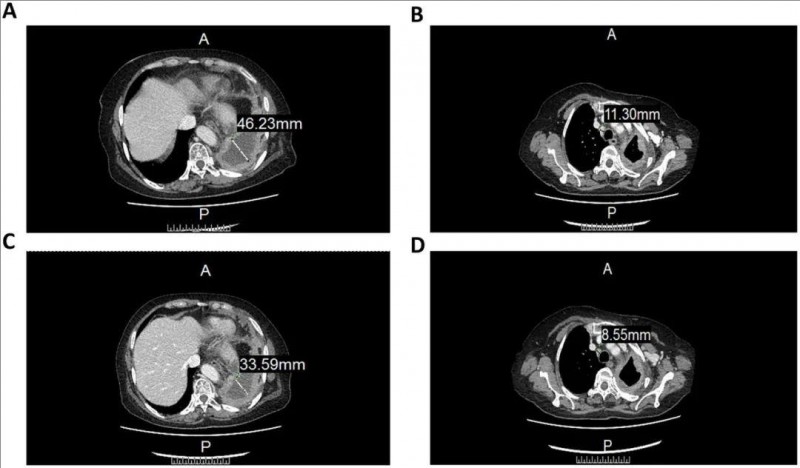
▲图源“Sage Journals”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
注:
①图A:CCCR-NK92细胞,治疗前CT图像。
②图B:一轮CCCR-NK92细胞治疗后的CT图像。
③图C:一轮细胞治疗后的CT图像。
④图D:两轮细胞治疗后的CT图像。
CAR-NK细胞重击胶质母细胞瘤,中位总生存期可长达135周
CAR-NK细胞除了治疗非小细胞肺癌外,在脑胶质母细胞瘤方面也取得了不俗的效果。Ⅰ期临床研究共入组9例复发性HER2阳性胶质母细胞瘤(GB)患者,医生在这些患者复发手术期间,沿手术腔边缘注射CAR-NK细胞,结果显示:
1、病情稳定及假性进展:影像学检查显示,56%(5例)的患者在复发手术和持续7~37周的CAR-NK治疗后,达到病情稳定(SD)。另2例患者在注射部位出现了假性进展,提示存在治疗所诱导的免疫反应。其中,1例患者在CAR-NK注射后第12周,复查MRI显示,切除边缘切除边缘周围,出现斑点状对比增强,并在接下来的几周内消失,可能与诱导的免疫反应相关,无需进一步治疗(详见下图)。
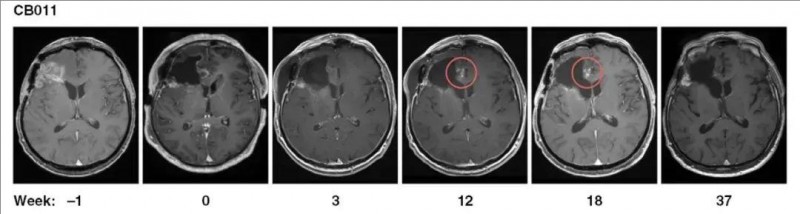
▲图源“Neuro-Oncology”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
2、中位总生存期(OS):所有入组患者(n=9)的中位总生存期(OS)为31周。而出现假性进展的2例患者其OS分别为135周、98周。
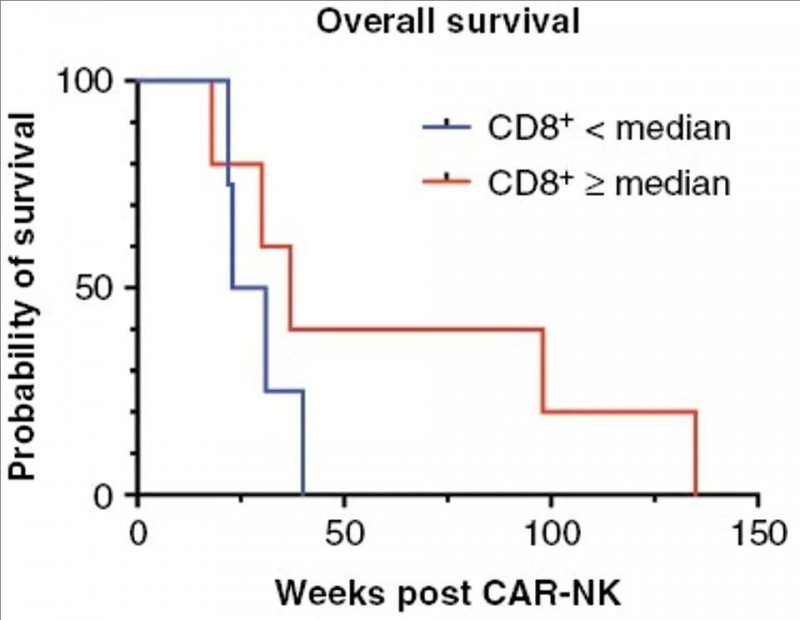
▲图源“Neuro-Oncology”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
3、中位无进展生存期(PFS):所有入组患者(n=9)的中位无进展生存期(PFS)为7周。而出现假性进展的2例患者PFS为37周(详见下图)。
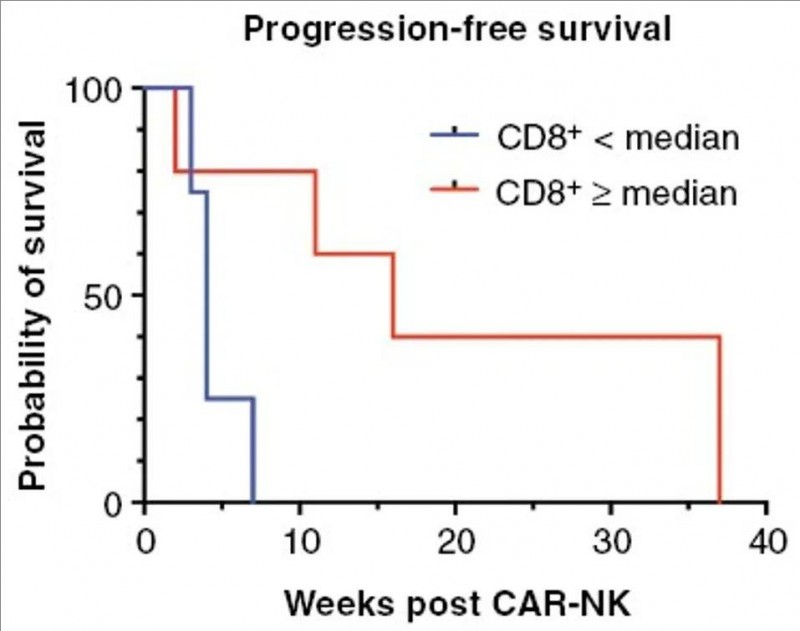
▲图源“Neuro-Oncology”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
此外,入组患者未出现剂量限制性毒性,也未见免疫效应细胞相关神经毒性综合征、细胞因子释放综合征等严重不良反应。综上,颅内注射靶向HER2的CAR-NK细胞,治疗复发性胶质母细胞瘤是安全可行的。
CAR-NK疗法剑指B细胞淋巴瘤,客观缓解率最高可达100%
CAR-NK细胞设计之初主要用于对抗各类血液系统恶性肿瘤,如白血病、淋巴瘤、骨髓瘤等,CAR-NK细胞的作用非常迅速,而且具有治疗时间更短、价格更低廉等优势,患者的接受度更高。
安德森癌症中心进行过一项关于“CAR-NK细胞治疗复发或难治性B细胞恶性肿瘤的Ⅰ/Ⅱ期临床研究(NCT03056339)”,结果同步发表在《新英格兰医学杂志》上。本次共入组37例年龄7~80岁的患者,包括弥漫性大B细胞淋巴瘤(DLBCL)、低度非霍奇金淋巴瘤(NHL)、未转化的慢性淋巴细胞白血病(CLL)。结果显示如下:
1、总生存率:治疗1年后,全部入组患者(n=37)的总生存(OS)率为68%(详见下图)。
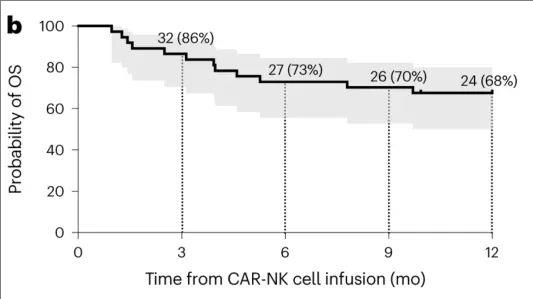
▲图源“nature medicine”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
2、无进展生存率:治疗1年后,全部入组患者(n=37)的无进展生存(PFS)率为32%(详见下图)。
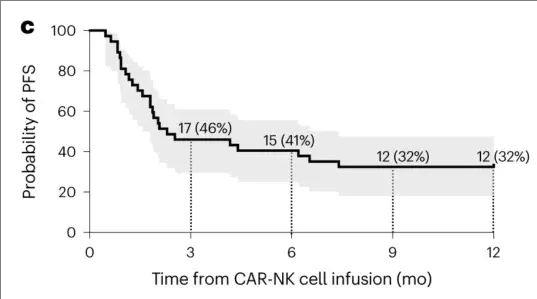
▲图源“nature medicine”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
3、客观缓解率(ORR):治疗第100天,全部入组患者(n=37)的ORR达到48.6%。其中,低度非霍奇金淋巴瘤(NHL)的ORR率更是高达100%,弥漫性大B细胞淋巴瘤(DLBCL)的ORR率为41%,未转化的慢性淋巴细胞白血病(CLL)的ORR率为67%。
4、完全缓解(CR)率:全部患者治疗第30天、100天、365天的CR率分别为27%、29.7%、37.8%。此外,治疗1年后,83%的低度NHL患者、29%的DLBCL患者、50%的CLL患者出现完全缓解(CR)。
小编寄语
CAR-NK细胞在临床研究中具有广阔的应用前景,经CAR修饰后的NK细胞,能更加精准的对抗肿瘤细胞,在治疗血液肿瘤及部分实体瘤中,展现了令人惊艳的初步疗效及安全性,而且相较于CAR-T细胞而言,CAR-NK细胞更易通过临床转化,实现大规模工业化生产,患者的接受度更高!本次CAR-NK细胞在我国顺利开展临床试验,更推动了此款新型疗法的发展,具有重要的影响!小编也希望早日迎来CAR-NK细胞获批上市的好消息,让更多的肿瘤患者获益。
如果您对目前的治疗方案存疑,或想寻求CAR-NK细胞、NK细胞、CAR-T细胞等国内外其他抗癌新技术的帮助,可咨询医学部,详细评估病情或申请国内外抗癌专家会诊。
参考资料
[1]Wang W,et al.Breakthrough of solid tumor treatment: CAR-NK immunotherapy[J]. Cell Death Discovery, 2024, 10(1):40.
https://www.nature.com/articles/s41420-024-01815-9
[2]Liu F,et al.Advances in CAR-NK cell therapy for lung cancer: is it a better choice in the future? Front Oncol. 2024 May 28;14:1390006.
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC11165017/
[3]Zhang X,et al.Cytokine release syndrome after modified CAR-NK therapy in an advanced non-small cell lung cancer patient: a case report[J]. Cell Transplantation,2022,31:09636897221094244.
https://journals.sagepub.com/doi/full/10.1177/09636897221094244
[4]Burger M C,et al.Intracranial injection of natural killer cells engineered with a HER2-targeted chimeric antigen receptor in patients with recurrent glioblastoma[J]. Neuro-oncology, 2023, 25(11): 2058-2071.
https://academic.oup.com/neuro-oncology/article/25/11/2058/7155851?login=false
[5]Marin D, Li Y,et al.Safety, efficacy and determinants of response of allogeneic CD19-specific CAR-NK cells in CD19+ B cell tumors: a phase 1/2 trial[J]. Nature medicine, 2024, 30(3): 772-784.
https://www.nature.com/articles/s41591-023-02785-8
[6]https://m.163.com/v/video/VE8DLS7L0.html







































 首页
首页 咨询
咨询 方舟新药
方舟新药 营养商城
营养商城