我国自研的肠道菌群抗癌新疗法登顶世界期刊,肠道菌群持续击杀结直肠癌、肝癌等,肿瘤缩小近半
2024年3月14日,我国浙江大学医学院的研究团队,在世界顶级期刊《细胞(CELL)》上发文称,他们历经五年时间,发现人体粪便中的主要成员——肠道菌群,可以产生小分子代谢物吲哚丙酸(由益生菌约氏乳酸杆菌产生),用以持续调动T细胞。
在免疫治疗过程中,T细胞会对肿瘤发起攻击,但癌细胞非常狡猾且善于伪装,普通T细胞可能会在攻击过程中,出现免疫耗竭。而经吲哚丙酸激活的T细胞仿佛被打了“鸡血”,可以持续杀伤肿瘤。此外,还可增强抗PD-1单抗在治疗结直肠癌、乳腺癌、黑色素瘤等实体瘤中的效果,有望为恶性肿瘤患者提供更加精准且个性化的肠道微生态治疗手段,具有巨大的临床应用潜力!
▲截图源自“Cell”
肠道菌群:开启肿瘤"个性化"治疗新时代
肠道和淋巴组织都是人体重要的免疫器官,人体约70%的免疫细胞都集中在肠道。据统计,人体微生物群由近40万亿个微生物、3000个物种组成,包括细菌、真菌、病毒等,并编码超过300万个基因,微生物之间丰富度各异,个体之间成分多样,对维持系统稳态和功能稳定性具有重要意义。
研究人员发现肠道菌群在抗肿瘤治疗中发挥着关键作用,现有证据表明,通过调节肠道微生物群的组成,以提高抗癌药物的疗效是可行的。目前可通过粪便菌群移植(FMT)、补充益生菌或益生元、饮食干预等方式,来改变肠道菌群的组成,从而改善癌症的治疗反应。其中,粪便菌群移植(FMT)是将健康供体的肠道菌群移植到患者体内,有助于重建患者胃肠道微生物环境的平衡。
▼正在进行的肠道菌群治疗癌症的临床研究
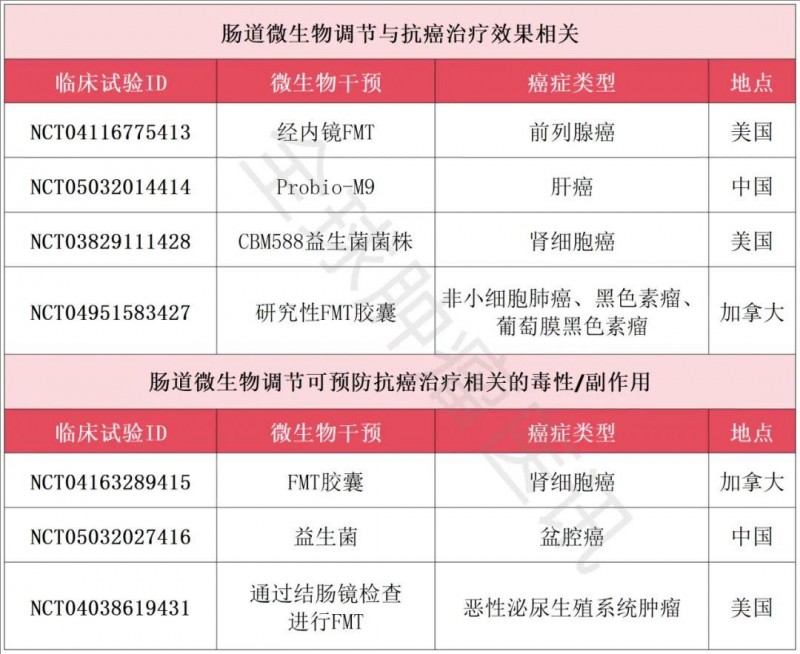
▲数据源自“nature”,全球肿瘤医生网医学部整理汇总
粪便菌群移植联合治疗结直肠癌,患者获得病理完全缓解
结直肠癌(CRC)是全球第二大癌症类型,由于筛查方案和方法不完善,约25%的患者可能会进展为晚期或转移性结直肠癌(mCRC),5年生存率仅为14%左右。目前,化疗、分子靶向治疗[如抗血管内皮生长因子(anti-VEGF)、抗表皮生长因子受体(anti-EGFR)]已成为mCRC的一线治疗方法。但对于部分接受一线治疗后病情进展的患者,效果并不理想。因此,迫切需要寻求新的替代疗法。
随着人们对紊乱的肠道菌群与多种疾病之间关系的认识不断加深,粪便菌群移植(FMT)已成为一种新兴的生物治疗手段,研究发现,肠道细菌的代谢产物直接作用于肠粘膜免疫细胞,可激活T细胞、树突状细胞和巨噬细胞,通过FMT控制肠道微生物会影响免疫系统,并有助于改善癌症患者的预后。
著名开放期刊《Cureus》曾报道过世界首个接受“粪便菌群移植(FMT)联合Bevacizumab(贝伐珠单抗)+Tislelizumab(替雷利珠单抗),IV期pMMR MSS晚期或转移性结直肠癌(mCRC)”将肿瘤大小缩小到可进行根治性手术的范围,从而获得病理完全缓解(pCR)的案例。
这位幸运的患者是一名57岁的中国男性,确诊为IV期pMMR MSS(错配修复充分和微卫星稳定)结直肠癌,并伴有肝转移。患者半个月来出现反复腹痛,大便形状异常。基因检测显示为KRAS/NRAS/BRAF野生型。患者先后接受了两次连续治疗,分别为抗EGFR+改良的FOLFOX6、抗VEGF+FOLFOXIRI。由于严重的化疗副作用,患者停止治疗,并决定接受第三此治疗,即粪便微生物移植(FMT)胶囊+抗VEGF+抗PD-1。结果显示如下:
1、肿瘤标记物
癌胚抗原(CEA)由入院时的30.1μg/L,在第三次治疗后骤降到5.38μg/L;CA199由入院时的62.64KU/L,在第三次治疗后骤降到30.61KU/L(详见下表)。
表1 不同阶段治疗后,该患者的肿瘤标志物水平对比
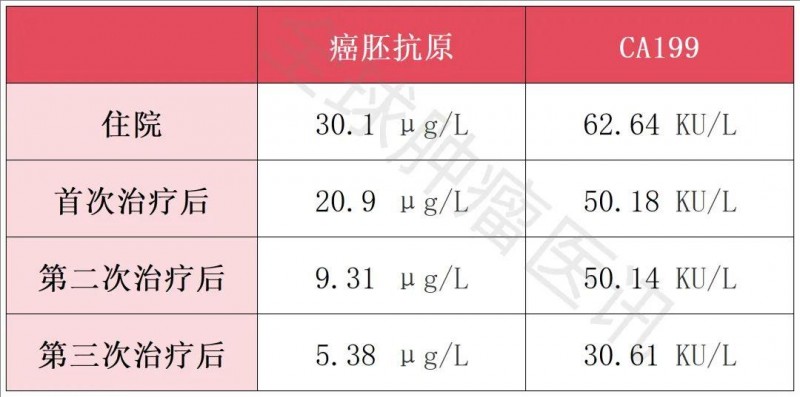
▲数据源自“Cureus”,全球肿瘤医生网医学部整理汇总
2、影像学检查
①治疗前:结肠镜检查发现距肛缘70cm处有一个结节性菜花状结节,病变肠道周围、上、中、下腹腔及腹膜后可见多个肿大淋巴结。结肠CT示升结肠肝曲附近肠壁有4.9cm×4.4cm大小的肿块(详见图A);腹膜后淋巴结转移病灶大小约为8.4cm×4.7cm(详见图B)。肝脏CT示肝脏内有多发斑块状、结节状、低密度影。其中,较大的肿瘤位于肝右叶,大小约为10.3cm×8.7cm(详见图C)。

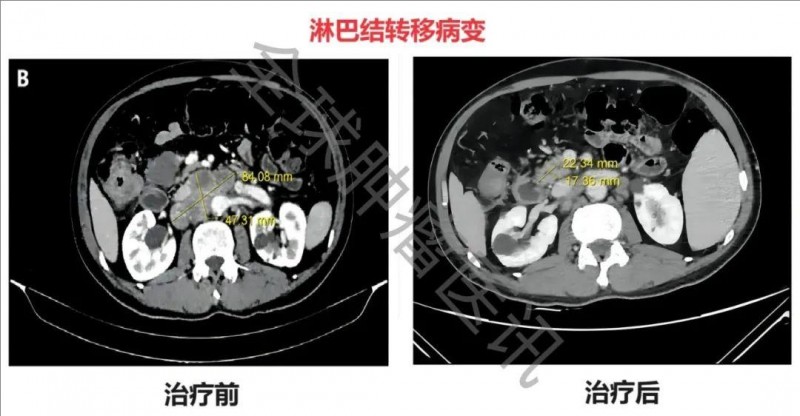
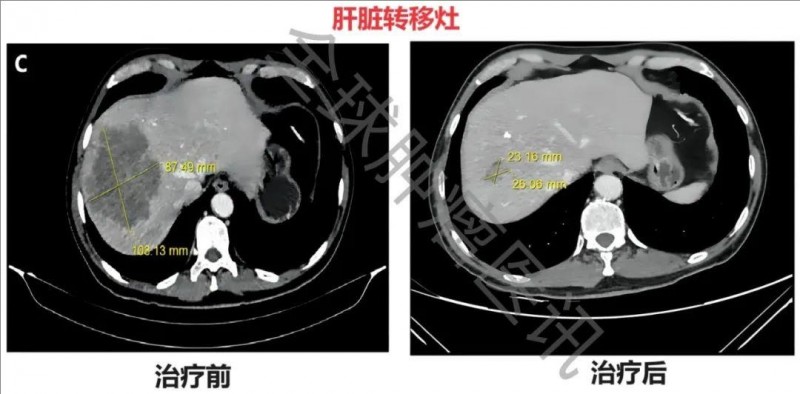
▲图源“PMC”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
②在第三次治疗后,CT显示,结肠(2.0cm×1.3cm)、肝脏(2.6cm×2.3cm)、淋巴结病灶(2.2cm×1.7cm)明显缩小(详见下表),部分病灶在影像学上已不复存在,达到部分缓解(PR),此时肿瘤已缩小到可行根治性手术切除的程度(详见下图)。随后对肝转移灶行微波消融(MWA),对结肠原发肿瘤及相关淋巴结行开放性根治性右半结肠切除术。最终患者幸运地获得了病理学完全缓解(pCR),且未见严重副作用。
表2 不同阶段治疗后,患者结肠肿瘤、腹膜后淋巴结及肝脏转移病变CT对比

▲数据源自“Cureus”,全球肿瘤医生网医学部整理汇总
综上,粪便菌群移植(FMT)在晚期或转移性结直肠癌的免疫疗法中具有巨大潜力,可以改善对免疫检查点抑制剂(ICI)的反应、提高患者的生存率。
除了本文提到的结直肠癌、肝癌外,肠道菌群在治疗肺癌、肾癌、乳腺癌等其他癌种方面,也取得了积极的疗效。
肝癌患者粪便微生物群移植后,肿瘤显著缩小47.7%
除了我国外,韩国也曾进行过“粪便微生物群移植(FMT)治疗晚期难治性胃肠道肿瘤”的相关研究(NCT04264975),同样也获得了惊艳的疗效。其中一位对纳武单抗耐药的转移性肝细胞癌(HCC)患者(患者R7),在接受持续免疫治疗+粪便微生物群移植(FMT)后,肿瘤病灶显著缩小47.7%,最终获得部分缓解(PR)。
1、肿瘤标志物下降:该患者在第2次粪便微生物群移植8周后,肿瘤标志物[包括血清甲胎蛋白(AFP)、PIVKA-II(拮抗剂II诱导蛋白)]显著下降(详见下图)。
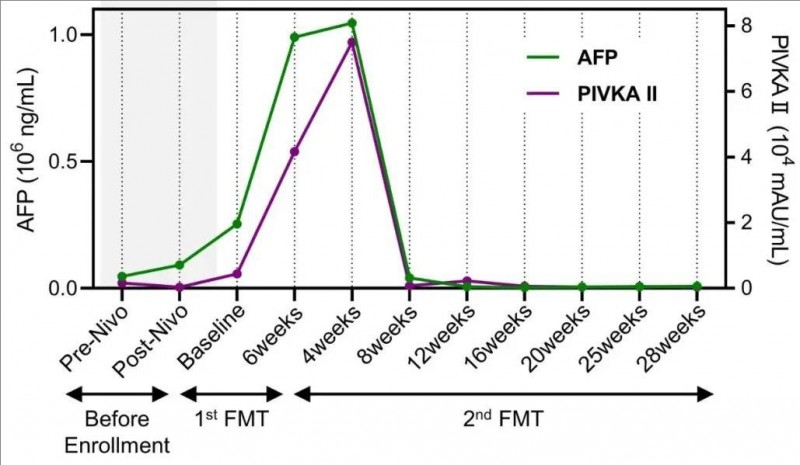
▲图源“Cell Host Microbe”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
2、肿瘤病灶缩小:该患者第2次粪便微生物群移植(FMT)8周后,肿瘤显著缩小了30.5%,之后又进一步缩小至47.7%,并最终获得部分缓解(PR)(详见下图)。
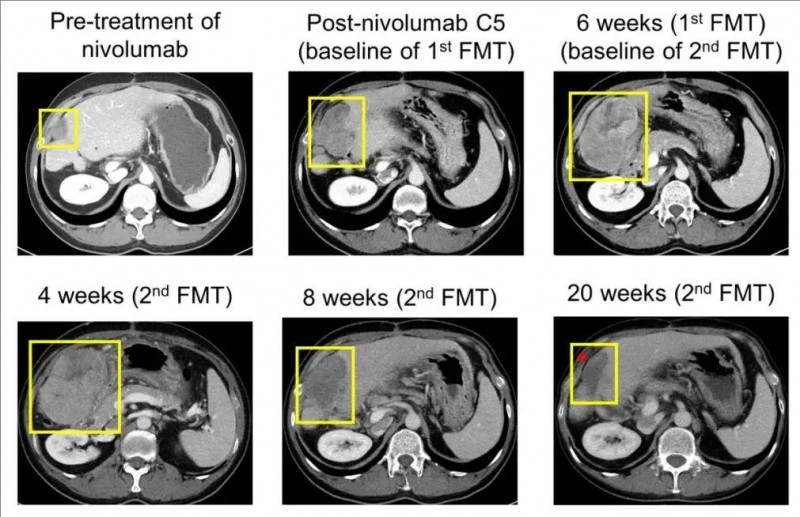
▲图源“Cell Host Microbe”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
注:在第二次FMT8周后,肿瘤缩小,并实现PR(下方红色星号)。
小编寄语
肠道菌群调节是继免疫细胞疗法、癌症疫苗后,又一大热的新型抗癌疗法,有助于提升患者的免疫力、提高抗癌治疗的效果、降低手术和放化疗的副作用、改善患者整体健康状况。
但鉴于患者的个体差异及癌症的复杂性,在治疗前需要对患者的微生物组,进行个性化分析及评估,以便为癌症患者设计特征性微生物组介导的抗癌方案,以提高治疗效果、消除治疗副作用。小编也希望未来随着饮食调理、粪菌移植、益生元及活性益生菌定制等多种治疗方法整合归一,真正地实现对肠道菌群的“个体化精准”调控,让更多的癌症患者获益!
如果您也想寻求肠道菌群、粪菌移植、定制益生菌等的帮助,可以通过医学部,咨询权威的营养专家。
参考资料
[1]Jia D,et al.Microbial linkbolite enhances immunotherapy efficacy by modulating T cell stemness in pan-cancer[J]. Cell, 2024, 187(7): 1651-1665. e21.
https://www.cell.com/cell/abstract/S0092-8674(24)00224-1?_returnURL=https%3A%2F%2Flinkinghub.elsevier.com%2Fretrieve%2Fpii%2FS0092867424002241%3Fshowall%3Dtrue
[2]Zhao L Y,et al.Role of the gut microbiota in anticancer therapy: from molecular mechanisms to clinical applications[J]. Signal Transduction and Targeted Therapy, 2023, 8(1): 201.
https://www.nature.com/articles/s41392-023-01406-7
[3]Cheng X,et al.Successful Treatment of pMMR MSS IVB Colorectal Cancer Using Anti-VEGF and Anti-PD-1 Therapy in Combination of Gut Microbiota Transplantation: A Case Report.Cureus.2023 Jul 24;15(7):e42347.
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC10445052/
[4]Kim Y,et al.Fecal microbiota transplantation improves anti-PD-1 inhibitor efficacy in unresectable or linkstatic solid cancers refractory to anti-PD-1 inhibitor[J]. Cell Host & Microbe, 2024.
https://www.sciencedirect.com/science/article/pii/S1931312824002282?via%3Dihub







































 首页
首页 咨询
咨询 方舟新药
方舟新药 营养商城
营养商城