小细胞肺癌新药,全球第一款PD-L1/VEGFA双特异性抗体药物PM8002注射液获批Ⅲ期临床!客观缓解率超70%
据NMPA官网消息,2024年9月27日,一款PD-L1/VEGFA双抗药物——PM8002注射液的新药IND获国家药品监督管理局药品审评中心(NMPA)的批准,目前该药的Ⅲ期临床已在国内登记,针对小细胞肺癌(SCLC)、三阴性乳腺癌的Ⅲ期临床研究也终于在千呼万唤中正式启动!据悉,PM8002注射液是全球首款同时也是目前唯一进入Ⅲ期临床研究的PD-L1/VEGF双抗药物。
PM8002注射液:首个进入Ⅲ期临床的PD-L1/VEGF双抗
PM8002注射液是普米斯研发的一款针对PD-L1和VEGF-A的双特异性抗体药物,同时也是全球首个且目前唯一一款进入Ⅲ期临床研究的PD-L1/VEGF双抗药物。
先前发表的研究数据表明,PM8002在多种实体肿瘤中具有潜在的抗肿瘤活性、可耐受的安全性。除了小细胞肺癌外,目前该药还针对三阴性乳腺癌、非小细胞肺癌(非鳞状)、肝细胞癌、间皮瘤、神经内分泌肿瘤等多款实体瘤在我国开展了相应的临床研究,相关临床研究数据陆续在ESMO、ASCO等学术大会上发布。
▲截图源自“NMPA”
小细胞肺癌新曙光,客观缓解率超70%
在2023年欧洲肿瘤内科学会(ESMO)上,公布了“PM8002联合紫杉醇,作为小细胞肺癌(SCLC)二线治疗”的Ⅱ期惊艳临床研究数据。

▲截图源自“OncologyPRO”
本次研究共入组27例接受一线铂类化疗(联合或不联合检查点抑制剂治疗)失败的晚期小细胞肺癌(SCLC)患者,入组接受PM8002联合紫杉醇治疗。
结果显示:疾病控制率(DCR)高达81.8%(18/22),总体客观缓解率(ORR)高达72.7%(16/22),中位无进展生存期(PFS)长达5.5个月。
综上,PM8002与紫杉醇联合使用,对一线铂类化疗失败的晚期小细胞肺癌(SCLC),表现出令人鼓舞的抗肿瘤活性,而且安全性可控,为那些晚期无药可用的小细胞肺癌患者带来了新的希望与选择!
超半数非小细胞肺癌患者,达到病情稳定
在2023年美国临床肿瘤学会(ASCO)上,公布了“PM8002治疗晚期非小细胞肺癌(NSCLC)”的Ⅱ期临床研究(NCT05918445)的惊艳数据。本次研究共入组61例晚期非小细胞肺癌(NSCLC)患者,包括晚期非鳞状NSCLC、EGFR突变的晚期非鳞状NSCLC、EGFR/ALK野生型NSCLC。
入组接受PM8002治疗后,结果显示:在61名可评估疗效的患者中,有16例(26%)达到部分缓解(PR),32例(52.5%)达到病情稳定(SD)。这也意味着超半数非小细胞肺癌患者在PM8002治疗后,病情得到控制(详见下表)!
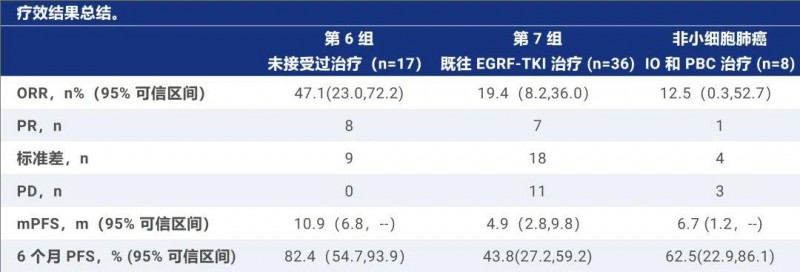
▲数据源自“ASCO”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
小编寄语
好消息是,如今这款PM8002抗癌新药终于在我国启动临床啦,主要针对小细胞肺癌、非小细胞肺癌、胆管癌、黑色素瘤等多款实体瘤。想了解PM8002更多信息或参加临床试验的病友,可将近期影像学及病理检查结果、治疗经历等资料,提交至医学部,进行初步评估或通过方舟计划寻求免费用药的机会!
参考资料
[1]Cheng Y,et al.1992P A phase II safety and efficacy study of PM8002 (anti-PD-L1 x VEGF-A bispecific) combined with paclitaxel as a second-line therapy for small cell lung cancer (SCLC)[J]. Annals of Oncology, 2023, 34: S1062.
https://oncologypro.esmo.org/meeting-resources/esmo-congress-2023/a-phase-ii-safety-and-efficacy-study-of-pm8002-anti-pd-l1-x-vegf-a-bispecific-combined-with-paclitaxel-as-a-second-line-therapy-for-small-cell-lu
[2]Wu C,et al.A phase Ib/IIa trial to textareauate the safety and efficacy of PM8002, a bispecific antibody targeting PD-L1 and VEGF-A, as a monotherapy in patients with advanced NSCLC[J]. 2024.
https://meetings.asco.org/abstracts-presentations/232220







































 首页
首页 咨询
咨询 方舟新药
方舟新药 营养商城
营养商城