12款一类抗癌新药/新技术首次在中国获批临床
据中国国家药监局药品审评中心(NMPA)消息,近期(2024年9月23日~2024年10月6日)共有11款一类创新药/新技术,首次在中国获得临床试验默示许可(IND),其中包括ADC药物、双抗类药物、CAR-T细胞疗法、TCR-T细胞疗法等。下面全球肿瘤医生网帮大家简单汇总一下,以供癌友们参考。
首次在中国获批临床的一类新药大汇总
ABBV-706
药品信息
①药物名称:ABBV-706注射用冻干粉。
②研发公司:AbbVie(艾伯维)。
③治疗靶点:靶向SEZ6。
④适应证:复发/难治小细胞肺癌。
药物介绍
ABBV-706注射用冻干粉是一款靶向SEZ6(是一种跨膜蛋白,在小细胞肺癌、中枢神经系统肿瘤、其他神经内分泌肿瘤中表达)的ADC药物,与拓扑异构酶1抑制剂有效载荷结合,在治疗小细胞肺癌(SCLC)、其他神经内分泌肿瘤(NEN)、中枢神经系统肿瘤(CNS)方面展现出了良好的疗效。
在2024 ASCO大会上,公布了ABBV-706的1期临床研究数据(NCT05599984),本次共入组49例患者(包括22例小细胞肺癌、5例中枢神经系统肿瘤、22例其他神经内分泌肿瘤),既往接受过2.5线治疗(范围1-6)。
结果显示:对于33名RECIST可评估患者,客观缓解率(ORR)达到21%(详见下图),其中7例达到部分缓解(PR)。
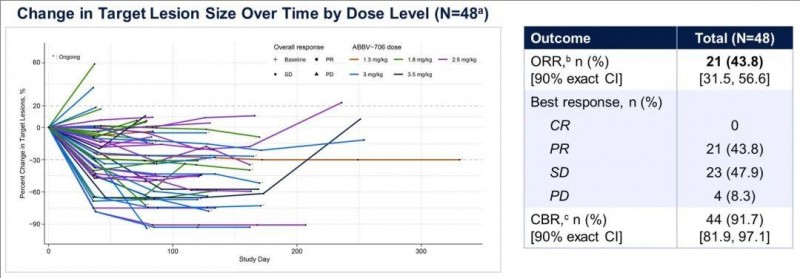
▲图源“NMPA”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
值得一提的是,其中一位76岁高级别胃神经内分泌肿瘤(胃部G3 NET转移)患者,既往曾接受过术前肿瘤切除手术+标准一线化疗,入组接受ABBV-706治疗6周后,达到部分缓解(PR),肿瘤缩小78%;治疗第12周,肿瘤进一步缩小至91%(详见下图)!
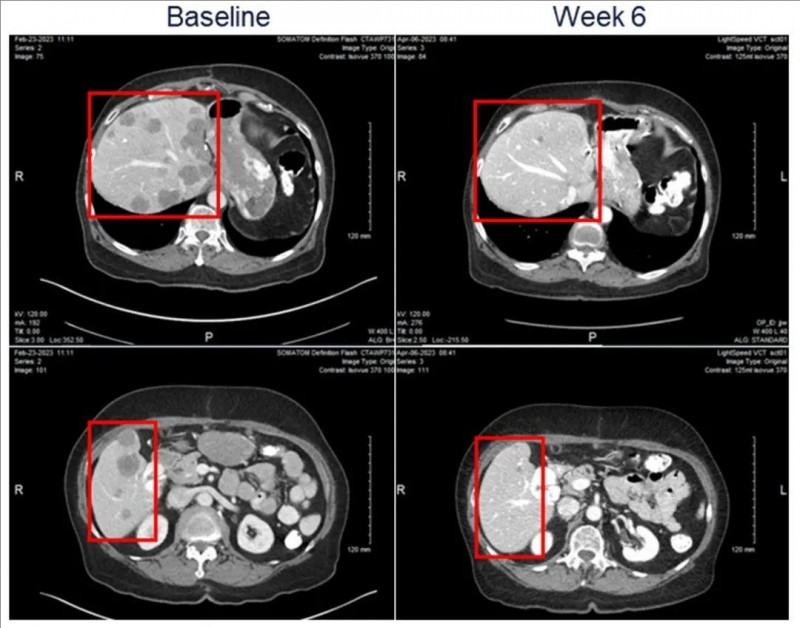
▲图源“NMPA”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
INV-9956胶囊
药品信息
①药物名称:INV-9956胶囊。
②研发公司:原力生命科学。
③治疗靶点:CYP11A1。
④适应证:晚期转移性去势抵抗性前列腺癌。
药物介绍
INV-9956是原力生命科学自主研发的一款强效且高选择性的口服CYP11A1抑制剂,可用于治疗去势抵抗性前列腺癌(CRPC),具有卓越的体内抗肿瘤疗效。2024年9月30日,INV-9956胶囊的新药IND申请获中国国家药监局药品审评中心(NMPA)批准,拟用于治疗晚期转移性去势抵抗性前列腺癌。在此之前(2024年7月16日)INV-9956就已获得美国食品药品监督管理局(FDA)批准,开展临床研究。
JNJ-78278343
药品信息
①药物名称:JNJ-78278343注射液。
②研发公司:强生公司。
③治疗靶点:KLK2-CD3。
④适应证:成年男性晚期前列腺癌。
药物介绍
JNJ-78278343注射液是由强生公司研发的一款KLK2-CD3双特异性抗体在研新药,通过与T细胞上的CD3结合,从而诱导T细胞活化,并将T细胞重定向至肿瘤细胞,最终导致T细胞介导的KLK2表达肿瘤细胞的裂解。目前JNJ-78278343的新药IND申请已获得中国NMPA的批准,拟用于成年男性的晚期前列腺癌的治疗。
BT8009
药品信息
①药物名称:BT8009。
②研发公司:Bicycle公司。
③治疗靶点:Nectin-4。
④适应证:尿路上皮癌。
药物介绍
BT8009是一种双环毒素结合物(BTC),由一种高度选择性的双环肽组成,该肽靶向nectin-4(是一种粘附分子,在尿路上皮癌等多种肿瘤中表达),通过可裂解的连接体与MMAE连接,可以高亲和性和选择性与靶标结合,具有高肿瘤渗透性。
CG009301
药品信息
①药物名称:注射用CG009301。
②研发公司:Cullgen Inc。
③治疗靶点:GSPT1。
④适应证:复发/难治性血液恶性肿瘤。
药物介绍
CG009301是一种高选择性GSPT1降解剂,用于治疗复发或难治性血液系统恶性肿瘤[包括但不限于急性髓系白血病(AML)、急性淋巴细胞白血病(ALL)、高风险骨髓增生异常综合征(MDS)]。2024年10月8日,中国国家药品监督管理局(NMPA)已批准CG009301的临床试验(IND)申请,Cullgen将很快在中国启动CG009301的I期临床试验。
SYN818
药品信息
①药物名称:SYN818片。
②研发公司:圣域生物。
③适应证:晚期实体瘤。
药物介绍
SYN818片是由圣域生物自主研发的一款新型强效且高选择性的1类小分子化合物,可精准靶向并高效抑制Polθ(DNA聚合酶θ)的活性,从而抑制肿瘤细胞的DNA损伤修复,最终达到抗肿瘤的目的。2024年9月30日,——SYN818片的新药IND申请,获得中国NMPA批准,用于晚期实体瘤的治疗。
GTA182
药品信息
①药物名称:GTA182片。
②研发公司:PRMT5。
③适应证:MTAPnull/lost晚期实体瘤。
药物介绍
GTA182是一种是一款可穿透血脑屏障的第二代蛋白质精氨酸甲基转移酶5(PRMT5)抑制剂,具有甲硫腺苷(MTA)协同作用,对MTAP缺失的癌细胞具有高度选择性,而且不针对MTAP正常表达的非癌细胞,这种选择性有望为MTAP缺失型癌症患者提供更有效、更安全的治疗选择。
约有10%的实体瘤存在MTAP缺失,包括胶质母细胞瘤、肺癌、胰腺癌和膀胱癌等,这些肿瘤的治疗选择很有限,患者的大量临床需求尚未得到满足。而GTA182对MTAP缺失型肿瘤的高选择性及其穿透血脑屏障的能力,使其成为可能治疗中枢神经系统肿瘤和非中枢神经系统适应症的临床开发的best-in-class药物,已在先前的研究中展现出具有抑制肿瘤生长和肿瘤消退的显著效果。
PTX-912
药品信息
①药物名称:注射用PTX-912。
②研发公司:博致生物。
③适应证:局部晚期/转移性实体瘤。
药物介绍
注射用PTX-912是由博致生物自主研发的新一代免疫细胞靶向的IL-2前药融合蛋白,显示出对 PD-1 通路的剂量依赖性抑制,可使IL-2前药在肿瘤微环境中被特异性激活,有助于改善IL-2的外周毒性问题,还可充分发挥IL-2的免疫激活及抗肿瘤功效。2024年10月12日,注射用PTX-912的临床试验默示许可获中国国家药品监督管理局批准,拟用于治疗局部晚期/转移性实体瘤。
YY2201
药品信息
①药物名称:YY2201片。
②研发公司:亚尧生物。
③治疗靶点:ATR。
④适应证:晚期实体瘤。
药物介绍
YY2201片是由亚尧生物自主研发的一款口服ATR小分子抑制剂,在此前的研究中,展现出良好的体内/体外活性。该药已获得中国NMPA及美国食品药品监督管理局(FDA)的IND临床批件(IND173030),用于晚期实体瘤的治疗。
首次在中国获批临床的新技术大汇总
IM96 CAR-T
药品信息
①药物名称:IM96 CAR-T细胞注射液。
②治疗靶点:GUCY2C。
③适应证:结直肠癌。
药物介绍
IM96 CAR-T细胞注射液是由我国自主研发的一款靶向GUCY2C的CAR-T细胞产品,目前新药IND申请已获我国NMPA批准,用于治疗晚期结直肠癌。
值得欣慰的是,在2024年美国临床肿瘤学会(ASCO)年会上,我国研究团队携IM96 CAR-T的I期临床数据(NCT05287165)惊艳亮相!结果显示:在19例可评估患者中,疾病控制率(DCR)高达73.7%,客观缓解率(ORR)达到26.3%(详见下图),可见IM96 CAR-T在转移性结直肠癌患者中,具有持久的疗效且安全性可控。此外,在DL3亚组中,无论有无肝转移,客观缓解率(ORR)均能达到40.0%,可见该药在肝转移患者中显示出很高的治疗潜力!
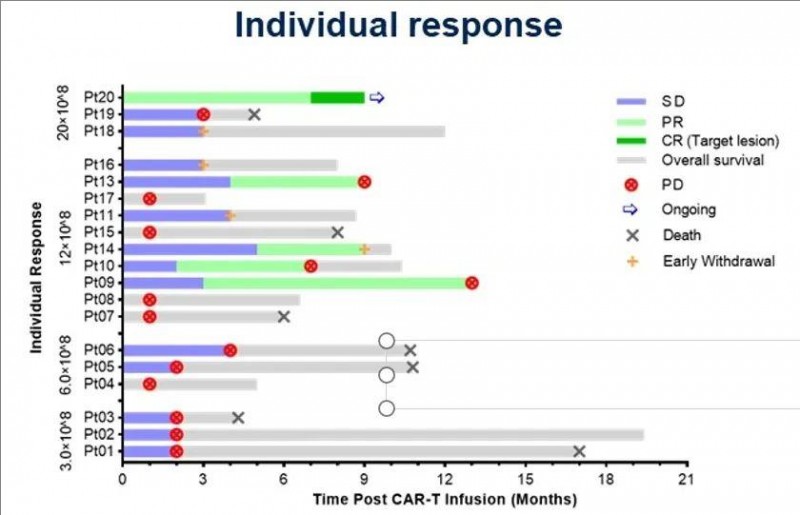
▲图源“ASCO”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
IPM001
药品信息
①药物名称:IPM001注射液。
②研发公司:臻知医学。
③治疗靶点:多抗原靶点。
④适应证:进展期原发性肝细胞癌。
药物介绍
IPM001注射液是由北京臻知医学自主研发的一款多抗原靶点的自体工程化T细胞(TCR-T)注射液,可靶向数十种肝癌相关抗原与新生抗原。2024年10月9日,IPM001注射液的新药临床研究申请,正式获得国家药品监督管理局(NMPA)默示许可,用于经二线系统性抗肿瘤治疗失败或不耐受的进展期原发性肝细胞癌的治疗,有望成为中国晚期肝癌患者的重要治疗选择之一。
IX001 TCR-T
药品信息
①药物名称:IX001 TCR-T注射液。
②研发公司:镔铁生物。
③治疗靶点:KRAS G12V突变。
④适应证:晚期胰腺癌。
药物介绍
IX001 TCR-T注射液是一款针对KRAS G12V突变的创新型TCR-T细胞疗法,可将特异性识别KRAS G12V突变的TCR基因序列,转入T细胞中,使其精准识别并杀伤胰腺癌细胞。2024年10月9日,该药的临床试验默示许可获中国国家药品监督管理局(NMPA)批准,拟用于HLA-A*11:01基因型、KRASG12V抗原表达阳性晚期胰腺癌的治疗。
小编寄语
以上新药/新技术仅为众多研发热点中的一小部分,还有多款抗癌新药或新型免疫疗法正在研发中,而且目前有多款在研药物已相继开展临床试验,这也意味着中国患者将有免费获得最新抗癌药物治疗的机会。同时,“方舟援助计划”也可为患者提供上市新药和未上市新药免费治疗的机会。对现有治疗方案不满意的患者,可将近期影像学及病理检查报告、治疗经历等资料,提交至医学部,进行初步评估或了解详细的入排标准。
参考资料
[1]QI C,et al.Phase I study of GUCY2C CAR-T therapy IM96 in patients with linkstatic colorectal cancer[J]. 2024.
https://meetings.asco.org/abstracts-presentations/234018
[2]Chandana S R,et al.First-in-human study of ABBV-706, a seizure-related homolog protein 6 (SEZ6)–targeting antibody-drug conjugate (ADC), in patients (pts) with advanced solid tumors[J]. 2024.
https://ascopubs.org/doi/10.1200/JCO.2024.42.16_suppl.3001
[3]https://www.cde.org.cn/







































 首页
首页 咨询
咨询 方舟新药
方舟新药 营养商城
营养商城