2025年一定要知道的四款重磅胃癌新药
几乎所有患者靶病灶不同程度缩小或控制稳定!2025年胃癌患者一定要关注这4款新药!
在中国,胃癌是最令人望而生畏的癌症之一,全球将近一半的新发胃癌患者和死亡病例都在中国!更可怕的是,在中国大部分患者确诊时已处于中晚期,治疗的方式非常有限,患者的生存面临着严峻的考验。
近年来,针对HER2,Claudin18.2,PD-L1,MET,FGFR2等靶点的药物纷纷问世,为胃癌开启了一个全新的治疗模式,创造了新的可能性。2024年,4款国际及国内在研的胃癌新药疾病控制率高达100%,交上了卓越的答卷,2025年将为病友照亮新的生存希望。
一、疾病控制率高达100%!国研单抗ASKB589初战告捷
ASKB589 是 AskGene研发的一种创新生物药物,它是一种针对 CLDN 18.2 的重组人源化单克隆抗体。该药物通过与表达 CLDN18.2 的癌细胞高亲和力结合,介导抗体依赖性细胞介导的细胞毒作用 (ADCC) 和补体依赖性细胞毒作用 (CDC)。ASKB589 旨在治疗 G/GEJ 癌、胰腺癌以及表达 CLDN18.2 的其他癌症类型。
2024年美国临床肿瘤学会胃肠道肿瘤研讨会(ASCO GI)上公布了这款国研药物的鼓舞人心的最新数据。ASKB589 联合化疗 (CAPOX) 和 PD-1 抑制剂作为局部晚期、复发和转移性胃 (G) 或胃食管连接部 (GEJ) 腺癌患者的一线治疗,疾病控制率高达100%!
截至 2023 年 12 月 20 日,共有 62 名 CLDN18.2 表达阳性的晚期胃癌患者接受了ASKB589 联合 CAPOX 和 PD-1 抑制剂治疗。
结果显示:客观缓解率(ORR)高达80%(36 名)患者达到部分缓解,肿瘤病灶显著缩小30%以上,还有2名幸运的患者肿瘤靶病灶完全消失!9 名(20.0%)患者达到疾病稳定,整体疾病控制率高达 100%,这意味着所有患者的肿瘤靶病灶都出现了不同程度的缩小或控制稳定!
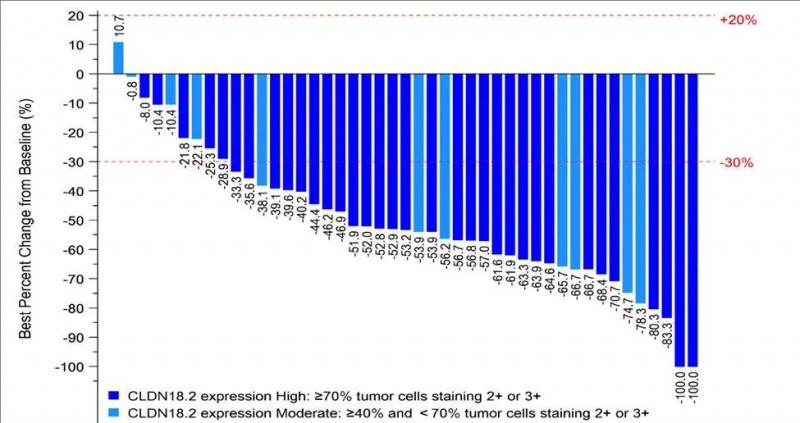
值得国内病友们振奋的是,目前这款药物临床试验仍在在中国招募患者,已有大量胃癌患者通过全球肿瘤医生网医学部成功入组!如想检测相关靶点或了解详情的病友可以致电医学部进行评估。
二、超50%肿瘤靶病灶显著缩小!HER2+胃癌迎来全新用药方案
维迪西妥单抗是我国首款获批上市的国产ADC(抗体-偶联)新药,也是我国首个获得美国FDA、中国国家药监局突破性疗法双重认定的ADC药物。
近期,维迪西妥单抗联合特瑞普利单抗在晚期 G/GEJ 癌或其他实体瘤中取得了令人鼓舞的疗效!

2020 年 7 月 13 日至 2022 年 8 月 30 日期间,共招募了 56 名符合条件的晚期胃或胃食管交界腺癌(G/GEJ)或其他实体瘤,HER2 IHC ≥1 或 ISH 阳性,并且至少一线治疗失败或无法耐受或无法获得标准治疗的患者,其中包括 30 名 G/GEJ 癌患者和 26 名其他实体瘤患者,这些患者入组后接受维迪西妥单抗联合特瑞普利单抗的治疗。
结果显示:52 名患者完成了疗效评估。
●胃或胃食管交界腺癌患者(n = 30)中确诊客观缓解率(ORR)为 43%(12/28,95% CI 25,63),中位无进展生存期(PFS)为 6.2 个月(95% CI 4.0,6.9),中位总生存期(OS)为 16.8 个月(95% CI 7.2,NE)。
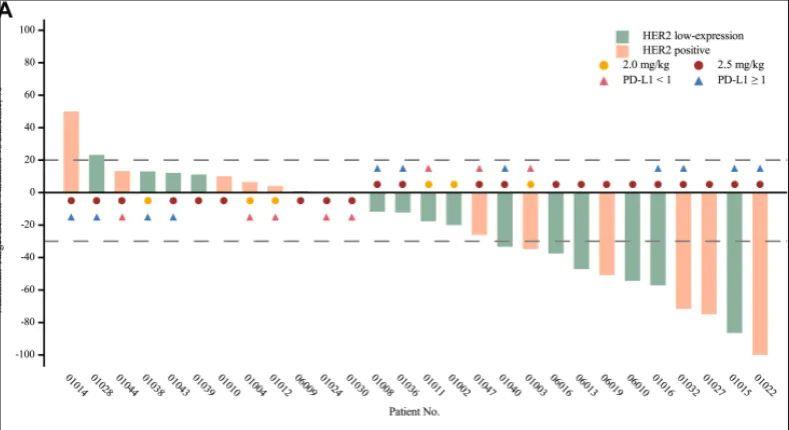
●接受 RP2D剂量方案治疗的 G/GEJ 癌患者(n = 24)ORR 达 50%(11/22,95% CI 28,72),中位 PFS 为 5.1 个月(95% CI 1.4,7.3),中位 OS 为 14.0 个月(95% CI 6.3,NE)。
●值得一体的是,在接受 RP2D 治疗的 G/GEJ 癌患者中,HER2 阳性和低 HER2 表达人群均观察到临床益处,其中,HER2 阳性患者的客观缓解率(ORR )高达 56%,低 HER2 表达为46% 。中位 PFS 分别为 7.8 个月 (95% CI 0.9, NE) vs. 5.1 个月 (95% CI 1.2, 6.9),中位 OS 分别为 NE 个月 (95% CI 4.3, NE) vs. 14.0 个月 (95% CI 5.1, NE)。好消息是维迪西妥单抗治疗HER2+胃癌临床研究已在国内启动,目前正在招募患者。已有大量胃癌患者通过全球肿瘤医生网医学部成功入组!如想检测相关靶点或了解详情的病友可以致电医学部进行评估。
三、97%患者肿瘤靶病灶显著缩小或稳定!FG-M108疗效喜人
FG-M108是明济生物自主研发的靶向CLDN18.2的ADCC增强型单克隆抗体,以适中亲和力高特异性的靶向CLDN18.2阳性肿瘤细胞,并通过增强的ADCC效应等充分调动患者机体的免疫功能来杀伤肿瘤。
2024年欧洲肿瘤内科学会(ESMO)年会上,FG-M108公布了FG-M108联合卡培他滨和奥沙利铂(CAPOX)一线治疗局灶晚期不可切除或者转移性胃/胃食管交界部(G/GEJ)腺癌的最新临床试验结果,非常振奋人心!
截止至2024年7月18日,入组了52名患有HER2-/CLDN18.2+(IHC 1+/2+/3+≥10%)晚期或转移性胃癌/胃食管交界腺癌的中国受试者。
结果显示:51例疗效可评估的受试者中,36例受试者属于CLDN18.2中高表达的患者(IHC 2+/3+≥40%),客观缓解率(ORR)高达81%(cORR为78%),疾病控制率(DCR)为97%!
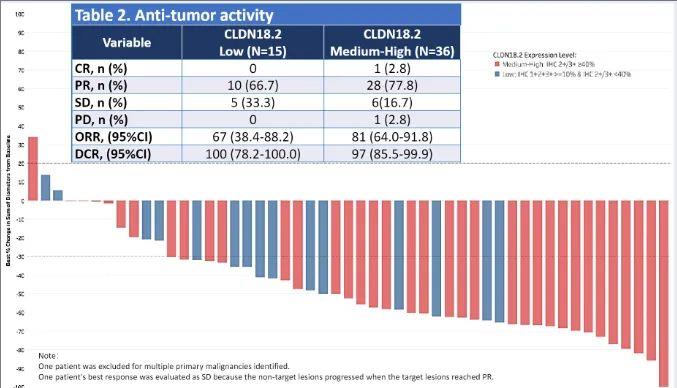
值得国内病友们振奋的是,目前这款药物临床试验仍在在中国招募患者,已有大量胃癌患者通过医学部成功入组!如想检测相关靶点或了解详情的病友可以致电医学部进行评估。
四、登顶《Nature Medicine》!中国首创CLDN18.2CAR-T实现疾病控制率96.1%
在2024年美国临床肿瘤学会(ASCO)上,北京大学肿瘤医院研究团队公布了“satri-cel治疗胃肠道肿瘤的1期临床试验(CT041-CG4006(NCT03874897))的最终结果”,引起巨大轰动!这是首个应用CLDN18.2-CAR-T细胞治疗实体瘤的临床研究数据,并同步发表在国际顶级期刊《Nature Medicine》杂志上。

这项研究共纳入98例CLDN18.2阳性晚期胃肠道肿瘤患者,包括胃和胃食管交界腺癌,胰腺癌,胆管癌等。入组接受不同剂量的satri-cel(即CAR-T细胞)回输治疗,回输剂量分别为2.5×10^8(89例患者)、3.75×10^8(6例患者)、5.0×10^8(3例患者)。
结果显示:在全部98例患者中:在基线时有目标病灶的90例患者中,70例患者的肿瘤出现了不同程度的缩小,总缓解率(ORR)为38.8%,疾病控制率(DCR)高达91.8%。
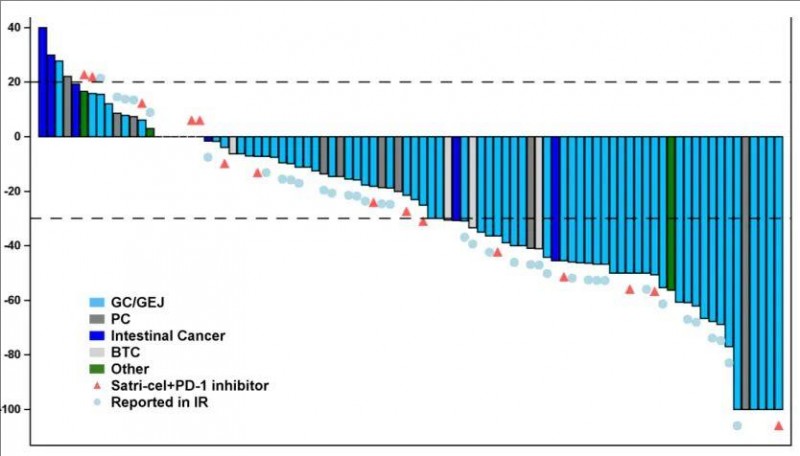
接受单药治疗(n=59)的胃/胃食管结合部(GC/GEJ)癌患者中:-51例患者有目标病灶:客观缓解率(ORR)为54.9%(28/51),疾病控制率(DCR)高达96.1%(49/51),中位持续缓解时间(mDOR)为6.4个月(95% CI:4.6,8.3)。中位无进展生存期(mPFS)为5.8个月(95% CI:4.1,8.0),中位总生存期(mOS)为9.0个月(95% CI:7.0,11.9)。
此外,一项1b 期多中心开放标签研究 ( NCT04404595 )正在美国 6 个地点开展临床试验,众多美国胃癌患者已成功入组。近期,美国两家知名的癌症中心分别报道了两位幸运的患者达到完全缓解和部分缓解,这意味着,中国CAR-T疗法正站在世界舞台绽放璀璨光芒,造福全球患者!
30岁年轻晚期印戒细胞胃癌患者CAR-T治疗后获得完全缓解

美国MD安德森公布治疗案例
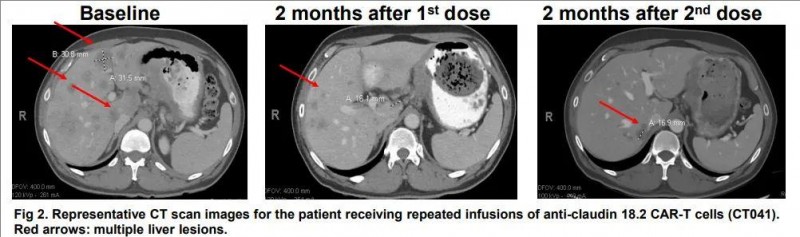
目前,satricabtagene autoleucel/CT041试验的长期随访显示,该疗法在经治CLDN18.2阳性晚期胃肠道(GI)肿瘤患者,特别是胃癌/胃食管结合部癌患者中,表现出高度有前景的疗效和可控的安全性。与传统抗肿瘤方法相比,它可能对现有的治疗格局产生重大影响,并推动更广泛的创新研究。
相信上面这些在研药物给了晚期胃癌患者新的希望,同时也能看出,我国的新药研发水平正以前所未有的速度迈向世界前列!随着新型临床研究的推进,对检测提出了更高要求,需要全面了解患者的基因图谱 ,已经做了检测的病友可提交病历至医学部初步评估获得用药方案及临床试验推荐。相信胃癌患者的明天会越来越好。




































 首页
首页 咨询
咨询 方舟新药
方舟新药 营养商城
营养商城