抗癌疫苗上演"肿瘤消失术"?痛击肺癌、胰腺癌、黑色素瘤等,从无药可用到总生存拉长19个月
癌症疫苗历经数十年的发展,逐渐从基础研究转向了临床研究阶段,近年来更是取得了突破性进展。NHS国家癌症临床主任PeterJohnson教授曾满怀期待地指出:“我们知道,即使手术成功,癌症有时也会复发。这可能与体内仍残留少量癌细胞有关,但使用针对这些残留癌细胞的癌症疫苗,或许可以阻止这种情况的发生”。
就在近期,国内外众多科研团队和医疗机构齐心协力,积极开展了多项针对癌症疫苗的前沿临床研究,并取得了令人瞩目的成绩。不仅成功将患者的总生存时间大幅延长至19个月,甚至实现了无进展生存期超577天的佳绩;更是在肺癌治疗领域创造了令人惊叹的奇迹——助力肺癌患者右肺病灶近乎消失,为全球癌症治疗事业注入了一剂强心针!下面小编为大家简单介绍一下,以坚定癌友们的抗癌信心!
癌症疫苗联合达沙替尼首例人体试验结果出炉,晚期检查点耐药黑色素瘤总生存时间延长至19个月
黑色素瘤的发病率呈持续上升态势。美国癌症协会预计,2021年黑色素瘤的确诊病例将超过10万例。在过去十年间,随着靶向小分子抑制剂(如BRAFi、MEKi)以及免疫检查点阻断疗法的出现,晚期IIIB-IV期黑色素瘤患者的一线治疗方案格局发生了重大调整。这些新疗法虽然提高了客观临床反应率(OCR),但免疫相关不良事件的发生率也显著攀升,且大多数黑色素瘤患者仍对免疫检查点阻断疗法表现出原发性或获得性耐药。因此,开发更为有效的其他治疗手段迫在眉睫。近年来,树突状细胞疫苗的问世,为这类患者带来了新的希望。
近期,匹兹堡大学癌症研究所开展了一项“针对晚期黑色素瘤的人类白细胞抗原(HLA)-A2+患者,应用癌症疫苗的首例人体前瞻性随机II期试点临床试验(NCT01876212)”引起了广泛关注,其令人瞩目的数据同步发表于《癌症免疫治疗杂志》。
本次研究共纳入16例晚期黑色素瘤患者,包括10例皮肤黑色素瘤患者、5例葡萄膜黑色素瘤患者、1例粘膜黑色素瘤患者。其中15例患者此前接受过程序性细胞死亡蛋白1(PD-1)阻断治疗后,病情出现进展。入组患者被随机分为两个治疗组:即A组(采用自体aDC1/TBVA肽基疫苗+从第5周开始使用达沙替尼的治疗方案)、B组(采用自体aDC1/TBVA肽基疫苗+从第1周开始使用达沙替尼的治疗方案)。
▼自体aDC1/TBVA肽基疫苗的产生
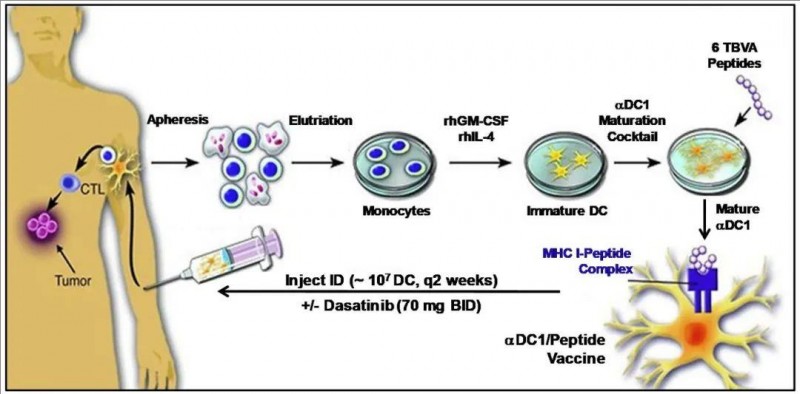
▲图源“BMJ”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
结果显示:在13例可评估患者中,6例患者(A组2例、B组4例)对外周血中≥3种疫苗肽产生了特异性CD8+T细胞反应。值得关注的是,在这6例产生疫苗特异性T细胞反应的患者中,有四名出现了客观临床反应率(OCR),其中4例达到部分缓解(PR),2例达到病情稳定(SD)(详见下图)。
▼瀑布图描绘了治疗期间肿瘤负荷的最大变化
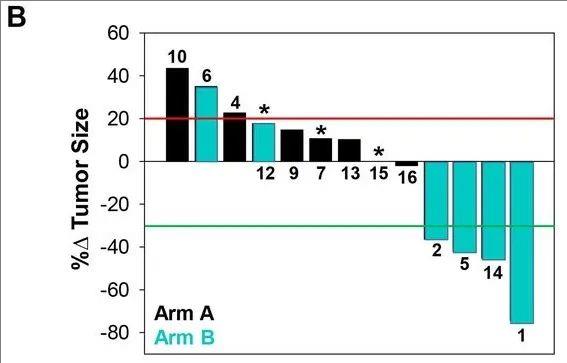
▲图源“BMJ”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
注:肿瘤大小分别用红色实线表示增加20%;绿色实线表示减少30%。
值得注意的是,与接受A组治疗(即疫苗+从第5周开始延迟使用达沙替尼)的患者相比,接受B组治疗(即联合疫苗+从治疗起始便立即使用达沙替尼)的患者总生存期(OS)得到显著改善,中位总生存期(OS)分别为19.1个月(B组) vs 8.3个月(A组);p=0.0086(详见下图-左)。此外,B组的无进展生存期(PFS)也呈现出改善趋势,中位无进展生存期(PFS)分别为7.9个月(B组) vs 2.2个月(B组);p=0.063(详见下图-右)。
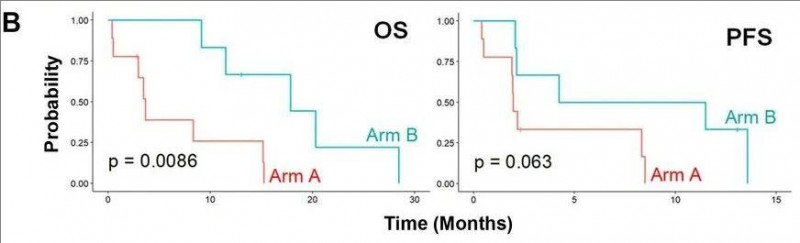
▲图源“BMJ”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
下图展示了两例代表性患者(患者1、患者5),在接受疫苗治疗后,产生了协调免疫反应,正电子发射断层扫描(CT)显示,内脏转移灶显著缩小(详见下图)。
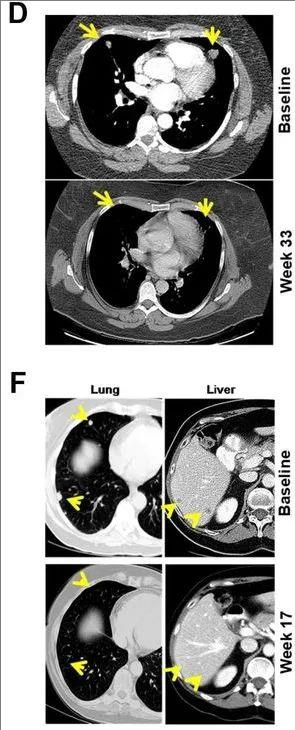
▲图源“BMJ”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
注:图中黄色箭头表示基线与治疗期间的靶病变。
国研KRAS G12V mRNA疫苗精准狙击肺癌与胰腺癌,助力患者右肺病灶近乎消失
KRAS与胰腺导管腺癌(PDAC)、非小细胞肺癌(NSCLC)等具有高致死性的癌症紧密相连。对于终末期患者来说,寻觅到优质的肿瘤新抗原候选物,乃是生产现成肿瘤疫苗的核心要点。但当下存在一个现实难题:晚期患者的治疗窗口期极为短暂,而个性化疫苗从测序、通过生物信息学进行预测,再到完成制造,一般需要较长时间(8-12周)。这一状况致使鲜有研究能够就mRNA疫苗对晚期癌症患者的疗效展开报道。
不过,值得欣慰的是,近期上海交通大学医学院附属瑞金医院胰腺疾病诊疗团队开展了一项“针对KRASG12V单靶点的mRNA肿瘤疫苗在晚期实体瘤中治疗效果的研究”,为mRNA疫苗应用于晚期实体瘤治疗带来了希望的曙光。据了解,这是首次通过人体研究证实针对多种新抗原的mRNA疫苗在13例晚期黑色素瘤患者中的安全性以及初步有效性,该疫苗甚至在两例终末期癌症患者体内促使肿瘤出现缩小。其令人瞩目的研究数据同步发表在国际医学顶级期刊《CellResearch》上。
其中患者001是一位86岁的女性,因胆道梗阻就医,后确诊为局部晚期胰头癌。鉴于其年龄较大且身体状况不佳[东部肿瘤协作组(ECOG)评分为3],遂未对其采取手术及化疗措施。此后肿瘤持续进展,患者在接受内镜逆行胰胆管造影(ERCP)并植入胆道支架后,再次出现胆道梗阻。最终,该患者因病情恶化,遂入组接受mRNA疫苗+帕博利珠单抗联合治疗。
结果显示:经过三个周期的治疗,该患者胰头肿瘤病灶在第一次随访时消退(详见下图),根据实体肿瘤疗效评价标准(RECIST),患者达到了部分缓解(PR)。更为惊喜的是,治疗期间,患者仅出现包括接种疫苗后发烧等可控的不良反应。
▼患者001癌症疫苗治疗前后的肿瘤病灶CT对比
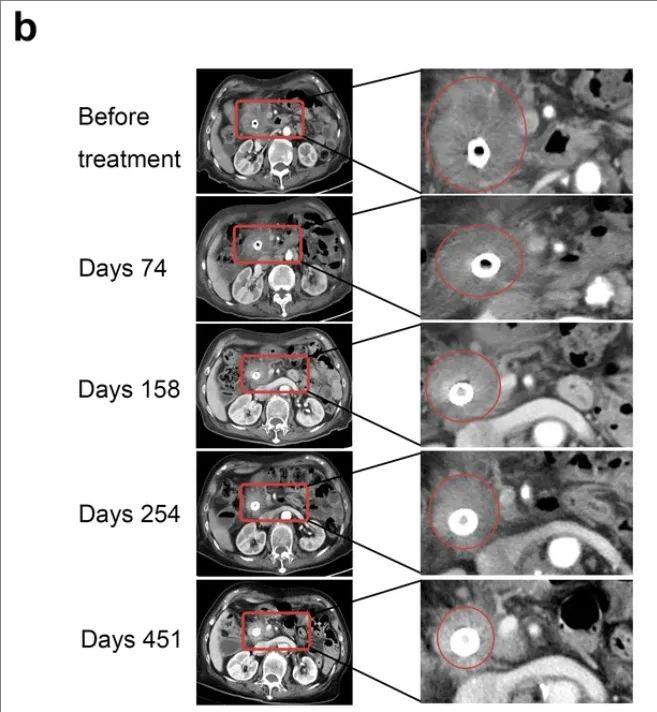
▲图源“cell research”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
患者002为一名69岁男性,在年度体检时发现肺部结节。经CT扫描及正电子发射断层扫描(PET-CT)检查,确认双肺及纵隔淋巴结处存在多个高代谢结节。随后,通过CT引导下穿刺活检,病理诊断为晚期非小细胞肺癌(NSCLC)。由于已错失手术时机,患者接受了帕博利珠单抗及化疗(白蛋白结合型紫杉醇、奈达铂)联合治疗。在完成三个治疗周期后的首次随访中,可见肿瘤病灶明显消退。然而,后续治疗周期中患者出现治疗耐药情况,并伴有严重不良反应,其中以肢体麻木和疲劳为主要表现的神经毒性尤为突出。鉴于此,患者停止化疗,转而选择mRNA疫苗+派姆单抗(即帕博利珠单抗)联合治疗,共进行9个周期。
结果显示:依据实体肿瘤疗效评价标准(RECIST)1.1评估,患者达到部分缓解状态,右肺病灶基本消失,左肺病灶及纵隔淋巴结有所缩小(见图1c)。值得一提的是,在此期间,患者除了出现预期内可控的发热或注射部位疼痛外,未见其他不良反应。
▼患者002癌症疫苗治疗前后的多个肿瘤病灶CT对比
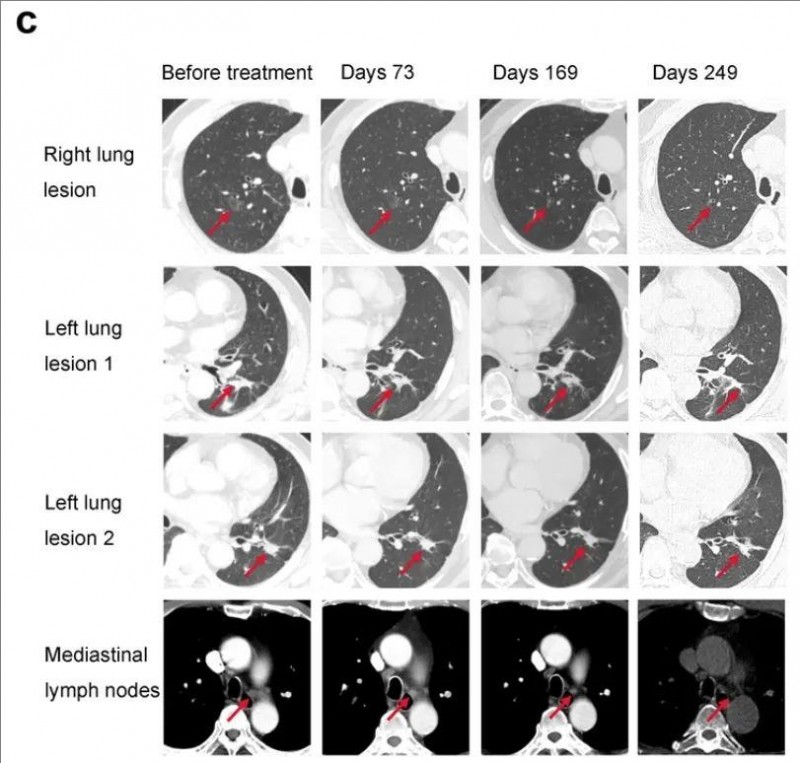
▲图源“cell research”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
想寻求DC疫苗、mRNA疫苗或其他个性化癌症疫苗帮助的患者,可将近期病理报告、出院小结、治疗经历等资料,提交至医学部,进行初步评估。
奇迹上演:WT1-DC疫苗携手化疗,助肺癌全身转移患者无进展生存期超577天
世界知名期刊《Cureus》近期报道了一个令人振奋的案例:一位复发性、多发性肺癌且伴全身转移的患者,在接受WT1树突状细胞疫苗(WT1-DC)治疗后,无进展生存超577天!
该患者是一位69岁的男性,确诊为右肺中叶IV期鳞状细胞癌,同时伴多发性骨转移、多发性肝转移、双侧肾上腺转移等。鉴于其病情,此时该患者已无法耐受手术及放射治疗,遂入组接受WT1树突状细胞疫苗(WT1-DC)+化疗(卡铂AUC6+紫杉醇方案)联合治疗。
结果显示:该患者无进展生存期(PFS)>577天,临床状况良好,体能状态评分为1,可正常生活。此前癌胚抗原(CEA)持续升高,但在联合雷莫芦单抗+多西他赛治疗后,CEA降至5.9。
值得一提的是,治疗前,该患者全身PET-CT检查显示,右下肺存在原发肿瘤,同时伴有多发性双侧肺内转移、多发性肝转移、双侧肾上腺转移、多发性骨转移等全身转移病灶。而在接受WT1-DC治疗第479天,复查PET-CT时发现,该患者全身转移灶明显改善,除右肺一处直径为1.0cm的转移病灶、肝脏一处直径为1.7cm的转移病灶外,未见其他转移灶(详见下图)。
▼该患者WT1-DC治疗前后,全身PET-CT对比
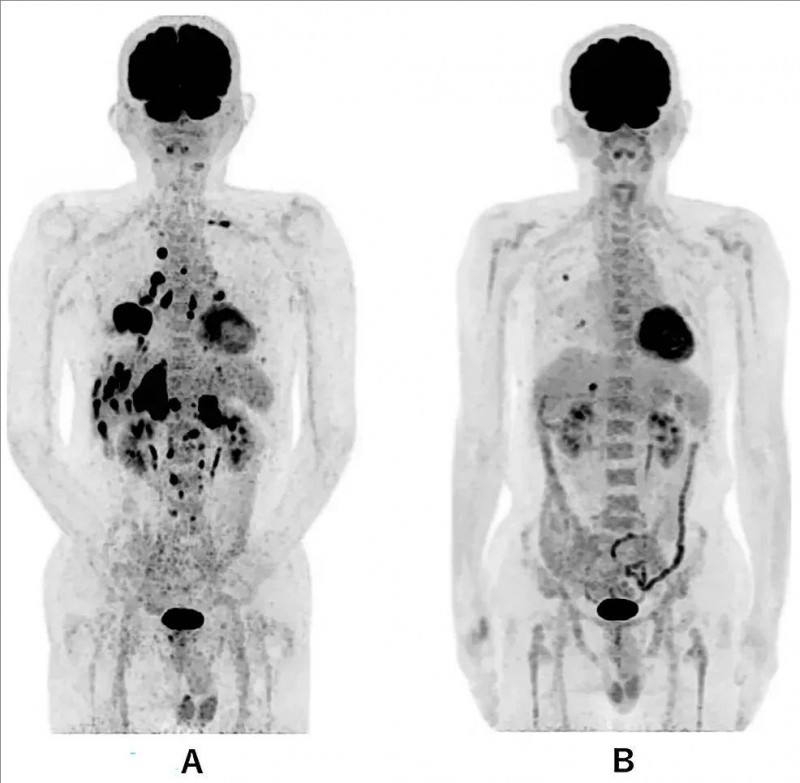
▲图源“Cureus”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
此外,该患者确诊时,胸部CT显示右下肺有原发性肺癌,同时伴有左右胸腔积液。而在接受WT1-DC治疗第114天,肺部原发病灶几乎消失;在治疗第213天,原发病灶虽出现一定程度的复发;但到治疗第338天,原发性及复发性病灶均出现缩小(详见下图)。
▼该患者WT1-DC治疗前后,胸部CT图像对比
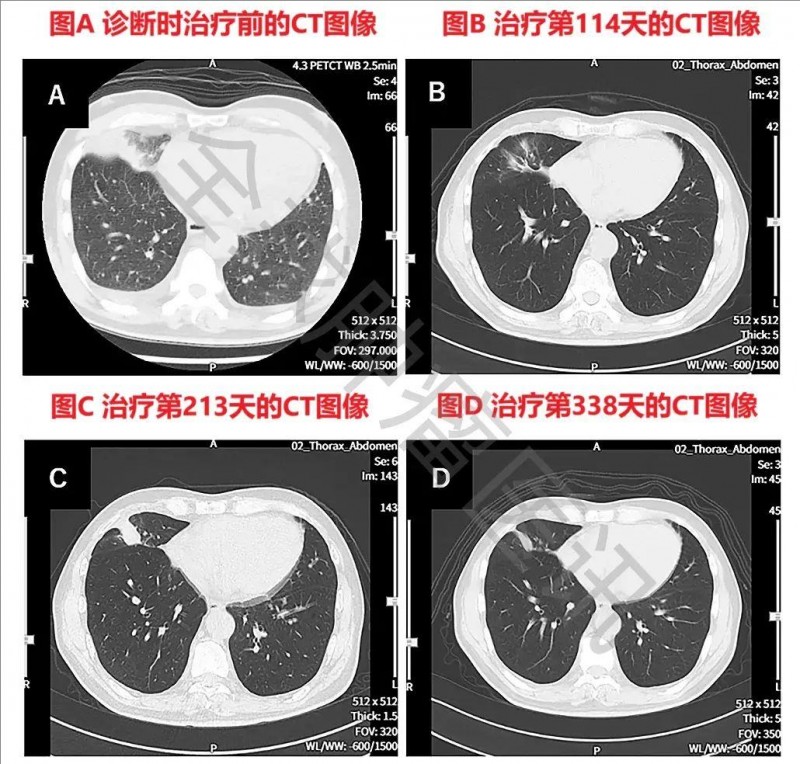
▲图源“Cureus”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
2025国研癌症疫苗火力全开,国内多中心启动临床
1、WGc-043注射液(EB病毒mRNA疫苗):淋巴瘤癌症疫苗
适应证:EB病毒阳性的复发或难治性淋巴瘤患者。
招募信息(部分)
1)筛选时18~75周岁(包括边界值)的男性或女性患者;
2)经组织学或细胞学确诊为标准治疗失败且缺乏有效治疗手段的复发/难治的EBV阳性【原位杂交(ISH或FISH)检测肿瘤组织中EBER阳性】的淋巴瘤,包括不限于:NK/T细胞淋巴瘤、弥漫大B细胞淋巴瘤(DLBCL)、霍奇金淋巴瘤(HL),或其他外周T细胞淋巴瘤(PTCL)等。
2、Vx-001:实体瘤癌症疫苗
适应证:晚期实体瘤/非小细胞肺癌。
招募信息(部分)
1)18周岁≤年龄≤75 周岁,性别不限;
2)经组织学和/或细胞学明确诊断为局部晚期或复发、转移性非小细胞肺癌患者,既往PD-1/PD-L1 治疗失败或不适合 PD-1/PD.L1治疗,且接受过完整含铂类化疗治疗(4~6 个疗程)后,无疾病进展。
3、ABO2102:胰腺癌疫苗
适应证:KRAS突变的晚期胰腺癌患者。
招募信息(部分)
1)年龄≥18 岁;
2)经组织病理学和/或细胞学确诊的晚期胰腺导管腺癌,患者为至少经一线 系统性治疗后疾病进展或无法耐受相关治疗者,或研究者评估认为不适 合化疗,或因其他原因拒绝化疗者。
3)具备研究者认可的基因检测报告,显示携带KRAS G12A、G12C、G12D、 G12V 或 G13D 任一基因突变既往接受过 KRAS 肿瘤疫苗治疗。
4、个体化肿瘤多肽制剂:肝癌疫苗
适应证:晚期肝细胞癌患者。
招募信息(部分)
1)年龄18-70岁(含边界),性别不限,种族不限;
2)既往经手术、靶向治疗或放化疗后发生病情进展,且尚缺乏高级别循证证据支持的进一步有效治疗手段,或诊断时指南中已无相应推荐治疗的晚期肝细胞癌患者;
3)同意并可以获取足够的肿瘤组织及外周血样本,用于全外显子、转录组、单细胞和免疫组库测序。
5、IPM514:消化道肿瘤疫苗
适应证:食管鳞状细胞癌。
招募信息(部分)
1)>18周岁;
2)组织学确诊的食管鳞状细胞癌;
3)至少一线系统性治疗失败,HLA分型为HLAA*02:01和/或 HLA-A*11:01型,脑转稳定。
6、CUD002:卵巢癌疫苗
适应证:难治性/耐药复发性卵巢癌。
招募信息(部分)
1)女性,年龄在18-75周岁(含临界值),体重≥45.0 kg,并自愿签署知情同意书;
2)经病理组织学和/或细胞学检查确诊的卵巢癌患者,WT-1阳性且存在至少一处用RECIST1.1标准可测量的病灶;
3)经研究者判断符合难治性/耐药复发性卵巢癌诊断的患者,既往接受过含铂化疗方案即初始治疗或复发治疗过程中进展的患者或既往接受过含铂化疗方案且末次化疗时间与末次复发时间间隔<6个月的患者。
7、ABO2011:实体瘤癌症疫苗
适应证:进展或转移性晚期实体瘤患者。
招募信息(部分)
1)受试者必须为18岁及以上。
2)经病理组织学或细胞学证实的进展或转移的晚期实体瘤。
3)既往接受过系统性标准治疗后疾病进展或不可耐受毒性(不可耐受毒性定义:>IV级的血液学毒性;或>亚级的非血液学毒性:或>工级的心、肝、肾等主要脏器的损害),且缺乏有效治疗方案的晚期实体瘤。
申请流程
想申请癌症疫苗临床试验的患者,需将近期病理报告、基因检测报告等资料汇总后,提交至医学部,进行初步评估。
小编寄语
癌症疫苗作为癌症治疗领域的新兴力量,历经数十载的发展,展现出了巨大的潜力和前景。随着研究的不断深入和技术的不断进步,我们有理由相信,癌症疫苗将在未来的癌症治疗中,发挥越来越重要的作用,还可与手术、化疗、放疗、免疫治疗等传统治疗手段相结合,形成综合治疗方案,为肿瘤患者带来更高的生存获益!小编也期望随着癌症疫苗的不断优化,未来可以创造出更多的抗癌奇迹!想寻求癌症疫苗等新型抗癌疗法帮助的患者,可将治疗经历、近期病理及影像学检查结果等,提交至全球肿瘤医生网医学部,进行初步评估或申请国内外抗癌专家会诊。
参考资料
[1]Storkus W J,et al.Dendritic cell vaccines targeting tumor blood vessel antigens in combination with dasatinib induce therapeutic immune responses in patients with checkpoint-refractory advanced melanoma[J]. Journal for immunotherapy of cancer, 2021, 9(11): e003675.
https://jitc.bmj.com/content/9/11/e003675
[2]Wang X,et al.Combination therapy of KRAS G12V mRNA vaccine and pembrolizumab: clinical benefit in patients with advanced solid tumors[J]. Cell Research, 2024, 34(9): 661-664.
https://www.nature.com/articles/s41422-024-00990-9
[3]Nagai H,et al.WT1 Dendritic Cell Vaccine Therapy Improves Immune Profile and Prolongs Progression-Free Survival in End-Stage Lung Cancer[J].Cureus,2023,15(10).
https://www.cureus.com/articles/193305-wt1-dendritic-cell-vaccine-therapy-improves-immune-profile-and-prolongs-progression-free-survival-in-end-stage-lung-cancer#!/







































 首页
首页 咨询
咨询 方舟新药
方舟新药 营养商城
营养商城