五大常用肿瘤过继性细胞疗法,开启癌症"临床治愈"的无限可能,打破18年长生存记录
在漫长的医学征程中,化疗时代面对复发、难治性恶性肿瘤这一“超级难题”,虽拼尽全力,却始终无法突破困境,难以抚平患者痛苦的“痛点”,但细胞新药时代有望攻克这一难关。尤其是近年来火爆全球、备受瞩目的CAR-T细胞治疗这一革命性细胞新药,开启了前所未有的、充满无限可能的全新医疗时代,其市场规模高达万亿级。
随着癌症免疫疗法的发展,作为肿瘤免疫疗法的重要分支的过继性细胞疗法(Adoptive Cell Therapy,ACT),逐步成为未来医学发展的关键方向之一,在治疗各种癌症类型方面展现出良好前景。ACT的理念是在体外激活患者自身的免疫细胞,再将其转移回患者体内,以识别和清除癌细胞。目前,常用的过继性细胞疗法(ACT)包括肿瘤浸润淋巴细胞(TIL)、T细胞受体工程化T细胞疗法(TCR-T)、嵌合抗原受体T细胞疗法(CAR-T)、树突状细胞(DC)疫苗等(依据Cellular & Molecular Immunology,2024),为无数被癌症阴霾笼罩的患者带来了重燃生命希望的曙光!
▲截图源自“WILEY”
过继性免疫细胞疗法:攻克肿瘤的前沿利刃
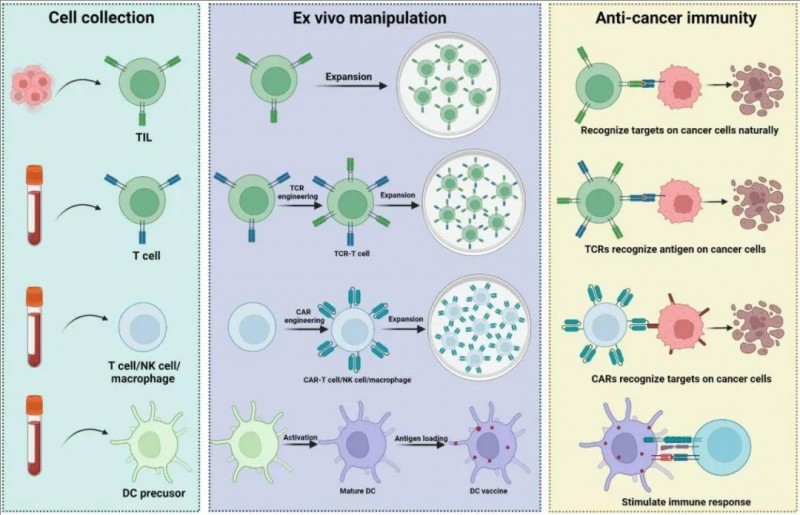
▲图源“WILEY”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
何谓过继性免疫细胞疗法?其主要包括哪些疗法?
过继性免疫细胞疗法(ACT),是从肿瘤患者体内提取免疫活性细胞,在体外对这些细胞进行扩增培养,并开展功能评估,之后再回输到患者体内,以此实现直接杀伤肿瘤,或者激发机体免疫系统对肿瘤细胞发起攻击。相较于其他依赖宿主内在抗肿瘤淋巴细胞的癌症免疫疗法,ACT具有免疫细胞数量充足、功能可按需改造、且免疫反应持久等优势。更为重要的是,作为一种个性化医疗手段,ACT能够有效规避标准治疗方案中,因个体差异而带来的种种问题。
在过往几十年间,ACT 实现了从使用全身淋巴细胞到运用功能性癌症特异性淋巴细胞的重大转变,主要涵盖肿瘤浸润淋巴细胞(TIL)疗法、T细胞受体工程化T细胞疗法、嵌合抗原受体T细胞疗法(CAR-T)、自然杀伤(NK)细胞疗法、树突状细胞(DC)疗法、巨噬细胞疗法等(依据Cellular & Molecular Immunology,2024)。
早期基于肿瘤浸润淋巴细胞(TIL)的ACT疗法,有力推动了转移性黑色素瘤治疗的进步。但遗憾的是,基于TIL的ACT仅对部分患者奏效。为扩大ACT的应用范围,科研人员开发出基因工程技术,将T细胞受体(TCR)和嵌合抗原受体(CAR)导入天然存在的T淋巴细胞中。如今,已有几种类型的基因工程T细胞获批用于临床治疗血液系统恶性肿瘤。不仅如此,这种基因工程方法还拓展到了其他免疫细胞亚群,像自然杀伤(NK)细胞和巨噬细胞。ACT除了直接杀伤肿瘤外,基于树突状细胞(DC)的疫苗接种也是一种常用手段,它能诱导机体产生更强的抗癌免疫反应。当下,ACT正处于持续发展与评估阶段,无论是单独应用,还是与其他免疫疗法联合使用,都在临床试验中有序推进。
过继性免疫细胞疗法的主要治疗过程
基于过继性免疫细胞疗法(ACT)的癌症治疗主要包含三个步骤:
第一步,从患者的外周血或肿瘤组织采集自体免疫细胞;
第二步,在体外对细胞进行扩增培养,和/或通过基因工程技术改造,以增强其抗癌活性;
第三步,将改造后的细胞回输到患者体内,促使肿瘤消退(详见下图)。
▼过继细胞疗法(ACT)治疗过程示例图
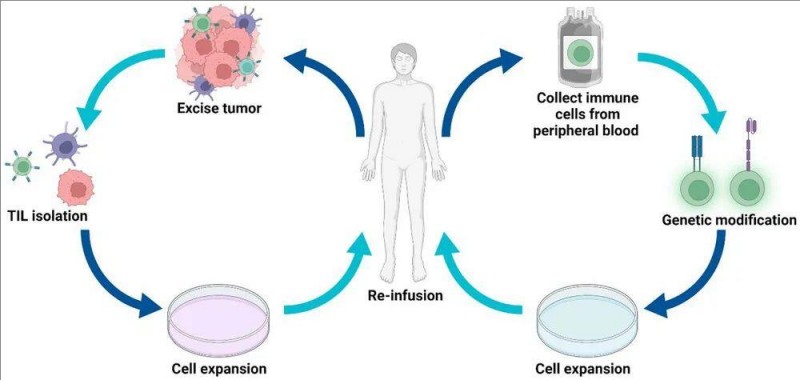
▲图源“WILEY”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
六大过继细胞疗法,开启癌症个性化治疗新时代
01、CAR-T细胞
CAR-T细胞疗法,全称为“嵌合抗原受体T细胞疗法”,是一种基于T细胞介导的CAR的细胞免疫疗法。它借助基因转导技术,向T细胞引入抗原特异性CAR分子,如同给T细胞安装了精准“导航头”,赋予T细胞精确攻击肿瘤的能力,可产生即时和长期的抗癌效果。CAR-T疗法能突破MHC限制,识别癌细胞表面的抗原或蛋白质,有效防止因癌细胞上MHC相关抗原下调导致的免疫逃逸。
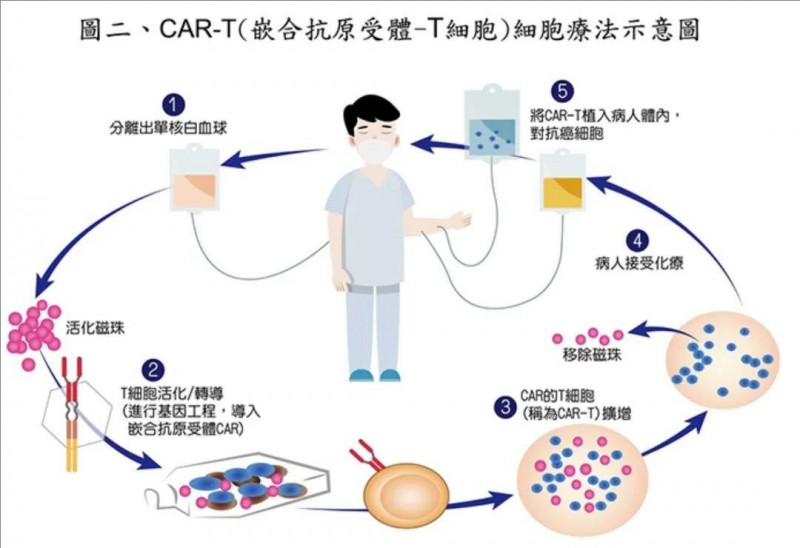
▲图源“TBCF”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
过去几十年,自体CAR-T细胞疗法在恶性肿瘤治疗,特别是血液肿瘤领域成绩斐然。中美等国已相继批准11款CAR-T细胞产品,用于治疗白血病、淋巴瘤、多发性骨髓瘤等多种血液肿瘤。美国食品药品监督管理局(FDA)批准的首个CAR-T疗法,便是用于治疗由骨髓中的前B细胞恶性转化引起的B细胞恶性肿瘤,其特征是B细胞谱系表面标志CD19的高表达。除此之外,FDA还批准了另外三种针对CD19的CAR-T细胞药物,用于治疗急性淋巴细胞白血病(ALL)、弥漫性大B细胞淋巴瘤(DLBCL)。同时,基于间皮素(MSLN)、B细胞成熟抗原(BCMA)、CD123等其他恶性肿瘤表面抗原的CAR-T疗法,也正在临床研究阶段。
▼CAR-T细胞疗法获批药物全汇总
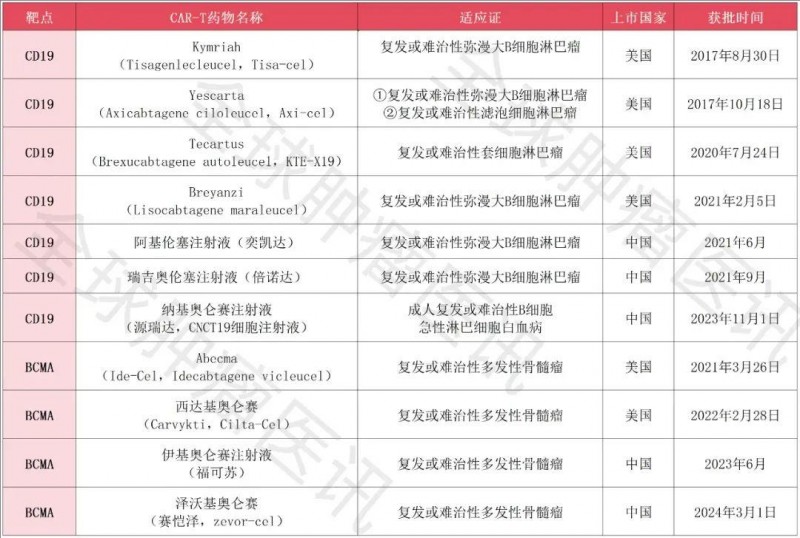
02、肿瘤浸润淋巴细胞(TIL)
“TIL细胞疗法(tumor-infiltrating lymphocytes,TIL)”即“肿瘤浸润淋巴细胞疗法”,虽然也属于过继性免疫细胞疗法,但与CAR-T及TCR-T不同的是,TILs是从患者自身的肿瘤活检组织中,通过DNA测序采集浸润的淋巴细胞,之后在体外进行扩增,最后再回输到患者体内的方法。
TIL细胞相当于深入到敌军内部的免疫细胞敢死队,具有优越的肿瘤病灶浸润能力及低脱靶毒性,可被招募到肿瘤部位直接对抗肿瘤,在治疗黑色素瘤、肝癌、非小细胞肺癌(NSCLC)、卵巢癌、乳腺癌、宫颈癌、结直肠癌(CRC)等多种实体瘤方面,具有独特的优势!
2024年2月16日,美国食品和药物管理局(FDA)批准了一款名为“Lifileucel(LN-144,Amtagvi®)”的TIL细胞产品,用于治疗既往接受过PD-1抗体治疗的不可切除或转移性黑色素瘤成人患者,这也是全球首款上市的TIL疗法,在实体瘤治疗领域具有里程碑式的意义!
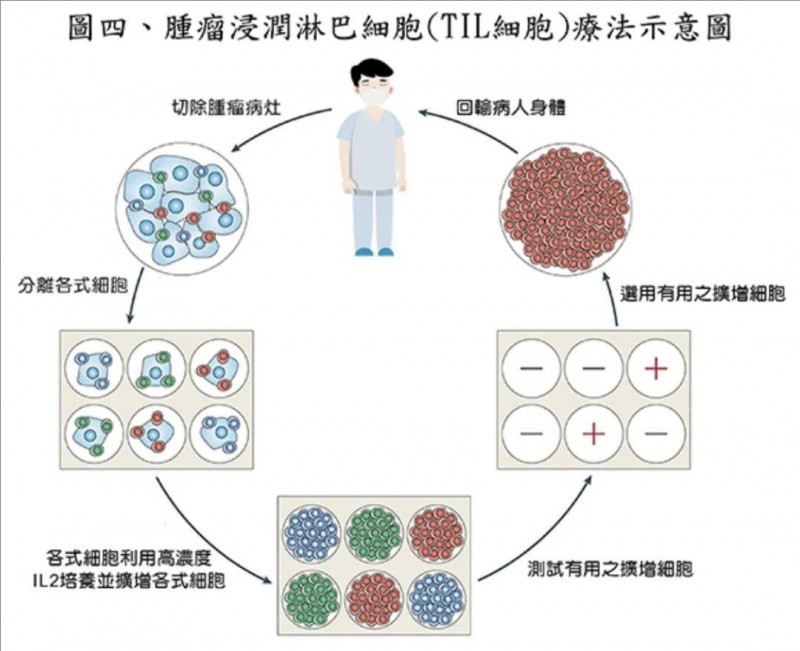
▲图源“TBCF”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
03、TCR-T细胞:实体瘤的利器
“TCR-T细胞疗法”即“T细胞受体工程化T细胞疗法”,是通过基因工程技术,将抗原特异性TCR基因序列(α和β链),转移到T细胞中,使其特异性识别肿瘤抗原,并且精准地杀死癌细胞。
TCR-T细胞可识别细胞膜表面或细胞内来源的肿瘤特异性抗原,其中靶向NY-ESO-1的TCR-T细胞,已在多项实体瘤(如难治复发性黑色素瘤、滑膜肉瘤、肺癌、肝细胞癌、宫颈癌等)的临床试验中,展现出了良好的安全性和有效性,是目前最有可能在实体瘤领域取得突破的T细胞免疫疗法。
2022年初,一款名为“Kimmtrack”的TCR-T细胞产品,获美国食品和药物管理局(FDA)批准,用于治疗葡萄膜黑色素瘤,这也是首款获批上市的TCR-T产品,自此为实体瘤治疗开辟了新的赛道!
04、CAR-NK细胞
“CAR-NK细胞”,全称为“嵌合抗原受体工程化自然杀伤细胞”,是一种新兴的免疫治疗手段。它融合了自然杀伤(NK)细胞天然的抗癌能力,以及嵌合抗原受体(CAR)技术的关键特性。改良后的NK细胞如同安装了“GPS”,能够精准定位并攻击目标。
在血液肿瘤与实体瘤等治疗领域,CAR-NK细胞治疗展现出巨大的应用潜力,有望成为CAR-T治疗的有力替代方案。特别是在实体瘤治疗方面,相较于CAR-T细胞治疗,CAR-NK细胞治疗具有更为显著的先天优势。
临床试验已展示出使用针对多种抗原的CAR-NK细胞治疗多种肿瘤的令人振奋的成果。目前,主要针对CD19、CD22、BCMA、CD33、CD7等靶点的CAR-NK疗法临床研究正在开展,用于治疗造血系统恶性肿瘤。此外,CAR-NK疗法也已应用于胶质母细胞瘤、卵巢癌、肝细胞癌、前列腺癌等实体瘤的治疗。
▼不同过继细胞疗法(ACT)的比较
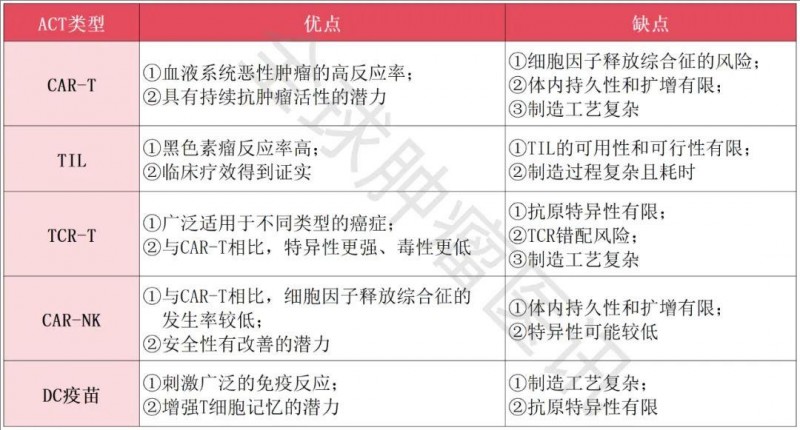
05、树突状细胞(DC)疫苗
树突状细胞(dendritic cell,DC)属于一类多功能抗原提呈细胞。它通过自身上的主要组织相容性复合体(MHC)分子与T细胞上的T细胞受体相互作用,同时借助共刺激分子,来对免疫反应进行调节。研究者充分利用树突状细胞摄取和呈递抗原的特性,深入挖掘其抗癌潜力。尤其是树突状细胞具备向细胞毒性T淋巴细胞(CTL)和辅助性T淋巴细胞交叉呈递抗原的潜力,因此,它能够作为疫苗,用于激发细胞毒性抗肿瘤免疫反应。
在癌症免疫治疗领域,过继性树突状细胞移植已作为癌症疫苗展开研究。树突状细胞疫苗(DC疫苗)的治疗过程是,先从癌症患者体内提取树突状细胞(DC),使其负载某种肿瘤相关抗原(TAA)来源,随后再将其回输到患者体内。实践证明,树突状细胞疫苗能够在各类免疫细胞中,引发具有针对性的强效抗癌免疫反应。
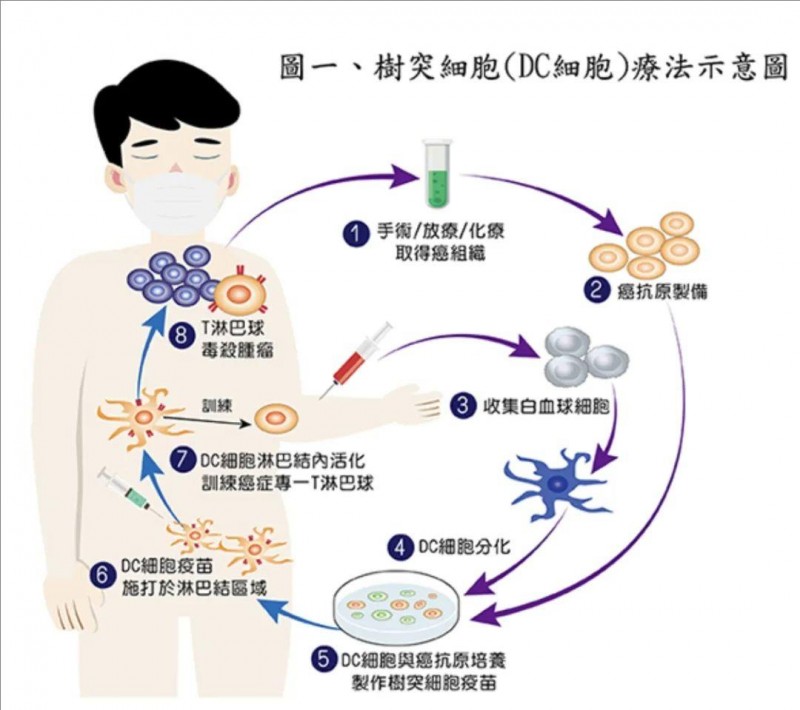
▲图源“TBCF”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
Sipuleucel-T是一种树突状细胞疫苗,它采用重组融合蛋白抗原,如前列腺酸性磷酸酶(PAP)和粒细胞-巨噬细胞集落刺激因子(GM-CSF)。目前,Sipuleucel-T是唯一一款获得临床批准,专门用于治疗前列腺癌的树突状细胞疫苗。
中国患者如何寻求肿瘤过继细胞疗法帮助
目前,国内多家癌症中心启动CAR-T、TILs、TCR-T疗法的临床试验,针对各类晚期实体瘤,进行临床招募。
1、CAR-T疗法:正在招募多发性骨髓瘤、复发/难治性淋巴瘤、胰腺癌、肺癌、肝癌、胃癌、结直肠癌、卵巢癌等癌种。
2、TCR-T疗法:目前TCR-T疗法的临床试验正在进行乙型肝炎病毒相关肝细胞癌、妇科恶性肿瘤(卵巢癌、子宫内膜癌)、晚期葡萄膜黑色素瘤、鼻咽癌、血液系统恶性肿瘤等癌种的招募。
3、TILs疗法:国内的TILs疗法已获得批准正式开展人体临床试验,包括肺癌、宫颈癌、乳腺癌、黑色素瘤、头颈部肿瘤等实体瘤,目前正在招募患者。
想要参加的患者,可先将治疗经历、出院小结、近期病理报告等资料,提交至医学部,了解详细的入排标准,并进行初步评估!
CAR-T暴击血液肿瘤,完全缓解率高达82%
全球知名期刊《Nature medicine》曾报道一项针对复发/难治性B细胞急性淋巴细胞白血病(B-ALL)、大B细胞淋巴瘤(LBCL)的1期临床研究(NCT03233854)。
该研究结果显示,LBCL组的完全缓解(CR)率达29%,B-ALL组CR率更是高达82%。其中,一位伴有全身转移的B细胞急性淋巴细胞白血病(B-ALL)患者(SA8),在输注CAR-T细胞6个月后,奇迹般地达到完全缓解(CR),总体CR率为88%(详见下图)。
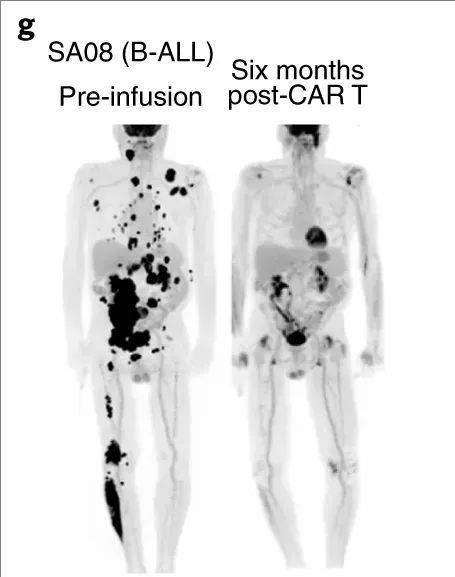
▲图源“nature medicine”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
CAR-T治疗实体瘤破纪录,神经母细胞瘤患者生存超18年
尽管CAR-T在血液病治疗领域前景广阔,但长期以来,其在实体瘤治疗中的疗效一直差强人意。令人欣慰的是,当下研究人员正全力以赴推动CAR-T细胞疗法在实体肿瘤治疗中的应用,重点聚焦于提升细胞运输与浸润效果。同时,他们也在积极开发更高效、标准化的CAR-T细胞制造方法,以增强其可扩展性与可及性。
振奋人心的是,近日全球知名期刊《Nature》头版发布了一则重磅消息:一位神经母细胞瘤患儿接受CAR-T细胞治疗后,已持续缓解超18年,且在此期间无需额外治疗,该研究成果同时在《NatureMedicine(自然医学)》杂志发表。
▲截图源自“Nature”
本次1期临床研究时间跨度为2004年至2009年,共纳入19例神经母细胞瘤患儿。结果显示:15年无事件生存率(EFS)为31.6%,其中活动性疾病患者为18.2%,NED患者为50%(P=0.044,详见下图)。
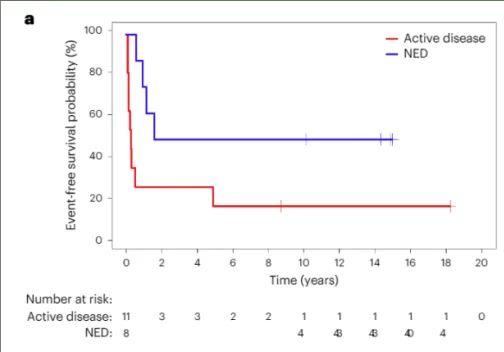
▲图源“Nature Medicine”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
在11名输注时患有活动性疾病的患者中,1例达到部分缓解(PR),3例成功实现完全缓解(CR)。在这3例完全缓解的患者里,2例患者的完全缓解(CR)状态持续了8年,1例患者的完全缓解(CR)状态更是奇迹般地持续了18年以上。据悉,在这长达18年的时间里,该患者未接受过其他针对癌症的治疗。更让人惊喜的是,她之后两次成功足月怀孕,均顺利生下正常婴儿。从目前已知信息来看,她很可能是接受CAR-T治疗的癌症患者中,存活时间及完全缓解持续时间最长的病例!这一成果为实体瘤患者带来了希望的曙光,具有非凡的里程碑意义。
TCR-T疗法暴击乙肝病毒相关肝细胞癌,肿瘤缩小74.5%,病毒100%清除
SCG101是一种乙肝抗原特异性的TCR-T细胞疗法,可以特异性靶向HBV抗原相关T细胞表位,有效清除HBV-HCC肿瘤细胞、HBV-DNA整合的癌前病变细胞和HBV感染细胞,维持持续的抗肿瘤和抗病毒效应。在国际细胞与基因治疗大会(ISCT)上,公布了SCG101治疗乙肝病毒相关肝细胞癌的惊艳数据。
一位确诊HBV相关肝细胞癌的患者,在接受单剂SCG101治疗后,获得部分缓解(PR)。在输注第28天,肿瘤靶病灶相比基线缩小66%,达到部分缓解(PR),并在治疗第4个月,肿瘤进一步缩小74.5%;另一处病灶完全消失。目前该患者肿瘤未进展时间已超过6.9个月,且保持持续的缓解状态。更为惊喜的是,乙肝表面抗原阳性肝细胞实现100%清除,HBV血清学标志HBsAg从557.96 IU/mL(治疗前),降至0.08 IU/mL(SCG101输注第28天)。
▼该患者在回输SCG101前后的影像学变化
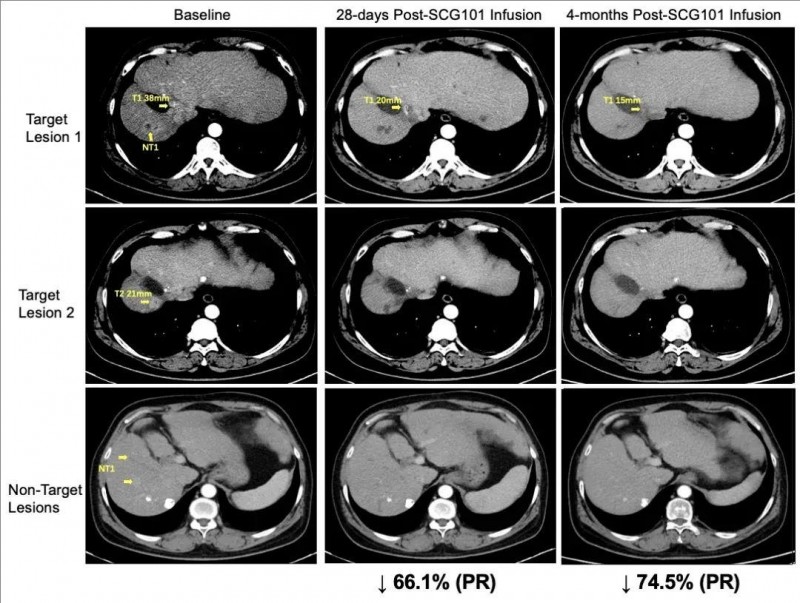
▲图源“SCG”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
见证奇迹!TIL细胞疗法助转移性乳腺癌患者,获得完全缓解
《临床肿瘤学杂志》曾报道过这样一个令人瞩目的案例:一位转移性乳腺癌患者,在接受TIL细胞疗法联合派姆单抗治疗后,竟奇迹般地获得了完全缓解。
TIL细胞治疗前,这位患者的胸壁(左上部位)、肝脏(左下部位)已出现转移病灶。在入组接受TIL细胞治疗后,其肿瘤完全缩小(详见下图),并最终成功实现了完全缓解(CR)。而更为振奋人心的是,在完成治疗5年后的复查影像学结果显示,她至今依然保持着无癌状态!
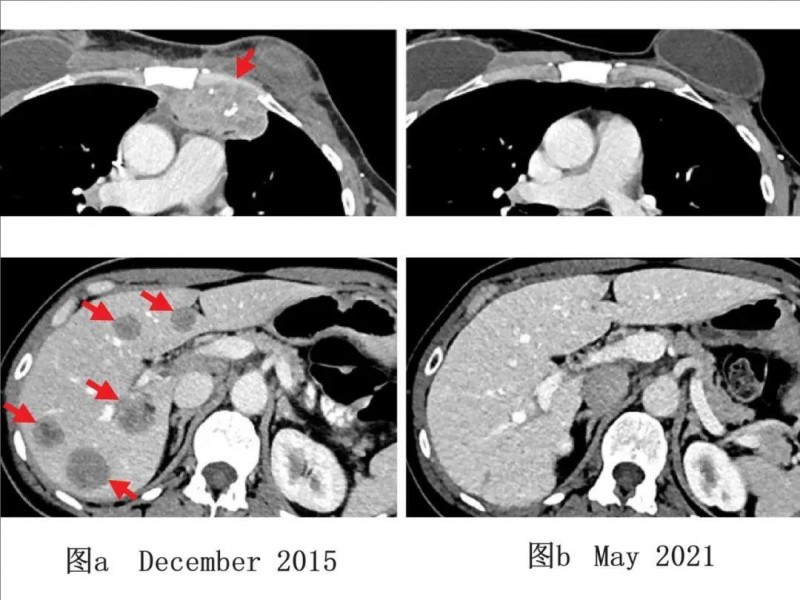
▲图源“NCI”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
CAR-NK细胞猛攻CD19阳性淋巴瘤/白血病等,客观缓解率高达73%
近日,MD安德森癌症中心开展了一项名为“应用CD19CAR-NK细胞(一种靶向CD19的CAR转导的自然杀伤细胞),治疗CD19阳性淋巴瘤”的临床研究(NCT03056339)。该研究共招募了44名复发性或难治性CD19阳性肿瘤患者,涵盖慢性淋巴细胞白血病(CLL)、非霍奇金淋巴瘤。
研究结果显示:客观缓解率(ORR)高达73%,其中有7例患者(包括3例慢性淋巴细胞白血病患者、4例淋巴瘤患者)奇迹般获得了完全缓解(CR)。
尤其值得关注的是,其中一位发生Richter转化的慢性淋巴细胞白血病(CLL)患者(患者 5),其高级别淋巴瘤也实现了完全缓解(CR)(详见下图)。
▼该患者CAR-NK细胞输注前后的FDG PET-CT、PET-CT对比
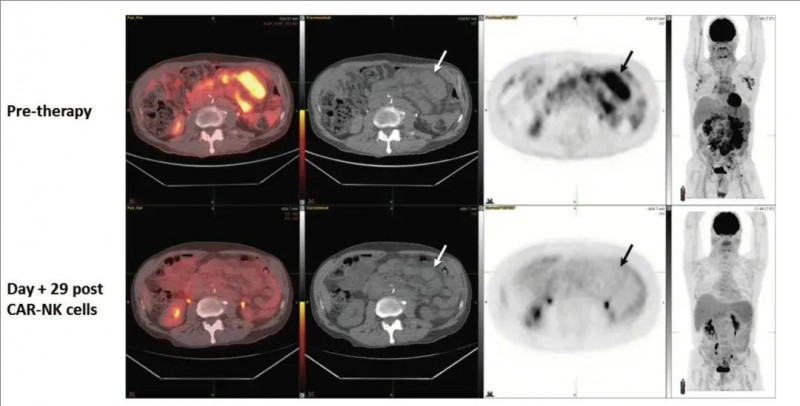
▲图源“N Engl J Med”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
WT1-DC携手化疗,肺癌全身转移患者无进展生存期超577天
全球知名《Cureus》杂志近期报道了一则振奋人心的案例:一位复发性、多发性肺癌全身转移患者,在接受WT1-DC+化疗联合治疗后,无进展生存竟然超过了577天!
该患者是一位69岁男性,确诊为右肺中叶IV期鳞状细胞癌,伴有多发性骨转移、肝转移及双侧肾上腺转移等,此时其身体状况已无法耐受手术与放疗,遂入组接受WT1树突状细胞疫苗(WT1-DC)联合化疗(卡铂AUC6+紫杉醇方案)治疗。
治疗结果显著:患者无进展生存期(PFS)超577天,体能状态良好(评分为1),能够正常生活。虽癌胚抗原(CEA)曾持续上升,但在联合雷莫芦单抗与多西他赛后,CEA降至5.9。
从影像检查来看,患者确诊时胸部CT显示右下肺原发性肺癌,伴有左右胸腔积液。经WT1-DC治疗114天后,肺部原发病灶近乎消失;治疗213天时,原发病灶虽有所复发;但到第338天,原发性及复发性病灶均缩小(详见下图)。
▼WT1-DC治疗前后胸部CT图像对比

▲图源“Cureus”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
此外,治疗前全身PET-CT显示:患者除右下肺原发肿瘤外,还存在多发性双侧肺内、肝、双侧肾上腺及骨转移等全身转移灶。而在WT1-DC治疗479天复查PET-CT发现,全身转移灶显著改善,除右肺一处1.0cm转移病灶、肝脏一处1.7cm转移病灶外,未见其他转移灶(详见下图)。
▼WT1-DC治疗前后全身PET-CT对比

▲图源“Cureus”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
小编寄语
癌症治疗长期以来都是全球医学领域面临的棘手难题。传统的手术、放疗和化疗等抗癌方法,存在较高的复发或转移风险,因此,开发新型抗癌手段迫在眉睫。随着医学技术持续进步,癌症治疗逐步迈入精准治疗时代。以CAR-T、TCR-T、TIL细胞疗法为代表的免疫细胞疗法,主要通过调动人体自身免疫细胞,精准识别并消灭癌细胞,同时对正常细胞组织损伤较小,彻底革新了传统抗癌模式。
不过,需要特别提醒病友们,癌症是一种极为复杂的疾病,单一治疗手段往往难以达到理想效果,通常建议采用综合性治疗方案。患者应依托权威医院及权威专家的正规治疗,在采取常规治疗手段(手术、放疗、化疗)治疗后,根据自身的经济情况,辅助免疫治疗技术等综合治疗方法,以达到巩固治疗效果、预防复发、提高生活质量,延长生存期等目的!
想寻求CAR-T、TILs、TCR-T、CAR-NK细胞疗法、DC疫苗或其他国内外抗癌新技术帮助的患者,可先将治疗经历、出院小结、近期病理报告等资料,提交至全球肿瘤医生网医学部,详细评估病情或申请国际会诊。
参考资料
[1]Du S,et al.Adoptive cell therapy for cancer treatment[C]//Exploration. 2023, 3(4): 20210058.
https://onlinelibrary.wiley.com/doi/full/10.1002/EXP.20210058
[2]Yagawa Y,et al.Peritoneal Dissemination and Malignant Ascites in Duodenal Cancer Successfully Treated With Adoptive Cell Therapy Using WT1-and MUC1-Pulsed Dendritic Cells and Activated T Cells With No Adverse Effects: A Case Report[J]. Cureus, 2024, 16(11).
https://www.cureus.com/articles/308954-peritoneal-dissemination-and-malignant-ascites-in-duodenal-cancer-successfully-treated-with-adoptive-cell-therapy-using-wt1--and-muc1-pulsed-dendritic-cells-and-activated-t-cells-with-no-adverse-effects-a-case-report#!/
[3]https://www.scgcell.com/newsinfo/6283011.html







































 首页
首页 咨询
咨询 方舟新药
方舟新药 营养商城
营养商城