如果您的基因检测报告有如下靶点突变,请及时联系我们,帮您匹配相关新药。
EGFR、ALK、ROS1、KRAS、NTRK、MET等
截止2021年上半年,FDA已经批准了款靶向药,CAR-T临床试验
已帮助个患者成功匹配相关临床实验并从中获益
提交病历资料:出院小结、重要检查报告、影像报告 (CT、核磁、Petct等)、病理报告、基因检测报告、 影像资料胶片或Dicom格式电子文件




如果您的基因检测报告有如下靶点突变,请及时联系我们,帮您匹配相关新药。
EGFR、ALK、ROS1、KRAS、NTRK、MET等
截止2021年上半年,FDA已经批准了款靶向药,CAR-T临床试验
中国上市
恩替司他片与芳香化酶抑制剂联合,治疗激素受体(HR)阳性、人类表皮生长因子受体-2(HER-2)阴性,经内分泌治疗复发或进展的局部晚期或转移性乳腺癌
恩替司他片是一种组蛋白去乙酰化酶(HDAC)抑制剂,可选择性抑制I类和IV类HDACs,抑制细胞增殖、促进终末分化和/或诱导凋亡,发
中国上市
用于成人HER2阳性早期和转移性乳腺癌的治疗
帕妥珠曲妥珠单抗注射液是美国罗氏制药研发的一款将曲妥珠单抗和帕妥珠单抗两药组合的复方制剂。2024年1月2日,获中国国家药品监
中国上市
特瑞普利单抗与紫杉醇(白蛋白结合型)联合,用于PD-L1阳性(CPS≥1)的复发或转移性三阴性乳腺癌(TNBC)的一线治疗
2024年6月25日,特瑞普利单抗新适应症的上市申请获得国家药品监督管理局(NMPA)批准,与紫杉醇(白蛋白结合型)联合,用于PD-L1
2020年12月17日,FDA批准了新药与化疗的联合用药方案,用于治疗HER2阳性的转移性乳腺癌成年患者。接受此类方案治疗的患者,应已经接受过2种或更多的抗HER2治疗方案,其中至少1种方案用于治疗转移性疾病。
MARGENZA(margetuximab-cmkb)简介通用名:margetuximab-cmkb商品名:MARGENZA全部名称:MARGENZA,margetuximab-cmkb适应症:M
2021年7月26日,美国食品药品监督管理局批准派姆单抗(Keytruda,默克)联合化疗作为新辅助治疗用于高危、早期、三阴性乳腺癌(TNBC),然后单药作为手术后的辅助治疗。
一项Ib/II 期PANACEA 试验数据显示,HER-2阳性乳腺癌患者对赫赛汀耐药后继续派姆单抗(Keytruda)联合赫赛汀治疗可持续获益。有
2021年4月7日,FDA 定期批准 sacituzumab govitecan 用于治疗三阴性乳腺癌
2020年4月22日,美国食品药品监督管理局FDA加速批准Trodelvy(sacituzumab govitecan-hziy)用于先前已接受过至少两种疗法治疗的
2017年9月,获得FDA首次批准联合氟维司群治疗HR阳性,HER2阴性晚期乳腺癌患者,这些患者之前内分泌治疗后疾病进展。在2018年2月,abemaciclib被批准与芳香酶抑制剂(AI)联合用作为一线疗法 ,用于治疗HR阳性,HER2阴性晚期或转移性乳腺癌的绝经后妇女。2021 年 10 月 12 日,FDA批准 abemaciclib(Verzenio,礼来公司)与内分泌疗法(他莫昔芬或芳香酶抑制剂)联合用于激素受体(HR)阳性、人表皮生长因子成人患者的辅助治疗受体 2 (HER2) 阴性、淋巴结阳
商品名:VERZENIO英文名:abemaciclib(玻玛西尼)规格:50,100,150,200mg厂家:礼来靶点:CDK4/6美国获批:2017年图注:美国原
已帮助患者成功匹配相关临床实验并从中获益
提交病历资料:出院小结、重要检查报告、影像报告 (CT、核磁、Petct等)、病理报告、基因检测报告、 影像资料胶片或Dicom格式电子文件





赫赛莱的中文全名叫恩美曲妥珠单抗,英文全名叫Trastuzumab Emtansine,缩写是T-DM1。...
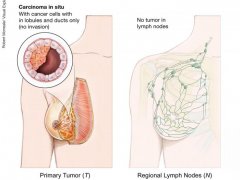
癌症分期是用于描述癌症生长的位置、大小和是否已经扩散到其他部位。医生通过诊断检查发现癌症分期,所以在所有检查完成前可能不会有明确分期。明确癌症分期可以帮助医生决定最好的治疗方案和预测患者的治疗预后。不同的癌症有不同类型的分期方式。...
接诊患者后,医生首先根据体检和影像学检查对乳腺癌患者进行 cTNM 分期,并以此制定治疗方案;对于接受手术的患者,术后标本送至...

许多患者病情进展到晚期,或发生转移,5年生存率急剧下降,仍然需要更多有效的药物来改善生存情况。...
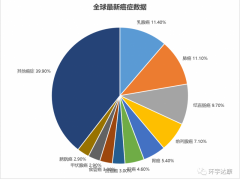
近日,世界卫生组织国际癌症研究机构(IARC)发布了2020年全球最新癌症负担数据显示,乳腺癌已超越肺癌成为全球最常见癌症!仅在美国,就将有近30万人被诊断出患有乳腺癌。...

今天,美国食品药品监督管理局(FDA)宣布授予乳腺癌新药图卡替尼的新药优先审批申请(NDA)。...