时间:2024-11-01 16:35 编辑:全球肿瘤医生网
美通社2024年10月31日报道,PD-L1抑制剂舒格利单抗注射液(择捷美、Sugemalimab)在英国获批用于转移性非小细胞肺癌
据美通社2024年10月31日报道,我国自研的PD-L1单抗药物舒格利单抗,获得英国药品和医疗保健用品管理局(MHRA)批准,与含铂化疗联合,用于转移性非小细胞肺癌(无EGFR敏感突变、无ROS1、ALK或RET基因组肿瘤变异)成人患者的一线治疗。
这是继今年7 月获得欧盟委员会批准后,舒格利单抗在海外市场获得的第二项上市许可申请的批准,并在今年的ESMO大会上,公布了其长期生存数据!舒格利单抗也成为了我国首个成功出海的国产PD-L1单抗药物,顺利拿到了欧盟和英国的入场券!
▲截图源自PR Newswire
国产舒格利单抗,我国获批五大适应证
舒格利单抗注射液(sugemalimab,择捷美)是由我国自主研发的一款抗PD-L1单克隆抗体,在患者体内产生免疫原性及相关毒性的风险更低,这使得舒格利单抗与同类药物相比,具有独特的优势。目前舒格利单抗在我国已有五大适应证获批,分别用于治疗:
1、同步或序贯放化疗后,未见疾病进展、不可切除、III期非小细胞肺癌(NSCLC)。
2、与化疗联合,作为转移性鳞状及非鳞状非小细胞肺癌(NSCLC)患者的一线治疗。
3、与铂类化疗药和氟尿嘧啶类药物联合,作为局部晚期、不可切除的、复发或转移性食管鳞癌的一线治疗。
4、用于复发或难治性的结外NK/T细胞淋巴瘤的治疗。
5、与铂类药物和氟尿嘧啶类联用,作为表达PD-L1(CPS5)的不可切除的局部晚期或转移性胃及胃食管结合部腺癌的一线治疗(2024年3月15日上市)。
舒格利单抗Ⅲ期临床数据惊艳,非小细胞肺癌4年总生存率提高15%
舒格利单抗本次在英国获批,主要是基于2024年欧洲肿瘤内科学会(ESMO)年会上,公布的一项GEMSTONE-302的III期临床研究(NCT03789604)的惊艳数据,研究结果同步发表在全球著名期刊《Nature Cancer》上。
本次研究共入组479例未经治疗的IV期鳞状或非鳞状非小细胞肺癌(NSCLC)患者,这些患者无EGFR、ROS1、ALK或RET融合突变,将其随机分为两组,即舒格利单抗组(n= 320)、安慰剂组(n= 159)。结果显示如下:
1、中位总生存期(OS):在意向治疗(ITT)人群中,患者病情显著改善,中位OS分别为25.2个月(舒格利单抗组) vs 16.9个月(安慰剂组)(详见下图)。值得一提的是,舒格利单抗联合化疗将非小细胞肺癌患者4年总生存(OS)率提高近15%,4年OS率分别为32.1%(舒格利单抗组) vs 17.3%(安慰剂组)。其中,鳞癌患者4年OS率提高近16%,非鳞癌患者4年OS率提高15%。舒格利单抗在治疗鳞癌与非鳞癌方面,尤其是以全Ⅳ期患者为基线的免疫研究中,四年总生存率的提高幅度遥遥领先!
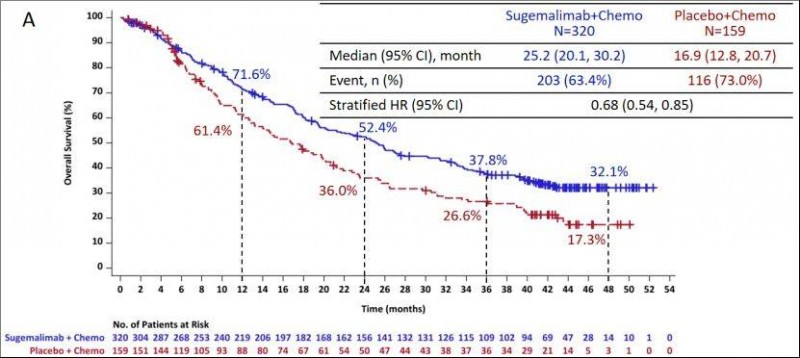
▲图源Nature Cancer,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
2、中位无进展生存期(PFS):在意向治疗(ITT)人群中,中位PFS分别为9.0个月(舒格利单抗组) vs 4.9个月(安慰剂组)。
3、伴脑转移患者的中位总生存期(OS):伴有脑转移的非小细胞肺癌患者的中位OS分别为26个月(舒格利单抗组) vs 9个月(安慰剂组)。值得一提的是,即便是伴脑转移的患者,舒格利单抗治疗后的4年总生存率也高达36.4%(详见下图)!
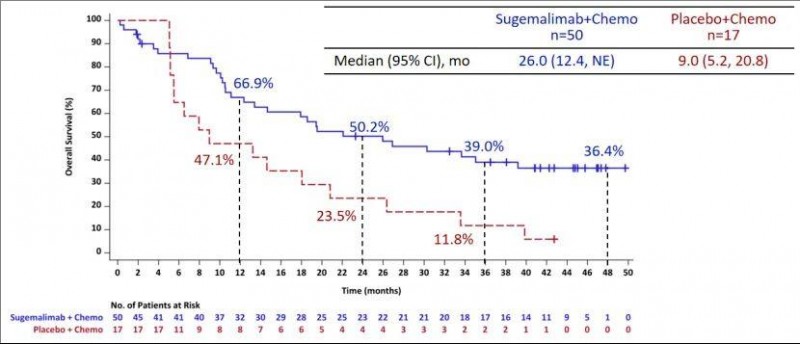
▲图源Nature Cancer,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
小编寄语
舒格利单抗本次在英国获批,标志着我国抗癌新药全球化布局迎来了又一重要的里程碑。而且今年在ESMO上公布的长期生存数据,更是进一步巩固了舒格利单抗在转移性NSCLC一线治疗格局中的重要地位,在3期临床研究中,更是将非小细胞肺癌患者的4年总生存率提高近15%,而且无论治疗鳞癌亦或是肺鳞癌,其4年生存率提高幅度均遥遥领先!
除了上文提到的舒格利单抗外,近期还有多款肺癌治疗新药获批上市或开展临床研究!对目前治疗方案不满意的患者,可将近期影像学检查、病理检查、治疗经历等资料,汇总后提交至医学部,初步评估是否有机会参加临床新药试验,或者通过方舟计划寻求免费用药的机会!
参考资料
[1]Zhou C,et al.Interim survival analysis of the randomized phase III GEMSTONE-302 trial: sugemalimab or placebo plus chemotherapy as first-line treatment for linkstatic NSCLC[J]. Nature cancer, 2023, 4(6): 860-871.
https://www.nature.com/articles/s43018-023-00578-z
[2]https://en.prnasia.com/releases/apac/cstone-announces-mhra-approval-of-sugemalimab-for-first-line-treatment-of-non-small-cell-lung-cancer-nsclc-in-the-uk-466706.shtml
本网站新闻资讯、文章、研究数据、治疗案例均来自于国内外医学论文,所涉及到的新药、新技术有可能还处于临床研究阶段,患者不能作为治疗疾病的依据。癌症治疗目前尚无治愈手段,患者需要在医生的指导下,在医院接受正规治疗或参加新药新技术临床试验。