注射用重组抗HER2人源化单克隆抗体临床试验,比较安瑞泽和赫赛汀治疗乳腺癌安全性有效性的III期试验
1、试验目的
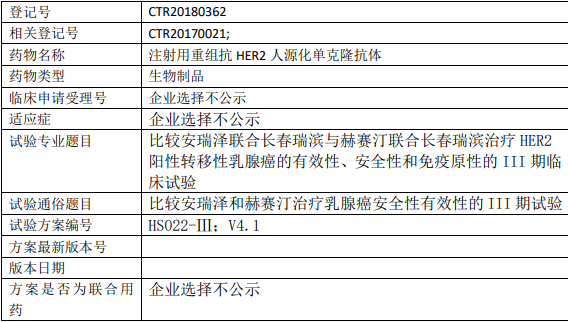
比较安瑞泽®(HS022)+长春瑞滨与赫赛汀®+长春瑞滨治疗 HER2 阳性的转移性乳腺癌的有效性、安全性、免疫原性。
2、试验设计
试验分类:安全性和有效性
试验分期:III期
设计类型:平行分组
随机化:随机化
盲法:双盲
试验范围:国内试验
3、受试者信息
年龄:18 岁(最小年龄)至 75 岁(最大年龄)
性别:女
健康受试者:无
入选标准
1.女性,年龄≥18 周岁且≤75 周岁(以签署知情同意书当天为准)者
2.组织学确诊的乳腺癌者;
3.无法实施根治手术和/或放射性治疗的复发或转移性乳腺癌者;
4.HER2 阳性乳腺癌者,HER2 阳性的定义:包括 IHC(+++)或 ISH阳性;IHC(++)应进一步通过荧光原位杂交(FISH)或显色原位杂交(CISH)、银增强原位杂交(SISH)等方法进行 HER2 基因扩增检测;
5.乳腺癌复发/转移后未接受过解救性全身治疗,这些治疗包括化疗、抗 HER2 治疗、其他靶向治疗或其他试验性抗肿瘤治疗。若既往曾接受过含曲妥珠单抗的(新)辅助治疗,且停用曲妥珠单抗至复发/转移之间的间期≥12 个月者允许纳入。
6.至少具有一个可测量的靶病灶(RECIST 1.1 标准)者:靶病灶至少有一条径线可以被精确测量,并且放疗后或经其他局部区域性治疗后的病灶只被评估为非靶病灶。骨转移病灶不作为可测量病灶;
7.东部肿瘤协作组(ECOG)体力状态评分小于 2 者;
8.随机入组前 4 周内左心室射血分数(LVEF)≥50%者;
9.充分的血液学、肝功能和肾功能,如以下实验室检查值所示:
a)中性粒细胞绝对值≥1.5×10^9/L;
b)血小板≥100×10^9/L、或血红蛋白≥90g/L;
c)血清总胆红素≤1.5 倍正常值上限(受试者有吉尔伯特综合征除外);
d)谷丙转氨酶和谷草转氨酶≤2.5倍正常值上限(肝转移的受试者≤5 倍正常值上限);
e)血肌酐≤1.5 倍正常值上限。
10.预计生存期≥3 个月者。
11.自愿签署知情同意书者。
排除标准
1.随机入组前 4 周内接受过重大手术或预期在试验期间实施重大手术者;或随机入组前 4 周内接受过辅助化疗者;或随机入组前
2 周内接受过放疗者;或随机入组前 2 周内接受过针对复发/转移性乳腺癌的内分泌治疗者;
2. 既往曾接受过长春瑞滨治疗者;
3. 随机入组时存在≥2 级的外周神经病变(CTC AE v4.03)者;
4. 有症状或未经治疗的已知脑转移或其他 CNS 转移。已完全切除和/或放疗后证明稳定或改善的中枢神经系统转移不是一项排除标准,只要影像学(CT/MRI)显示在筛选前稳定至少 4 周,且无脑水肿证据及无需糖皮质激素或抗惊厥药物;
5. 随机入组前 4 周内参与了其他临床试验者(如为单克隆抗体临床试验,则为 3 个月);
6. 既往 5 年内患有任何其它恶性肿瘤,不包括完全治愈的宫颈原位癌、基底细胞或鳞状上皮细胞皮肤癌患者;
7. 既往有明确的神经或精神障碍史,包括癫痫或痴呆;
8. 对于试验用药品的任何成分或辅料过敏,包括对苯甲醇过敏者;
9. 随机入组前 2 周内接受过全血或成分血输血者;
10. 目前患有影响静脉注射、静脉采血疾病者;
11. 目前存在严重的、不能控制的系统性疾病(如呼吸困难、支气管痉挛、哮喘急性发作期或其他需要持续吸氧治疗的疾病等),经研究者判断会显著影响受试者参加/完成试验、及疗效评估;
12. 具有下列任一心脏疾病者:
a)目前患有未经治疗的或经治疗无法控制的高血压(收缩压>150mmHg 或舒张压>100mmHg),或不稳定性心绞痛;
b)按照纽约心脏病学会标准,目前患有任一级别的充血性心力衰竭病史,或严重的需要治疗的心律失常(房颤或阵发性室上性心动过速除外);
c)签署知情同意书前 6 个月内曾发生过心肌梗塞;
13. 目前需要每天全身性使用皮质类固醇药物进行长期治疗者(剂量>10 mg/天的甲泼尼龙的等效剂量),吸入性皮质类固醇除外;
14. 人类免疫缺陷病毒抗体、梅毒螺旋体抗体、丙型肝炎病毒抗体中任何一项阳性者均需排除。或存在需要治疗的具有临床意义的活动性乙型肝炎感染者:乙肝表面抗原[HBsAg]或乙肝核心抗体[HBcAb]阳性,且乙肝病毒脱氧核糖核酸[HBV-DNA]检测结果大于等于各医院参考值上限者;
15. 妊娠或哺乳期女性;或筛选时,育龄妇女血妊娠试验呈阳性者;或育龄期女性及其配偶不愿意在临床试验期间及结束后 7 个月内采取有效避孕措施者;
16. 研究者认为不适合入组或可能因为其他原因而不能完成本试验者。
研究者信息
1、主要研究者信息
姓名:唐金海
学位:医学博士
职称:主任医师
单位名称:江苏省人民医院(南京医科大学第一附属医院)
姓名:江泽飞
学位:医学博士
职称:教授
单位名称:中国人民解放军第三 O 七医院(军事医学科学院附属医院)
2、各参加机构信息
序号
机构名称
(主要)研究者
国家
省(州)-城市
1
江苏省人民医院(南京医科大学第一附属医院)
唐金海
中国
江苏省-南京市
2
中国人民解放军第三 O 七医院
江泽飞
中国
北京市-北京市
3
北京医院
张永强
中国
北京市-北京市
4
北京大学首钢医院
莫雪莉
中国
北京市-北京市
5
承德医学院附属医院
李青山
中国
河北省-承德市
6
哈尔滨医科大学附属肿瘤医院
张清媛
中国
黑龙江省-哈尔滨市
7
山东省肿瘤医院
王永胜
中国
山东省-济南市
8
青岛大学附属医院
王海波
中国
山东省-青岛市
9
济宁医学院附属医院
王军业
中国
山东省-济宁市
10
郑州大学第一附属医院
樊青霞
中国
河南省-郑州市
11
安徽医科大学第一附属医院
顾康生
中国
安徽省-合肥市
12
浙江大学医学院附属第二医院
邓甬川
中国
浙江省-杭州市
13
南昌市第三医院
曹亚丽
中国
江西省-南昌市
14
华中科技大学同济医学院附属协和医院
程晶
中国
湖北省-武汉市
15
襄阳市第一人民医院
文欣轩
中国
湖北省-襄阳市
16
湘潭市第一人民医院
张海明
中国
湖南省-湘潭市
17
南京军区福州总医院
陈曦
中国
福建省-福州市
18
广西医科大学第一附属医院
钟进才
中国
广西省-南宁市
19
东莞市人民医院
贾筠
中国
广东省-东莞市
20
佛山市第一人民医院
庞丹梅
中国
广东省-佛山市
21
吉林省肿瘤医院
程颖
中国
吉林省-长春市
22
辽宁省肿瘤医院
孙涛
中国
辽宁省-沈阳市
23
浙江省肿瘤医院
王晓稼
中国
浙江省-杭州市
24
安徽省立医院
潘跃银
中国
安徽省-合肥市
25
大连医科大学附属第二医院
张阳
中国
辽宁省-大连市
26
西安交通大学第一附属医院
杨谨
中国
陕西省-西安市
27
四川大学华西医院
李梅
中国
四川省-成都市
28
吉林大学第一医院
李薇
中国
吉林省-长春市
29
襄阳市中心医院
易铁男
中国
湖北省-襄阳市
30
云南省肿瘤医院
唐一吟
中国
云南省-昆明市
31
河南省肿瘤医院
闫敏
中国
河南省-郑州市
32
湖南省肿瘤医院
欧阳取长
中国
湖南省-长沙市
33
中南大学湘雅医院
王守满
中国
湖南省-长沙市
34
江西省肿瘤医院
吴毓东
中国
江西省-南昌市
35
徐州市中心医院
孙丽
中国
江苏省-徐州市
36
烟台毓璜顶医院
张良明
中国
山东省-烟台市
37
中山大学附属第一医院
林颖
中国
广东省-广州市
38
中山大学孙逸仙纪念医院
姚和瑞
中国
广东省-广州市
39
上海市第一人民医院
李琦
中国
上海市-上海市
40
北大医疗鲁中医院
陈小华
中国
山东省-淄博市
41
重庆市肿瘤医院
曾晓华
中国
重庆市-重庆市
42
唐山市人民医院
王晓红
中国
河北省-唐山市
43
首都医科大学附属北京友谊医院
曹邦邦
中国
北京市-北京市
44
柳州市人民医院
罗展雄
中国
广西省-柳州市
45
北京肿瘤医院
李惠平
中国
北京市-北京市
46
湖北省肿瘤医院
吴新红
中国
湖北省-武汉市
47
福建医科大学附属协和医院
许春森
中国
福建省-福州市
48
济南市中心医院
孙玉萍
中国
山东省-济南市
49
江苏省肿瘤医院
张莉莉
中国
江苏省-南京市
50
浙江大学医学院附属第一医院
傅佩芬
中国
浙江省-杭州市
51
广东医科大学附属第一医院
张英
中国
广东省-湛江市
52
上海交通大学医学院附属瑞金医院
沈坤炜
中国
上海市-上海市
53
四川省肿瘤医院
李卉
中国
四川省-成都市
54
德阳市人民医院
贾新建
中国
四川省-德阳市
55
西南医科大学附属医院
文庆莲
中国
四川省-泸州市
56
蚌埠医学院第一附属医院
钱军
中国
安徽省-蚌埠市
57
泰州市人民医院
黄河
中国
江苏省-泰州市
58
内江市第二人民医院
王绪娟
中国
四川省-内江市
59
河北大学附属医院
臧爱民
中国
河北省-保定市
60
长治医学院附属和平医院
武建军
中国
山西省-长治市
61
沧州市人民医院
石金升
中国
河北省-沧州市
62
邢台市人民医院
孔祥顺
中国
河北省-邢台市
63
河南科技大学第一附属医院
姚俊
中国
河南省-洛阳市
64
内江市第一人民医院
唐树彬
中国
四川省-内江市
65
赣州市人民医院
郭小青
中国
江西省-赣州市
66
宜春市人民医院
陈金平
中国
江西省-宜春市
67
宁夏医科大学总院
刘新兰
中国
宁夏省-银川市
68
云南省第一人民医院
孙建伟
中国
云南省-昆明市
69
赣南医学院第一附属医院
谢瑞莲
中国
江西省-赣州市
70
南通大学附属医院
郭小青
中国
江苏省-南通市
71
粤北人民医院
黄湛
中国
广东省-韶关市




























 首页
首页 咨询
咨询 方舟新药
方舟新药 营养商城
营养商城