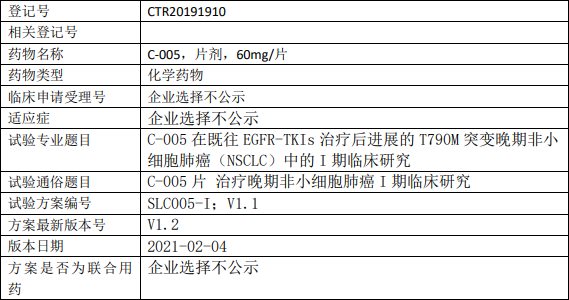
C-005临床试验,C-005片治疗晚期非小细胞肺癌I期临床试验
1、试验目的
主要目的:评价 C-005 在既往使用一代或二代 EGFR-TKI 耐药后产生 T790M 突变的晚期 NSCLC 患者的安全性和耐受性;确定 C-005 在携带 EGFR 突变的局部晚期或转移性 NSCLC 患者的 MTD(剂量递增阶段),及在确定的推荐剂量水平上的疗效(扩大入组阶段),为后续的临床试验给药剂量提供依据。
次要目的:考察 C-005 及其可能的主要代谢产物在 NSCLC 患者的 PK 特征。
2、试验设计
试验分类:安全性和有效性
试验分期:I 期
设计类型:单臂试验
随机化:非随机化
盲法:开放
试验范围:国内试验
3、受试者信息
年龄:18 岁(最小年龄)至 75 岁(最大年龄)
性别:男+女
健康受试者:无
入选标准
1.年龄 18-70 岁(含边界),扩大入组阶段可放宽至 75 岁(含边界),性别不限;
2.ECOG 全身状态(PS)0~1 分,扩大入组阶段可放宽至 2 分;
3.预期生存期不少于 3 个月;
4.组织学或细胞学确诊,且不适合手术或放疗的局部晚期或转移性 NSCLC,根据 IASLC 2015 年第八版肺癌 TNM 分期为 IIIB 至 IV期;
5.存在 EGFR 敏感突变(19 外显子缺失、21 外显子 L858R 或 L861R突变等)或符合 Jackman 标准,且经第一代或第二代 EGFR-TKI 治疗后出现疾病进展(有影像学依据),并且在剂量递增阶段接受既往采用组织或血液检测出的 EGFR T790M 突变,或获取组织或血液样本,经临床研究中心或中心实验室检测出 EGFR T790M 突变;在扩大入组阶段仅接受获取 EGFR TKIs 治疗疾病进展后的组织,经中心实验室检测 EGFR T790M 突变的患者,如无法获得组织,可采用血液检测;
6.患者至少有一个根据 RECIST 1.1 版标准判断的可测量病灶,即CT 或 MRI 显示最长径至少 10 mm,若 CT 扫描层厚>5 mm,病灶直径最小为层厚的 2 倍(可接受入组前 28 天内的检查结果);
7.允许病情稳定、研究治疗开始前不需要使用类固醇药物治疗满
4 周的无症状脑转移者;
8.入组前符合下列实验室检查结果:
骨髓储备基本正常:中性粒细胞绝对计数(ANC)≥1.5×10^9/L(1500/mm3),血小板≥90×10^9/L,以及血红蛋白≥90 g/L;
肝脏功能基本正常:总胆红素≤1.5×ULN(正常值上限);ALT 和 AST ≤2.5×ULN,如有肝转移,则总胆红素≤3×ULN,ALT 和 AST≤5×ULN;
肾功能正常:肌酐≤1.5×ULN 或 24 小时肌酐清除率≥55 mL/min(采用标准的 Cockcroft -Gault 公式);
凝血功能基本正常:INR≤1.5×ULN,APTT ≤1.5×ULN;
9.有生育能力的合格患者(男性或女性)必须同意在试验期间和末次给药后 3 个月内采用一种经医学认可的物理避孕措施(如宫内节育器、避孕套、输卵管或输精管结扎等);育龄期女性患者研究入组前 7 天内血清或尿 HCG 检查必须为阴性;
10.自愿参加本次临床试验,理解研究程序且已签署知情同意。
排除标准
1.研究药物首次给药前 14 天内接受了化疗、靶向治疗(EGFR-TKI参考排除标准第 2 条)或其他抗肿瘤药物治疗;
2. 研究药物治疗前 7 天内使用了 EGFR-TKI 治疗(例如:吉非替尼、厄洛替尼),曾使用第 3 代 EGFR-TKI(如 AZD9291、艾维替尼和艾氟替尼等);
3. 研究药物首次给药前,上一次治疗的毒性反应尚未恢复到 1 级或以下(根据 NCI CTCAE V5.0),其中脱发除外;4. 曾对唯一靶病灶进行过放疗(放疗后该病灶出现明确进展者除外),或研究药物首次给药前 2 周内接受过局部姑息性放疗(针对骨痛的放疗除外);
5. 研究药物首次给药前 4 周内接受过重大外科手术或伤口未完全愈合,或在研究期间计划进行大手术;
6. 正在参加其他干预性临床研究或距离前一项干预性临床研究结束不满 4 周;
7. 经研究者判断在研究期间可能会需要同步接受其他抗肿瘤治疗;
8. 正在服用任何已知抑制或诱导 CYP3A4 或 CYP2C8 活性的药物或中草药(可在距离研究药物首次给药前 1 周停用的除外);
9. 已知对同类药物或研究药物的任何组分(包括活性成分和非活性辅料)过敏;
10. 存在可能明显影响口服药物吸收、分布、代谢或排泄的一种或多种因素,例如难以控制的恶心和呕吐、吞咽困难等;
11. 受试者五年内患有其他原发恶性肿瘤,以下情况除外:治愈的基底细胞癌或皮肤鳞癌;宫颈原位癌;浅表膀胱癌;肿瘤治愈且已达到 5 年及以上无疾病生存;
12. 心脏功能存在任何下述情况:左心室射血分数(LVEF)<50%;静息心电图 QTcF 男性≥450ms,女性≥470ms(若异常,则取 3 次的平均值判断合格性);各种有临床意义的心律、传导、静息 ECG形态异常,例如完全性左束支传导阻滞,III 度传导阻滞,II 度传导阻滞,PR 间期>250ms;存在可能增加 QTcF 延长风险或心律失常事件风险的因素,如低钾血症、先天性长 QT 综合征、或家族史中一级亲属有长 QT 综合征或不到 40 岁就不明原因猝死,或需要服用任何可能延长 QT 间期的合并用药;按 NYHA 标准,III~IV级心功能不全;
13. 存在间质性肺病、药物诱导的间质性肺病、需要类固醇治疗的放射性肺炎的既往病史,或者任何临床活动性间质性肺病的迹象;
14. 药物治疗控制不佳的慢性系统性合并疾病(如高血压,糖尿病,甲状腺疾病,慢性肺部、肝脏、肾脏或心脏疾病);
15. 具有脾脏和胸腺疾病病史者,及自身免疫性疾病患者(包括器官特异性和系统性自身免疫病);
16. 处于急性感染期并需要药物治疗;
17. HIV 抗体、梅毒螺旋体特异抗体(TPHA)、HCV 抗体检测阳性;乙肝表面抗原(HBsAg)阳性且 HBV DNA 病毒拷贝数阳性;
18. 有严重的眼睛疾病;
19. 既往有明确的神经或精神障碍史;
20. 有精神类药物滥用或吸毒史;
21. 妊娠或哺乳期妇女;
22. 研究者认为不适合参加本研究的其他情况;
23. 存在已知的 C797S、Ex20ins 耐药突变,或 c-Met 扩增;
24. 存在 EGFR G719X 或 L861Q 突变。
研究者信息
1、主要研究者信息
| 姓名 | 学位 | 职称 | 单位名称 |
| 郑莉 | 医学博士 | 主任医师 | 四川大学华西医院 |
| 田攀文 | 医学博士 | 副主任医师 | 四川大学华西医院 |
2、各参加机构信息
| 序号 | 机构名称 | (主要)研究者 | 国家 | 省(州)-城市 |
| 1 | 四川大学华西医院 | 郑莉 | 中国 | 四川省-成都市 |
| 2 | 四川大学华西医院 | 田攀文 | 中国 | 四川省-成都市 |
| 3 | 中南大学湘雅三医院 | 阳国平,曹培国 | 中国 | 湖南省-长沙市 |
| 4 | 浙江省台州医院 | 吕冬青 | 中国 | 浙江省-台州市 |
| 5 | 杭州市第一人民医院 | 马胜林 | 中国 | 浙江省-杭州市 |
| 6 | 天津医科大学总医院 | 钟殿胜 | 中国 | 天津市-天津市 |
| 7 | 哈尔滨医科大学附属肿瘤医院 | 于雁 | 中国 | 黑龙江省-哈尔滨市 |
| 8 | 德阳市人民医院 | 陈兆红,张标 | 中国 | 四川省-德阳市 |
| 9 | 济南市中心医院 | 孙美丽,温清 | 中国 | 山东省-济南市 |




























 首页
首页 咨询
咨询 方舟新药
方舟新药 营养商城
营养商城