

根据世界卫生组织2023年最新统计,全球每年新增肝癌病例约98万例,其中约30%为早期患者,值得关注的是,随着精准医疗技术的发展,早期肝癌五年生存率已从20世纪90年代的35%提升至目前的70%以上(数据来源:《柳叶刀·肿瘤学》2023年刊)。
手术成功仅仅是抗癌征程的一个重要节点,术后的康复与护理同样至关重要。
根据最新的临床研究数据,早期肝癌患者在经过根治性手术治疗后,五年生存率可达70%以上,这一数据不仅为患者带来了希望,也凸显了术后规范管理和科学护理的重要性。

2025年2月24日,全球肿瘤医生网联合上海馨心医学科技发展基金会特别邀请福建医科大学附属协和医院血液科主任医师--许贞书教授,主治医师--徐淑娟教授为病友们深度解读针对多发性骨髓瘤的多种创新治疗方式!
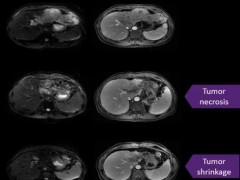
近日,FDA传来喜讯,批准来恩生物新型mRNA编码的T细胞受体(TCR)-T细胞治疗产品Liocyx-M004,启动国际多中心2期临床试验。
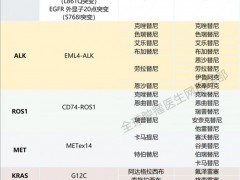
2024年,多款火遍癌友圈的明星药物及新技术因疗效显著获得突破性治疗指定及优先审批,值得肺癌病友期待,其中一些即将在2025年上市。
早期肺癌术后五年生存率达100%,意味着在统计范围内所有患者均存活超过五年。但这一数据存在两大误区......
在癌症治疗领域,“五年生存率”常被视为评估疗效的核心指标,这一概念并非指患者仅能存活五年,而是统计患者在确诊后经过治疗存活超过五年的比例。
注射用芦康沙妥珠单抗(SKB264)是靶向人滋养层细胞表面抗原2(TROP-2,在多种上皮来源肿瘤中高表达)的抗体偶联药物(ADC)药物,其偶联方式和毒素小分子具有自主知识产权,拟用于恶性实体瘤的治疗。
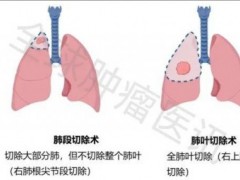
小编根据最新数据,整理了一份“在肺癌治疗领域表现突出、五年生存率数据较为可观的国内外医院榜单”(注:排名不分先后),以供肺癌患者及家属参考,大家可以先收藏以备不时之需!
美国临床肿瘤学会(ASCO)统计显示,约3%-5%的早期胃癌患者术后出现局部复发,多因切缘残留或淋巴管侵袭未被检出。
KN026是由津曼特生物从康宁杰瑞引进的创新HER2双特异性抗体,它能够同时靶向 HER2 蛋白的两个不同的活性区域。

胃癌患者有救了!中国首创Claudin18.2 CAR-T舒瑞基奥仑赛注射液中国胃癌关键II期临床试验取得初步阳性结果,基于此,预计将于2025年上半年向国家药品监督管理局(NMPA)提交上市申请!

全球肿瘤医生网医学部为大家奉上《2025年胃癌抗癌宝典》,包含了治疗方案盘点、2025即将上市的新药新技术和康复指导,请大家收藏,无论您处在胃癌治疗的哪个阶段,这份报告都将给您带来全新的生存机遇!

2024年12月31日,胃癌患者迎来了一个振奋人心的好消息,全球首款CLDN18.2的IgG1单抗——佐妥昔单抗,终于获得中国国家药品监督管理局(NMPA)批准上市,与含氟尿嘧啶类和铂类药物化疗联合,用于CLDN18.2阳性、HER2(人表皮生长因子受体2)阴性的局部晚期不可切除或转移性胃或胃食管交界处(GEJ)腺癌的一线治疗。
TQB3909是一款BCL-2抑制剂。B细胞淋巴瘤2(BCL-2)是细胞凋亡的关键蛋白质调节剂,其蛋白家族于内源性细胞凋亡通路上起重要把关作用。
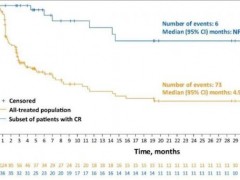
全球肿瘤医生网医学部为大家奉上《2025年淋巴瘤抗癌宝典》,包含了治疗方案盘点、2025即将上市的新药新技术和康复指导,请大家收藏,无论您处在淋巴瘤治疗的哪个阶段,这份报告都将给您带来全新的生存机遇!
U16注射液是上海优卡迪智造生命科技有限公司(以下简称“优卡迪”)自主研发的一款针对非霍奇金淋巴瘤的CAR-T细胞治疗产品。
LUCAR-20SP细胞制剂是一种靶向CD20的通用型CAR-T疗法,主要用于治疗复发或难治B细胞非霍奇金淋巴瘤。
CN201是一种靶向CD3/CD19的双特异性抗体,CD3分子广泛分布于成熟T细胞表面的膜抗原,与T细胞抗原识别受体(TCR)组合成复合受体分子激活T细胞,实现T细胞重定向。
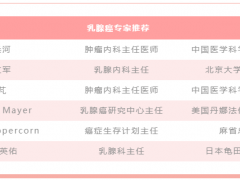
全球肿瘤医生网医学部为大家奉上《2025年乳腺癌抗癌宝典》,包含了治疗方案盘点、2025即将上市的新药新技术和康复指导,请大家收藏,无论您处在乳腺癌治疗的哪个阶段,这份报告都将给您带来全新的生存机遇!
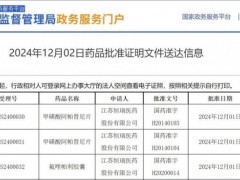
据中国国家药品监督管理局(NMPA)官网最新公示,就在今天(2024年12月2日),江苏恒瑞医药自研的两款抗癌新药——甲磺酸阿帕替尼、氟唑帕利胶囊的新适应症上市申请,已获得中国国家药品监督管理局(NMPA)批准,适用于伴有胚系BRCA突变的HER2阴性乳腺癌(氟唑帕利胶囊单药或联合甲磺酸阿帕替尼)。

2024年11月27日,我国第一款国产TROP2 抗体偶联药物(ADC)——芦康沙妥珠单抗,获中国药品监督管理局(NMPA)批准上市!

在接受了新型个体化免疫疗法后,3名患者肿瘤显著缩小,其中2名患者在6个月和10个月内获得了部分缓解。
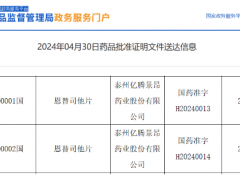
2024年4月24日,中国国家药品监督管理局(NMPA)正式批准恩替司他片(恩替诺特/Entinostat、景助达)亿腾景昂开发的1类创新药恩替司他片(恩替诺特/Entinostat、景助达)联合芳香化酶抑制剂用于治疗激素受体(HR)阳性、人类表皮生长因子受体-2(HER-2)阴性,经内分泌治疗复发或进展的局部晚期或转移性乳腺癌患者。



