时间:2019-01-16 10:12 编辑:全球肿瘤医生网
2019年1月14日,Exelixis公司宣布,美国食品和药物管理局(FDA)批准CABOMETYX(卡博替尼,cabozantinib)片剂用于先前接受过索拉非尼治疗的肝细胞癌(HCC)患者。

Exelixis总裁兼首席执行官Michael M. Morrissey博士说,CABOMETYX的新适应症的获批无疑是侵袭性肝细胞癌(HCC)治疗进展的重要里程碑,我们将继续探索CABOMETYX如何使除肾细胞癌以外的难以治疗的癌症患者受益。
FDA对CABOMETYX的批准是基于CABOMTIY的CELESTIALIII期临床研究,对先前接受索拉非尼治疗的晚期HCC患者的结果。与安慰剂相比,CABOMETYX在总生存期(OS)方面表现出具有统计学意义和临床意义上的改善。
关于CELESTIAL研究
CELESTIAL研究是一项全球双盲的,将卡博替尼用于经索拉非尼治疗的晚期肝癌患者的二线及二线以上治疗的III期临床研究。患者2:1随机分配接受卡博替尼(60 mg qd) 或安慰剂治疗。
入组标准包括:病理确诊为HCC,Child-Pugh A级,ECOG PS 评分1,既往需接受过索拉非你治疗。既往接受过2线系统性治疗的患者,最后一线治疗需进展。主要研究终点为总生存期。次要终点包括PFS(无进展生存期)和ORR(客观缓解率价)。
入组 | 中位OS(月) | 中位PFS(月) | ORR(%) |
卡博替尼(470人) | 10.2 | 5.2 | 4.0 |
安慰剂(237人) | 8.0 | 1.9 | 0.4 |
结果显示,在既往接受过索拉非尼治疗的晚期HCC患者中,卡博替尼相比安慰剂,显著改善OS和PFS。不良事件报道与卡博替尼既往的安全性数据一致。试验数据于2018年1月在2018年美国临床肿瘤学会胃肠癌研讨会(ASCO-GI)上发表,于2018年7月在《新英格兰医学杂志》上发表。
关于CABOMETYX(cabozantinib)
卡博替尼(XL184),俗称184,卡博替尼是多靶点酪氨酸激酶抑制剂,靶点众多。据报道,184的靶点包括MET、VEGFR1/2/3、ROS1、RET、AXL、NTRK、KIT,至少有9个,应该是靶点最多的抗癌药了。
提示:只有通过基因检测,找到靶点,才能选对靶向药进行个体化治疗!
其中靶点MET和AXL 2与预后不良相关,也与索拉非尼耐药机制相关。也许正因此,卡博替尼的III期临床研究CELESTIAL研究才获得了一个良好的结果。从这项研究可以预测,未来肝癌的二线及二级以上治疗,可以继续寻找索拉非尼的耐药机制,也可以考虑联合治疗等等。
目前,FDA已经批准卡博替尼用于复发难治的晚期甲状腺髓样癌和索坦治疗失败的晚期肾癌。
根据JCO发表的临床数据,184在肾癌一线治疗中刷新了历史数据新高,PK肾癌一线用药舒尼替尼(索坦)完胜。
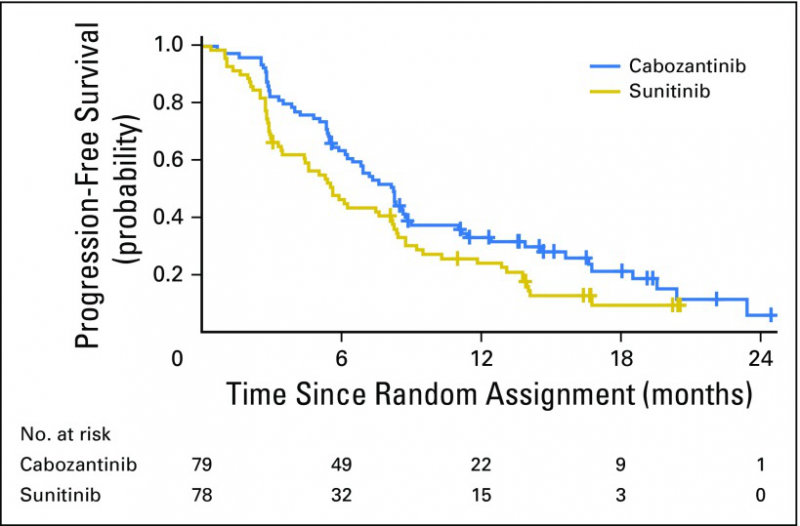
临床设计:招募157位晚期初诊的肾癌患者,一线使用184(79人)或者舒尼替尼(78人)。184剂量每天60mg;舒尼替尼剂量每天50mg,用药4周,停药2周。
临床数据:184(蓝色) VS 舒尼替尼(黄色),无进展生存率46% VS 18%,无进展生存期8.2个月 VS 5.6个月,OS为30.3个月 VS 21.8个月。具体临床数据如下:
卡博替尼尚在临床试验的适应症还包括:肝癌、软组织肉瘤、非小细胞肺癌、前列腺癌、乳腺癌、卵巢癌、肠癌等,新一代神奇光谱抗癌药的桂冠非卡博替尼莫属!
肝癌专家推荐
黎功
北京清华长庚医院
主任医师教授 硕士生导师
患者朋友在线咨询抗癌技术、药品或专家,或加入各大癌症病友群,可登录。
患者朋友在线咨询抗癌技术、本文介绍的药品或申请专家咨询,或想加入各大癌症病友群,请点击下图链接。

本网站新闻资讯、文章、研究数据、治疗案例均来自于国内外医学论文,所涉及到的新药、新技术有可能还处于临床研究阶段,患者不能作为治疗疾病的依据。癌症治疗目前尚无治愈手段,患者需要在医生的指导下,在医院接受正规治疗或参加新药新技术临床试验。